Ketene
| Ketene |
 Allgemeine Struktur |
Struktur der Stammverbindung Keten |
Ketene (Betonung auf der zweiten Silbe: Ketene) sind eine Gruppe organischer Verbindungen mit der allgemeinen Formel RR'C=C=O. R und R' können beliebige Reste sein. Ethenon (=Keten) ist der einfachste Vertreter dieser Stoffgruppe mit der Formel H2C=C=O. Ketene sind sehr reaktiv, fast alle dimerisieren sofort zum entsprechenden Diketen. Ketene sind formal innere Anhydride der entsprechenden Carbonsäuren.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Ketene wurden zuerst von Hermann Staudinger 1905 in Form von Diphenylketen entdeckt (Umsetzung von -Chlordiphenylacetylchlorid mit Zink) und systematisch untersucht.[1] Inspiriert war er von den ersten Beispielen reaktiver organischer Zwischenprodukte und stabiler Radikale, die Moses Gomberg 1900 entdeckte (Verbindungen mit Triphenylmethylgruppe). Staudinger fand mit den Ketenen eine neue derartige Stoffklasse.[2]
Herstellung
[Bearbeiten | Quelltext bearbeiten]Industriell erzeugt man Keten durch katalytische Hochtemperatur-Pyrolyse von Aceton oder Essigsäure bei 700 °C.
- Ketensynthese durch Pyrolyse von Aceton. Als Nebenprodukt entsteht Methan.
Allgemein sind Ketene durch Umsetzung von Carbonsäurehalogeniden, die mindestens einen α-ständigen Wasserstoff tragen, mit Basen wie Triethylamin in situ zugänglich:[3]
Ketene können auch durch eine Wolff-Umlagerung entstehen.
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Ketene sind durch ihre kumulierten Doppelbindungen sehr reaktionsfreudig.[4]
Bildung von Carbonsäureestern
[Bearbeiten | Quelltext bearbeiten]Durch Reaktion mit Alkoholen entstehen Carbonsäureester:
Bildung von Carbonsäureanhydrid
[Bearbeiten | Quelltext bearbeiten]Ein Keten reagiert mit einer Carbonsäure zu einem Carbonsäureanhydrid:
Bildung von Carbonsäureamiden
[Bearbeiten | Quelltext bearbeiten]Ketene reagieren mit Ammoniak zu primären Amiden:
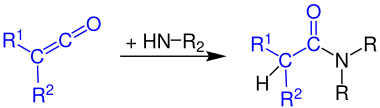
Bei der Reaktion von Ketenen mit primären Aminen entstehen sekundäre Amide:
Ketene reagieren mit sekundären Aminen zu tertiären Amiden:
Hydrolyse
[Bearbeiten | Quelltext bearbeiten]Durch Reaktion mit Wasser entstehen aus Ketenen Carbonsäuren:
Bildung von Enolacetaten
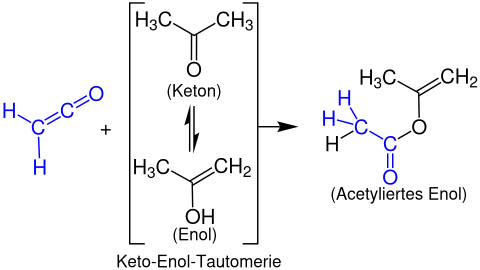
[Bearbeiten | Quelltext bearbeiten]Mit enolisierbaren Carbonylverbindungen entstehen aus Ketenen Enolacetate. Das folgende Beispiel zeigt die Reaktion von Ethenon mit Aceton unter Bildung eines Propen-2-yl-acetats:
Dimerisierung
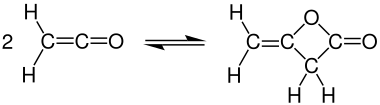
[Bearbeiten | Quelltext bearbeiten]Bei Raumtemperatur dimerisiert Keten schnell zu Diketen, kann jedoch durch Erhitzen wiedergewonnen werden:
[2+2]-Cycloaddition
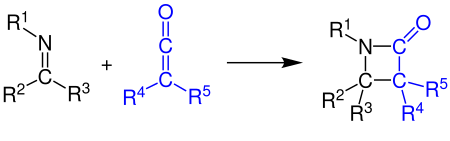
[Bearbeiten | Quelltext bearbeiten]Ketene können u. a. mit Alkenen, Carbonylverbindungen, Carbodiimiden und mit Iminen unter [2+2]-Cycloaddition reagieren. Das Beispiel zeigt die Synthese eines β-Lactams durch die Reaktion von einem Keten mit einem Imin (Siehe Staudinger-Synthese):[5][6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Staudinger, Ketene, eine neue Körperklasse. Berichte der deutschen chemischen Gesellschaft, Band 38, 1905, S. 1735–1739.
- ↑ Thomas T. Tidwell, The first century of Ketenes (1905-2005): the birth of a family of reactive intermediates, Angewandte Chemie, Int. Edition, Band 44, 2005, S. 5778–5785.
- ↑ Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 410, ISBN 3-342-00280-8.
- ↑ Siegfried Hauptmann: Organische Chemie: mit 65 Tabellen. Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-87144-902-4, S. 410–412.
- ↑ Jie Jack Li: Name reactions. A collection of detailed reaction mechanisms. 3. Auflage. Springer-Verlag, Berlin 2006, ISBN 978-3-540-30030-4, S. 561–562, doi:10.1007/3-540-30031-7.
- ↑ Hermann Staudinger: Zur Kenntnis der Ketene. Diphenylketen. In: Justus Liebigs Annalen der Chemie. Band 356, Nr. 1–2. John Wiley & Sons, Inc., 1907, S. 51–123, doi:10.1002/jlac.19073560106.