Perfluorcuban
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
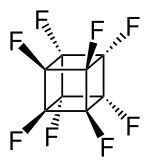
| ||||||||||
| Allgemeines | ||||||||||
| Name | Perfluorcuban | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C8F8 | |||||||||
| Kurzbeschreibung |
sublimierbarer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 248,075 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
2,429 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Perfluorcuban (auch Octafluorcuban) ist eine fluororganische Verbindung mit der Summenformel C8F8. Wie Cuban besteht sie aus acht Kohlenstoffatomen, die zu einem Würfel verbunden sind, wobei an jeder Ecke des Kohlenstoffwürfels ein Fluoratom gebunden ist. Es ist ein farbloser Feststoff, der bei Raumtemperatur sublimiert.
Die Verbindung wurde von den Lesern der Chemical & Engineering News zum „Molekül des Jahres 2022“ gewählt.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Es war wegen seiner ungewöhnlichen Elektronenstruktur seit langem nur von theoretischem Interesse, da sich das freie ungepaarte Elektron nach der Reduktion zum C8F8−1-Anion überwiegend im Inneren des Würfels befindet. Laut Röntgenkristallographie sind die C–C-Abstände mit 1,572 Å in Octafluorcuban identisch lang wie die des Ausgangs-Cubans.[2]
Perfluorcuban ist zwar definitionsgemäß kein PFAS, ist aber wie diese sehr persistent in der Umwelt.[5]
Synthese[Bearbeiten | Quelltext bearbeiten]
Das Molekül wurde 2022 synthetisiert, indem es in mehreren Schritten aus einem Cubancarbonsäureester hergestellt wurde. Eine Lösung des Cubanmonoesters wird in 1,2-Dichlor-3-(2-chlor-1,1,2,2-tetrafluorethoxy)-1,1,2,3,3-pentafluorpropan (CFE-419) angefertigt. Diese wird bei 20 °C mit einem Überschuss an Fluorgas behandelt, was zur Bildung des Heptafluorcubanmonoesters mit einer durchschnittlichen Ausbeute von 15 % führt. Der Ester wird anschließend ohne weitere Isolierung in situ einer Umesterung unterzogen, wodurch Benzylheptafluorcubancarboxylat als Produkt anfällt. Bei der Hydrolyse des Esters führt eine anschließende Decarboxylierung zu Heptafluorcuban mit einer Ausbeute von 76 %.[2]
Um das Octafluorcuban zu erhalten, wird Heptafluorcuban mit Lithium-bis(trimethylsilyl)amid und N-Fluorbenzolsulfonimid in Tetrahydrofuran bei Temperaturen von −78 °C umgesetzt, was zu einer Ausbeute von etwa 51 % führt.[2]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b Derek Low: Perfluorocubane Is (As You Would Expect) Weird, Science Blogs, 2022.
- ↑ a b c d M. Sugiyama, M. Akiyama, Y. Yonezawa, K. Komaguchi, M. Higashi, K. Nozaki, T. Okazoe: Electron in a cube: Synthesis and characterization of perfluorocubane as an electron acceptor. In: Science. Band 377, 2022, S. 756–759, doi:10.1126/science.abq0516.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Leigh Krietsch Boerner: Check out C&EN’s molecules of the year for 2022, Chemical & Engineering News, 2022.
- ↑ Hannah Flerlage, J. Chris Slootweg: Modern chemistry is rubbish. In: Nature Reviews Chemistry. 2023, doi:10.1038/s41570-023-00523-9.