Puromycin
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
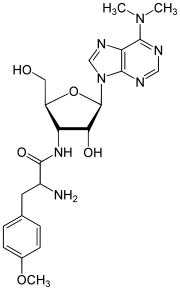
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Puromycin (vorgeschlagener INN)[1] | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C22H29N7O5 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 471,51 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
mäßig in Wasser (50,3 g·l−1 bei 25 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Puromycin, auch Purimycin, ist ein aus Streptomyceten (Streptomyces alboniger) isoliertes Nukleosid-Antibiotikum, welches die Protein-Biosynthese hemmt und damit gegen einige Tumoren, Amöben, Trypanosomen und Würmer wirksam ist. Da es auch für den Menschen giftig ist, wird es vor allem bei Experimenten in der Mikrobiologie und der Zellbiologie eingesetzt. Strukturell leitet es sich von Adenosin bzw. von N6,N6-Dimethyladenosin ab.
Wirkung
[Bearbeiten | Quelltext bearbeiten]Puromycin wirkt auf zweierlei Weisen:
- Termination der Translation: Puromycin inhibiert die Translation, indem es eine verfrühte Termination einleitet.[4] Dies geschieht dadurch, dass sich das Puromycin während des Peptidyltransfers anstatt einer Tyrosyl-tRNA an die Eingangsstelle (A-Stelle) des Ribosoms bindet. Ein Teil des Moleküls ähnelt dabei dem 3’-Ende (CCA) der Aminoacyl-tRNAs. Aus diesem Grund wird die sich in der Elongation befindliche Polypeptidkette auf den Pseudoaminosäurearm des Puromycins übertragen und es kommt zu einer verfrühten Termination der Translation.
- Inhibierung des Proteinimportes: Puromycin hemmt den Proteinimport in Mitochondrien, indem es eine intramitochondriale, ATP-abhängige Reaktion behindert.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Puromycin wird ausschließlich für Forschungszwecke verwendet.[5] Aufgrund seiner toxischen Wirkung auch auf eukaryotische Zellen ist es für therapeutische Zwecke nicht geeignet. Puromycin stellt damit einen Grenzfall zwischen Antibiotikum und Toxin dar.
Mögliche Anwendungen in der Forschung sind die Selektion genetisch veränderter Zelllinien sowie die Inhibition sogenannter Puromycin-sensitiver Aminopeptidasen. Auch andere Aminopeptidasen werden von Puromycin mit unterschiedlich starker Wirkung inhibiert.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Puromycin dihydrochloride bei Fermentek (englisch)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ INN Proposed List 15, World Health Organisation (WHO), 9. Oktober 1965.
- ↑ a b c Eintrag zu Aspirin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ a b Datenblatt Puromycin dihydrochloride from Streptomyces alboniger bei Sigma-Aldrich, abgerufen am 22. April 2011 (PDF).
- ↑ M. A. Darken: Puromycin inhibition of protein synthesis. In: Pharmacol. Rev. 16, 1964, S. 223–243. PMID 14211122.
- ↑ R. W. Roberts, J. W. Szostak: RNA-peptide fusions for the in vitro selection of peptides and proteins. In: Proceedings of the National Academy of Sciences. Band 94 , Nr. 23, 11. Nov 1997, S. 12297–12302. PMID 9356443.