Zanamivir
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
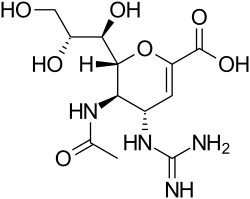
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Zanamivir | |||||||||||||||||||||
| Andere Namen |
(4S,5R,6R)-5-Acetylamino-4-guanidino-6-[(1R,2R)-1,2,3-trihydroxypropyl]-5,6-dihydro-4H-pyran-2-carbonsäure | |||||||||||||||||||||
| Summenformel | C12H20N4O7 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
Hemmung der viralen Neuraminidase, Hemmung der Freisetzung neu gebildeter Influenza A- und B-Viren | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 332,31 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Zanamivir ist der erste Arzneistoff aus der Gruppe der Neuraminidase-Hemmer, der zur Therapie der Grippe (Influenza) eingesetzt wird. Das Arzneimittel Relenza® wurde durch Biota Holdings, Australien entwickelt, es wird seit 1999 von GlaxoSmithKline vertrieben und unterliegt der ärztlichen Verschreibungspflicht.
Stand der Forschung
[Bearbeiten | Quelltext bearbeiten]Als Inhibitor der viralen Neuraminidase kann er das Freisetzen weiterer Viren und damit das Auftreten oder Fortschreiten der Erkrankung verhindern, sofern er innerhalb der ersten 48 Stunden verabreicht wird. 2014 wurden nach Untersuchungen der Cochrane Collaboration Zweifel an der Wirksamkeit und Sicherheit von Zanamivir und Oseltamivir laut.[3] Eine Metaanalyse der Cochrane Collaboration fand bei einer Behandlung mit Zanamivir bei Erwachsenen eine Verkürzung der Erkrankungsdauer von 6,6 auf 6 Tage.[3] Jedoch hatte Zanamivir keinen Einfluss auf die Häufigkeit schwerer Verlaufsformen wie Pneumonie oder Bronchitis.[3]
Anwendung
[Bearbeiten | Quelltext bearbeiten]Da Zanamivir nur zu ca. 2 % aus dem Magen-Darm-Trakt aufgenommen wird, muss es als Pulver mithilfe des Inhaliergeräts Diskhaler verabreicht werden.
Studien
[Bearbeiten | Quelltext bearbeiten]Therapie
[Bearbeiten | Quelltext bearbeiten]Die ersten klinischen Untersuchungen mit Zanamivir zur Behandlung von Infektionen mit Influenzaviren erfolgten 1994/1995.
Bei jungen Patienten mit einem Durchschnittsalter von 30 Jahren samt nachgewiesener Influenzainfektion kam es dabei zu einer Reduktion der Fieberdauer von 6,8 Tagen bei Placebogabe auf 5,2 Tage bei Verabreichung von Zanamivir, sofern dieses innerhalb von 30 Stunden nach Auftreten der Symptome eingenommen wurde. Die Dauer bis zur klinischen Besserung/Symptomfreiheit betrug in der Placebogruppe 6,3 Tage gegenüber 5,4 Tagen in der Zanamivirgruppe.
Andere Studien bestätigten diese Ergebnisse weitgehend und bescheinigen Zanamivir eine Reduktion der Fieberdauer von 6 Tagen unter Placebo auf 4,5 Tage bzw. eine Verkürzung der Dauer bis zur Symptomfreiheit um einen Tag.
In Deutschland erklärte der Bundesausschuss der Ärzte und Krankenkassen das Medikament im Jahr 2000 für entbehrlich.
Prophylaxe
[Bearbeiten | Quelltext bearbeiten]Eine randomisierte, kontrollierte Studie zeigte bei 1107 Studenten während einer Grippe-Epidemie, dass die tägliche Gabe von Relenza über einen Zeitraum von 28 Tagen zu einer Abnahme der Influenza-Erkrankungen von 6 % in der Placebogruppe auf 2 % in der Relenzagruppe führte: In der Placebogruppe erkrankten 34 von 554 und in der Zanamivir-Gruppe 11 von 553 Studienteilnehmern. Mit Fieber erkrankten in der Placebogruppe 19 Menschen, in der Zanamivir-Gruppe 3. Das bedeutet, dass pro 35 behandelte Personen eine Grippeerkrankung verhindert werden konnte.[4]
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Die häufigsten unerwünschten Arzneimittelwirkungen sind bei Personen mit Asthma bronchiale oder chronisch obstruktiver Lungenerkrankung eine mehr als 20%ige Reduktion der Lungenfunktion (FEV1 oder Peak Flow). Mitunter kam es hier auch zu schweren Bronchospasmen mit vereinzelten Todesfällen.
Diskussion
[Bearbeiten | Quelltext bearbeiten]Daten zur Wirksamkeit und Sicherheit dieser Substanz bei älteren Patienten und Risikogruppen liegen ebenso wenig vor wie eindeutige Daten zum Effekt auf die Inzidenz von Komplikationen und Todesfällen.
Über die Verwendung von Zanamivir bei Patienten mit eingeschränkter Nieren- oder Leberfunktion sowie bei Herzinsuffizienz liegen noch wenige Daten vor.
Herstellung
[Bearbeiten | Quelltext bearbeiten]Verschiedene vielstufige Synthesen für Zanamivir, ausgehend von N-Acetylneuraminsäure, sind in der Literatur beschrieben.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage. 2006, ISBN 0-911910-00-X, S. 1744.
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von Zanamivir im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 12. Juli 2020.
- ↑ a b c Tom Jefferson, Mark A Jones, Peter Doshi, Chris B Del Mar, Rokuro Hama, Matthew J Thompson, Elizabeth A Spencer, Igho Onakpoya, Kamal R Mahtani, David Nunan, Jeremy Howick, Carl J Heneghan: Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children. In: British Medical Journal, 2014, Online-Vorabveröffentlichung. doi:10.1002/14651858.CD008965.pub4.
- ↑ AS Monto, DP Robinson, ML Herlocher et al. Zanamivir in the prevention of influenza among healthy adults: a randomized controlled trial. In: JAMA, 7. Juli 1999, 282(1), S. 31–35; PMID 10404908. Volltext. jama.ama-assn.org; abgerufen am 26. September 2008.
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dietmar Reichert: Pharmaceutical Substances. 4. Auflage. 2 Bände. Thieme-Verlag, Stuttgart 2000, ISBN 1-58890-031-2; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.