Xanthon
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
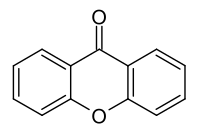
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Xanthon | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C13H8O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Nadeln[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 196,19 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
351 °C[1] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Xanthon (auch Xanthen-9-on oder Dibenzo-γ-pyron) ist eine heterocyclische chemische Verbindung, die zu den Ethern und Ketonen gehört und Namensgeber der Stoffgruppe der Xanthone ist. Das Reduktionsprodukt Xanthen bildet den Grundkörper der Xanthen-Pflanzenfarbstoffe. Es ist isomer zum Fluoron (Xanthen-3-on).
Vorkommen und Darstellung
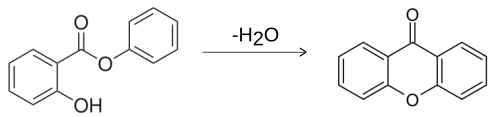
[Bearbeiten | Quelltext bearbeiten]Xanthon selbst kommt in der Natur nicht vor, jedoch etwa 200 seiner Derivate wie beispielsweise Chinonin (Mangoferin), Corymbiferin, Euxanthinsäure, Euxanthon, Gentisin und Mangostin. Die Darstellung von Xanthon erfolgt durch Destillation von Salicylsäurephenylester.
Eigenschaften und Verwendung
[Bearbeiten | Quelltext bearbeiten]Xanthon bildet farblose, leicht sublimierbare Nadeln, die von 174 bis 176 °C schmelzen und bei etwa 351 °C sieden. Es ist leicht löslich in Ethanol, Ether, Chloroform und Benzol, aber unlöslich in Wasser. In konzentrierter Schwefelsäure löst sich die Verbindung mit gelber Farbe zu einer Flüssigkeit mit intensiv hellblauer Fluoreszenz. Unter reduktiven Bedingungen lässt sich Xanthon in Xanthen und Xanthydrol überführen, durch Einwirkung von Grignard-Verbindungen entstehen Xanthyliumsalze. Die einzig bekannte Verwendung von Xanthon ist der Einsatz als spezifisches Insektizid, welches vor allem auf Larven von Motten als sogenanntes Larvizid wirkt.[7]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Eintrag zu Xanthon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 30. September 2014.
- ↑ a b Datenblatt Xanthon bei Alfa Aesar, abgerufen am 22. Januar 2010 (Seite nicht mehr abrufbar).
- ↑ a b Datenblatt Xanthone bei Sigma-Aldrich, abgerufen am 19. Juni 2023 (PDF).
- ↑ U.S. Army Armament Research & Development Command. Chemical Systems Laboratory, NIOSH Exchange Chemicals. Vol. NX#01611.
- ↑ a b Eintrag zu Xanthone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ National Academy of Sciences. National Research Council, Chemical-Biological Coordination Center, Review. Vol. 5, S. 25, 1953.
- ↑ Steiner, L. F. and S. A. Summerland. 1943. Xanthone as an ovicide and larvicide for the codling moth. Journal of economic entomology 36, 435–439.