Bariumnitrat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
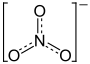
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bariumnitrat | |||||||||||||||
| Andere Namen |
Barytsalpeter | |||||||||||||||
| Summenformel | Ba(NO3)2 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 261,35 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
3,24 g·cm−3 [2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
mäßig in Wasser (90 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,5 mg·m−3[1] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−988,0 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Bariumnitrat ist ein Nitratsalz des Erdalkalimetalls Barium. Es besitzt die Formel Ba(NO3)2 und gehört zur Stoffgruppe der Nitrate.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Bariumnitrat lässt sich durch folgende chemische Reaktionen darstellen:
Eigenschaften[Bearbeiten | Quelltext bearbeiten]

Bariumnitrat tritt als farbloser kristalliner Feststoff auf. Es ist giftig und ein schwach wassergefährdender Stoff. Es verursacht in der Brennerflamme die für Barium typische grüne Flammenfärbung und kann als Oxidationsmittel benutzt werden.
Bariumnitrat zersetzt sich bei Temperaturen größer 550 °C zu Bariumoxid, Stickstoff, Sauerstoff und Stickstoffmonoxid. Aufgrund des freigesetzten Sauerstoffs und vor allem des freiwerdenden Stickstoffmonoxids ist Bariumnitrat ein gutes Oxidationsmittel.
Wasserfreies Bariumnitrat kristallisiert im kubischen Kristallsystem in der Raumgruppe Pa3 (Raumgruppen-Nr. 205) mit dem Gitterparameter a = 811,84 pm. In der Elementarzelle befinden sich vier Formeleinheiten.[5] Die Kristalle sind isotyp zu Strontiumnitrat.
Verwendung[Bearbeiten | Quelltext bearbeiten]
Bariumnitrat wird in der Pyrotechnik u. a. zur Herstellung von Wunderkerzen verwendet, in welchen es als Oxidationsmittel fungiert. Auch kommt Bariumnitrat häufig als Surrogat des Kaliumnitrats zum Einsatz, um der Flamme eine grünliche Farbe zu verleihen. Außerdem wird es als Oxidator in den Zündhütchen von Patronen und Kartuschen verwendet. Eine hochbrisante Mischung aus TNT und Bariumnitrat wird Baratol genannt.
Es wird auch in Leuchtschirmen für Fernsehempfänger benutzt.
Analytik[Bearbeiten | Quelltext bearbeiten]
Einen ersten Hinweis bei der Identifizierung von Barium in Bariumnitrat erhält man durch die grüne Flammenprobe. Das Anion kann mittels Ringprobe oder Lunges Reagenz (siehe auch Nachweise für Anionen) nachgewiesen werden.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Datenblatt Bariumnitrat bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b c d Eintrag zu Bariumnitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl aryl sulphonic acid, and of salts specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-6.
- ↑ H. Nowotny, G. Heger: Structure refinement of strontium nitrate, Sr(NO3)2, and barium nitrate, Ba(NO3)2. In: Acta Cryst. 1983, C39, S. 952–956. doi:10.1107/S0108270183006976.






