Cyansäure
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
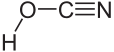
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cyansäure | |||||||||||||||
| Summenformel | HOCN | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 43,02 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Die Cyansäure ist eine instabile chemische Verbindung. Sie entsteht beim Ansäuern von Cyanaten,[2] tautomerisiert jedoch praktisch vollständig zur stabileren Isocyansäure. Eindeutig nachgewiesen werden konnte Cyansäure nach Bestrahlen von Isocyansäure mit UV-Licht (224 nm) in einer Argon- oder Stickstoff-Matrix bei 4 bzw. 20 K.[3][4] Cyansäure ist isomer zu Knallsäure.
Cyanate[Bearbeiten | Quelltext bearbeiten]
Cyanate sind die Salze mit dem Cyanat-Ion (NCO−) oder die Ester der Cyansäure mit der Struktur R–OCN.[5][6] Anorganische Cyanate wie Kaliumcyanat sind stabile wasserlösliche Verbindungen und farblos. Cyansäureester trimerisieren im Allgemeinen zu Cyanursäuretriestern.[2] Dies geschieht bei Alkylcyanaten sehr schnell (schon während der Herstellung), bei Arylcyanaten langsam.[7]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Für die freie Säure ist aufgrund ihrer Instabilität keine Anwendung bekannt. Anorganische Cyanate werden als Hilfsstoffe bei der Wärmebehandlung von Werkstoffen aus Stahl und als Ausgangsstoffe zur Herstellung von Pharmaka und Harnstoffherbiziden verwendet.[8]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. 24. Auflage. Hirzel, Stuttgart 2004, ISBN 3-7776-1221-9.
- ↑ Eintrag zu Cyansäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Juni 2014.
- ↑ Bozzano G. Luisa: Organic Functional Group Preparations: Volume 1. Academic Press, 2012, ISBN 978-0-08-092556-1, S. 362 (books.google.com).
- ↑ Ronald Rich: Inorganic Reactions in Water. Springer, 2007, ISBN 978-3-540-73962-3, S. 330 (books.google.com).
- ↑ Martin, D & Bauer, M & Pankratov, V. (2007). Cyclotrimerisation of Cyano-compounds into 1,3,5-Triazines. Russian Chemical Reviews. 47. 975. doi:10.1070/RC1978v047n10ABEH002288.
- ↑ Jürgen Falbe, Manfred Regitz: RÖMPP Lexikon Chemie, 10. Auflage, 1996-1999: Band 2: Cm - G. Georg Thieme Verlag, 2014, ISBN 978-3-13-199971-9, S. 833, 838 (books.google.com).