Dicobaltoctacarbonyl
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
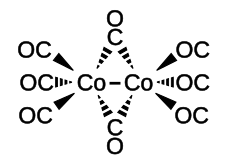
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Dicobaltoctacarbonyl | |||||||||||||||
| Summenformel | [Co2(CO)8][1] | |||||||||||||||
| Kurzbeschreibung |
orangefarbene Kristalle[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 341,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
1,78 g·cm−3 (25 °C)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
sehr schlecht in Wasser (<0,1 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Dicobaltoctacarbonyl ist ein zweikerniger Komplex, bei dem zwei Cobaltkerne von acht Carbonylliganden umgeben sind.
Darstellung[Bearbeiten | Quelltext bearbeiten]
Der Komplex kann durch die Reaktion von Cobalt(II)-Salzen (z. B. Cobalt(II)-acetat oder Cobalt(II)-carbonat) unter hohem Kohlenstoffmonoxid-Druck hergestellt werden.[5] Oftmals wird diese Reaktion in Anwesenheit von Cyanidsalzen durchgeführt.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Dicobaltoctacarbonyl ist ein orangefarbener Feststoff (größere Kristalle sind rot), der sich bei 52 °C zu Tetracobaltdodecacarbonyl [Co4(CO)12] zersetzt. Auch bei Raumtemperatur zersetzt sich der Komplex an Luft langsam unter Freisetzung von Kohlenstoffmonoxid.[2]
Der Komplex liegt im Gleichgewicht zwischen zwei Strukturen, von denen eine aus zwei trigonal-bipyramidal-koordinierten Cobaltkernen mit einer Bindung zwischen den Cobaltatomen, die andere aus einem durch zwei Carbonylliganden verbrückten Komplex besteht. Das Gleichgewicht liegt hierbei auf der Seite der verbrückten Komplexspezies. Die Bindungslänge zwischen den Cobaltkernen im verbrückten Komplex beträgt 252 pm, die Co–C-Bindung zu den terminalen Carbonylen ist 180 pm, zu den verbrückenden Carbonylen 190 pm lang.[6]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Dicobaltoctacarbonyl wird in der Pauson-Khand-Reaktion zur Synthese von Cyclopentenonen benötigt. Hierbei liefert es durch Abspaltung von zwei Carbonyliganden die Cobaltspezies, die zur Addition an das eingesetzte Alkin dient. Gleiches gilt für die Nicholas-Reaktion, zu der dieselbe Cobaltspezies benötigt wird.
Durch Hydrierung des Komplexes bildet sich der einkernige Komplex [CoH(CO)4].
Dieser Komplex wird als Katalysator für die Hydroformylierung eingesetzt. Dabei wird Dicobaltoctacarbonyl mit Wasserstoff umgesetzt, so dass Cobaltcarbonylhydrid als katalytisch wirkende Spezies entsteht.[7]
Die technische Synthese von Phenylbrenztraubensäure nutzt die Verbindung als Katalysator bei der doppelten Carbonylierung von Benzylchlorid mittels Kohlenmonoxid und Wasser.[8]
Durch Reduktion mit elementaren Alkalimetallen können [Co(CO)4]−-Ionen gebildet werden.
Literatur[Bearbeiten | Quelltext bearbeiten]
- Christoph Elschenbroich: Organometallchemie. (= Teubner-Studienbücher Chemie). 5. überarbeitete Auflage. Teubner, Wiesbaden 2005, ISBN 3-519-53501-7.
- Lutz H. Gade: Koordinationschemie. Wiley-VCH, Weinheim u. a. 1998, ISBN 3-527-29503-8.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu Cobaltcarbonyle. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Dezember 2015.
- ↑ a b c d e f g h Eintrag zu Dicobaltoctacarbonyl in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Richard P. Pohanish: Sittig's Handbook of Toxic and Hazardous Chemicals and Carcinogens, 5th Edition. William Andrew, 2008, ISBN 978-0-8155-1904-1, S. 697 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt di-Cobaltoctacarbonyl bei Merck, abgerufen am 24. März 2011.
- ↑ Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1833.
- ↑ G. G. Sumner, H. P. Klug, L. E. Alexander: The crystal structure of dicobalt octacarbonyl. In: Acta Cryst. 1964, 17, S. 732–742, doi:10.1107/S0365110X64001803.
- ↑ Christoph Elschenbroich: Organometallchemie. 6. Auflage. Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 633–637.
- ↑ W. Bertleff, M. Roeper, X. Sava: Carbonylation. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag, Weinheim 2007. doi:10.1002/14356007.a05_217.pub2
- Feuergefährlicher Stoff
- Gesundheitsschädlicher Stoff bei Verschlucken
- Hautreizender Stoff
- Sensibilisierender Stoff
- Giftiger Stoff bei Einatmen
- Stoff mit Verdacht auf krebserzeugende Wirkung
- Stoff mit Verdacht auf reproduktionstoxische Wirkung
- Gesundheitsschädlicher Stoff (Organschäden)
- Umweltgefährlicher Stoff (chronisch wassergefährdend)
- Cobaltverbindung
- Carbonylkomplex







![{\displaystyle \mathrm {[Co_{2}(CO)_{8}]\ +\ H_{2}\longrightarrow \ 2\ [CoH(CO)_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/a4f80426e35289df4aa70d29aa181a9541c9ca69)
![{\displaystyle \mathrm {[Co_{2}(CO)_{8}]\ +\ 2\ Na\longrightarrow \ 2\ Na[Co(CO)_{4}]} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b394ef88a0038694e0d2d227b0087bef2fc68f96)