Niob(V)-fluorid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
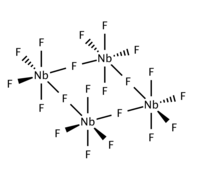
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Niob(V)-fluorid | ||||||||||||||||||
| Andere Namen |
Niobpentafluorid | ||||||||||||||||||
| Summenformel | NbF5 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 187,90 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||||||||
| Dichte |
3,293 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
233,3 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Niob(V)-fluorid ist eine anorganische chemische Verbindung des Niobs aus der Gruppe der Fluoride.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Die Erstsynthese von Niob(V)-fluorid wurde von Otto Ruff und Julian Zedner an der Technischen Hochschule Danzig durchgeführt und am 15. Januar 1909 zur Veröffentlichung eingereicht.[3]
Niob(V)-fluorid kann durch Reaktion von Niob(V)-chlorid mit Fluorwasserstoff gewonnen werden.[1]
Ebenfalls möglich ist die Darstellung aus den Elementen[1]:
sowie durch die Umsetzung von elementarem Niob mit Zinn(II)-fluorid im Stickstoffstrom bei 400 bis 500 °C[4]:
Allgemein lässt sich Niob(V)-fluorid ähnlich wie Tantal(V)-fluorid durch Fluorierung mit Fluor oder Fluorwasserstoff aus den Oxiden (Niob(V)-oxid) gewinnen.[5]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Niob(V)-fluorid ist ein farbloser, sehr hygroskopischer Feststoff[4], der in Wasser und Ethanol unter Solvolyse löslich ist. Er ist wenig löslich in Kohlenstoffdisulfid und Chloroform. Mit Alkalilaugen hydrolysiert er. Die stark lichtbrechenden Kristalle zerfließen an Luft.[1] Als Feststoff (im Gegensatz zum monomeren Gas) liegt die Verbindung als Tetramer vor und besitzt eine Ringstruktur, bei der vier Niobatome ein nahezu gleichseitiges Parallelogramm bilden.[6] Er hat eine monokline Kristallstruktur mit der Raumgruppe C2/m (Raumgruppen-Nr. 12).[7]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Niob(V)-fluorid kann als Ausgangssubstanz für die Synthese von Niob(IV)-fluorid verwendet werden[4].
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 261.
- ↑ a b c Datenblatt Niobium(V) fluoride, 98% bei Sigma-Aldrich, abgerufen am 20. Juni 2013 (PDF).
- ↑ Otto Ruff: Über einige neue Fluoride. In: Chem. Ber., 1909, 42 (1), S. 492–497 (doi:10.1002/cber.19090420175).
- ↑ a b c Frank P. Gortsema: Niobium(IV) fluoride and niobium(V) fluoride - A. Niobium(V) fluoride. In: Aaron Wold and John K. Ruff (Hrsg.): Inorganic Syntheses. Band 14. McGraw-Hill Book Company, Inc., 1973, ISBN 07-071320-0 (defekt), S. 105–109 (englisch).
- ↑ Anatoly Agulyansky: Chemistry of Tantalum and Niobium Fluoride Compounds. Elsevier, 2004, ISBN 0-08-052902-X, S. 24 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Hans Peter Latscha, Martin Mutz: Chemie der Elemente. Springer DE, 2011, ISBN 3-642-16915-5, S. 224 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Jean d’Ans, Ellen Lax, Roger Blachnik: Taschenbuch für Chemiker und Physiker. Springer DE, 1998, ISBN 3-642-58842-5, S. 632 (eingeschränkte Vorschau in der Google-Buchsuche).




