Valinomycin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
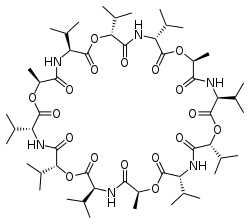
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Valinomycin | ||||||||||||||||||
| Andere Namen |
Cyclo(D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl-D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl-D-α-hydroxyisovaleryl-D-valyl-L-lactoyl-L-valyl) | ||||||||||||||||||
| Summenformel | C54H90N6O18 | ||||||||||||||||||
| Kurzbeschreibung |
beigefarbener Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 1111,32 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Valinomycin ist ein Cyclodeca-Depsipeptid und zählt zu den Makrolid-Antibiotika. Es wird von mehreren Arten von Streptomyceten (z. B. Streptomyces fulvissimus) produziert.
Struktur[Bearbeiten | Quelltext bearbeiten]
Valinomycin besteht aus den enantiomeren Aminosäuren L-Valin und D-Valin sowie den Hydroxysäuren L-Lactat und D-Hydroxyisovalerat. Die cyclische Struktur, bestehend aus der dreifach repetitiven Tetra-Depsipeptid-Einheit [–L-Lac–L-Val–D-Hiv–D-Val–]3, bildet einen symmetrischen Ring mit 36 Atomen aus wechselnden Amid- und Ester-Bindungen.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Valinomycin ist ein Ionophor, das selektiv Kalium-Ionen transportiert.[5][6] Dabei wird K+ in einer käfigartigen Struktur komplexiert und so durch die Zellmembran transportiert. Durch diese Transportvorgänge bricht das Membranpotential zusammen und die Zelle stirbt ab.[7]
Die Komplexbildungskonstante für den Kalium-Valinomycin-Komplex beträgt 106, während sie für den Natrium-Valinomycin-Komplex lediglich bei 10 liegt. Dieser große Unterschied (Selektivität) ist für die Transportvorgänge in biologischen Systemen von großer Wichtigkeit.
Verwendung[Bearbeiten | Quelltext bearbeiten]
Die meisten Elektroden zum Nachweis von Kaliumionen nutzen die spezifische Komplexierung von Kaliumionen durch Valinomycin, welches in einer Konzentration von etwa 0,7 % in eine Kunststoffmembran eingebettet ist.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- The Virtual Museum of Minerals and Molecules: Valinomycin
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Datenblatt Valinomycin bei Sigma-Aldrich, abgerufen am 25. April 2011 (PDF).
- ↑ a b Eintrag zu Valinomycin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ Eintrag zu Valinomycin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Dezember 2014.
- ↑ a b Eintrag zu Valinomycin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Rose Lars und Jenkins ATA: The effect of the ionophore valinomycin on biomimetic solid supported lipid DPPTE/EPC membranes. In: Bioelectrochem. 70. Jahrgang, Nr. 2, 2007, S. 387–393, PMID 16875886.
- ↑ Cammann K: Ion-selective bulk membranes as models for biomembranes. In: Top. Curr. Chem. 128. Jahrgang, 1985, S. 219–258, doi:10.1007/3-540-15136-2_8.
- ↑ Safiulina D, Veksler V, Zharkovsky A und Kaasik A: Loss of mitochondrial membrane potential is associated with increase in mitochondrial volume: physiological role in neurones. In: J Cell Physiol. 206. Jahrgang, Nr. 2, 2006, S. 347–353, PMID 16110491.
