Clobutinol
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
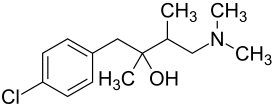
| ||||||||||||||||||||||
| Vereinfachte Strukturformel – Gemisch von vier Stereoisomeren | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Clobutinol | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C14H22ClNO | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 255,78 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Clobutinol (ursprünglicher Handelsname: Silomat, Boehringer Ingelheim) ist ein Arzneistoff, der als Hustenstiller (Antitussivum) eingesetzt wurde. Clobutinol hemmt das Hustenzentrum im Gehirn und lindert starken Reizhusten („trockenen“ Husten).
Mitte 2008 endete die Verkehrsfähigkeit für alle Clobutinol-haltigen Fertigarzneimittel, nachdem Nebenwirkungen am Herzen mit einem Risiko für lebensbedrohliche Folgen bekannt geworden waren (siehe „Von der Markteinführung bis zum Rückruf“).
Klinische Angaben[Bearbeiten | Quelltext bearbeiten]
Anwendungsgebiete[Bearbeiten | Quelltext bearbeiten]
Clobutinol wurde bei trockenem Reizhusten eingesetzt.
Unerwünschte Wirkungen[Bearbeiten | Quelltext bearbeiten]
Clobutinol galt bis zu seinem Rückruf als sehr gut verträgliches und sicheres Arzneimittel.
In einer bislang nicht vollständig publizierten Studie bei gesunden Probanden führte Clobutinol dosisabhängig zu einer erheblichen Verlängerung des QT-Intervalls im EKG, die die gegenwärtig akzeptierten Grenzwerte überschreitet.[2] Durch eine QT-Verlängerung können potenziell lebensbedrohliche Herzrhythmusstörungen (»Torsade-Arrhythmien«) verursacht werden. In der Literatur findet sich bislang ein Fall einer Torsade-Arrhythmie.[3] Auch ein Fall eines Grand-mal-Anfalls nach Überdosierung könnte theoretisch mit den Wirkungen auf das EKG in Verbindung gebracht werden.[3][4]
Weiterhin wurden auch Einzelfälle von allergischen Reaktionen bekannt.[5]
Wirkungsmechanismus[Bearbeiten | Quelltext bearbeiten]
Clobutinol hemmt das Hustenzentrum im verlängerten Mark (Medulla oblongata) und verringert so die Häufigkeit und Intensität von Hustenstößen. Bei produktivem bzw. verschleimtem Husten könnte das erwünschte Abhusten des Schleims unterdrückt werden. Daher wurde Clobutinol nur zur Anwendung bei trockenem Reizhusten empfohlen.
Von der Markteinführung bis zum Rückruf[Bearbeiten | Quelltext bearbeiten]
Clobutinol wurde in den 1950er Jahren bei der Dr. Karl Thomae GmbH (heute Teil von Boehringer Ingelheim) entwickelt und 1960/61 zum Patent angemeldet.[6] 1961 wurde es in Deutschland unter dem Namen Silomat als Fertigarzneimittel eingeführt.[7]
Nach Bekanntwerden des Auftretens einer Torsade-Arrhythmie bei einem kleinen Jungen im Jahr 2004[3] wurde zunächst die Gebrauchsinformation mit entsprechenden Hinweisen versehen, ferner forderte das deutsche Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) den Hersteller auf, Clobutinol auf mögliche Wirkungen auf die elektrische Reizleitung des Herzes zu untersuchen. Nach Angaben des Herstellers hatten bis dahin mehr als 200 Mio. Patienten den oft rezeptfrei verfügbaren Wirkstoff über 40 Jahre hinweg eingenommen.[7] Auch unter Experten galt der Wirkstoff als sicher.[8]
Nach Vorlage der Probandenstudie[2] ordnete das BfArM am 31. August 2007 das Ruhen der Zulassung für alle Clobutinol-haltigen Arzneimittel an. Die Entscheidung des BfArMs beruhte auf einer Nutzen-Risiko-Abwägung: Obwohl das Risiko potentiell lebensbedrohlicher Nebenwirkungen als gering einzuschätzen sei, stünden andere Arzneimittel für die Behandlung der eher leichten Erkrankung Reizhusten zur Verfügung.[9] Am gleichen Tag zog Boehringer Ingelheim alle eigenen Clobutinol-haltigen Arzneimittel weltweit aus dem Handel zurück.[7]
Im Oktober 2007 folgte die Empfehlung des Ausschusses für Humanarzneimittel der Europäischen Arzneimittelagentur, die Zulassung für alle Clobutinol-haltigen Arzneimittel in der EU zu widerrufen. Eine entsprechende Entscheidung der Europäischen Kommission wurde im Juni 2008 vom BfArM umgesetzt.[10]
Nach dem Rückruf von Clobutinol wurde spekuliert, dass es – statistisch gesehen – feststehe, dass zahlreiche Patienten an Clobutinol gestorben seien. Niemand habe das als sicher geltende Hustenmittel verdächtigt, Zwischenfälle auszulösen.[8] Das Risiko für ein Auftreten von QT-Verlängerungen mit lebensbedrohlichen Folgen wurde zunächst als gering eingeschätzt.[3] Der Junge, bei dem die Torsade-Arrhythmie als Folge der Clobutinoleinnahme aufgetreten war, überlebte trotz einer vorbestehenden Herzschädigung.[3]
Boehringer Ingelheim vertreibt seit November 2008 wieder Hustenmittel unter dem Warenzeichen Silomat. Clobutinol wurde durch den Wirkstoff Pentoxyverin ersetzt. Weiterhin ist auch ein Arzneimittel Silomat DMP im Handel. Als Wirkstoff enthält es Dextromethorphan.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Entscheidung der Kommission vom 10-I-2008 betreffend die Zulassung(en) eines Humanarzneimittels (von Humanarzneimitteln) mit dem Wirkstoff „Clobutinol“ gemäß Artikel 107 der Richtlinie 2001/83/EG des Europäischen Parlaments und des Rates. Anhang 2. (PDF; 16 kB) Europäische Kommission, 10. Januar 2008; abgerufen am 28. September 2008.
- ↑ a b c d e C. Bellocq, R. Wilders, J. J. Schott u. a.: A common antitussive drug, clobutinol, precipitates the long QT syndrome 2. In: Mol Pharmacol. 66, 2004, S. 1093–1102. PMID 15280442
- ↑ M. S. Ramirez, A. M. Rojas, L. A. Perez, I. A. Arias, M. Calles, A. Aranguren: Grand mal seizure and clobutinol overdose. In: Vet Hum Toxicol., 35, 1993, S. 444. PMID 8249270
- ↑ C. S. Seitz, E. B. Bröcker, A. Trautmann: Allergy evaluation after emergency treatment: anaphylaxis to the over-the-counter medication clobutinol. In: Emerg Med J. 24, 2007, S. e19. PMID 17351213
- ↑ Patent US3121087A: Amino-substituted butanols as cough-depressants. Angemeldet am 28. Juni 1961, veröffentlicht am 11. Februar 1964, Anmelder: Dr. Karl Thomae GmbH, Erfinder: Alex Berg.
- ↑ a b c Geschichte. 1948–1988. ( vom 26. Oktober 2016 im Internet Archive)Boehringer Ingelheim GmbH; abgerufen am 28. September 2008.
- ↑ a b A. S. Kekulé: Tödlicher Hustensaft. In: Tagesspiegel. 5. September 2007; abgerufen am 9. März 2015.
- ↑ Clobutinol-haltige Arzneimittel:BfArM ordnet Ruhen der Zulassung an. 31. August 2007, abgerufen am 24. Februar 2016.
- ↑ Clobutinol-haltige Arzneimittel: BfArM ordnet Widerruf der Zulassung an. 13. Juni 2008.