Cobalt(II)-nitrat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
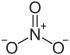
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cobalt(II)-nitrat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | Co(NO3)2 | ||||||||||||||||||
| Kurzbeschreibung |
rotbraune, hygroskopische Kristalle (Hexahydrat)[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 182,94 g·mol−1 (wasserfrei)
291,04 g·mol−1 (Hexahydrat) | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
100–105 °C (Zersetzung)[1] | ||||||||||||||||||
| Löslichkeit |
sehr gut in Wasser (1030 g·l−1 bei 25 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend, fortpflanzungsgefährdend (CMR)[4] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Cobaltnitrat ist ein Salz der Salpetersäure, gebildet aus dem Cobaltkation und dem Nitratanion. Das braunrote und hygroskopische Salz liegt in der Regel als Hexahydrat vor und bildet monokline Kristalle, die in Wasser, Ethanol und anderen organischen Lösemitteln gut löslich sind. Oberhalb von 55 °C geht das Hexahydrat unter Wasserabgabe schnell in das Trihydrat über. Bekannt ist auch ein Monohydrat, das kristallwasserfreie Salz ist blassrot und von pulvriger Konsistenz.
Verwendung[Bearbeiten | Quelltext bearbeiten]


Es wird in der klassischen anorganischen analytischen Chemie zum qualitativen Nachweis von Zink als Rinmans Grün (ZnCo2O4) und Aluminium als Thénards Blau (CoAl2O4) auf der Magnesiarinne verwendet. Es kann auch als Reagenz in der Zwikker-Reaktion zum Nachweis NH-azider Verbindungen zum Einsatz kommen.
Es dient außerdem zur Herstellung von hochreinem Cobalt und wird als Buntpigment für Keramiken verwendet.
Des Weiteren werden Lösungen davon dazu verwendet, Porzellantiegel dauerhaft zu beschriften.
Darstellung[Bearbeiten | Quelltext bearbeiten]
Cobalt(II)-nitrat wird durch Auflösen von Cobalt, Cobalt(II)-oxid oder Cobalt(II)-carbonat in verdünnter Salpetersäure hergestellt.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Cobalt(II)-nitrat kristallisiert in Abhängigkeit vom Kristallwassergehalt in verschiedenen Kristallstrukturen, deren Eigenschaften in untenstehender Tabelle angeführt sind. Das Hexahydrat geht bei 106 °C in das Dihydrat über.[6]
| Gitterparameter der verschiedenen Modifikationen von Cobalt(II)-nitrat | |||||||
| Formel | Kristallsystem | Raumgruppe | a [ Å ] | b [ Å ] | c [ Å ] | β | Z |
|---|---|---|---|---|---|---|---|
| Co(NO3)2 · 6 H2O[7] | monoklin | C2/c (Nr. 15) | 14,29 | 6,14 | 12,66 | 112,79° | 4 |
| Co(NO3)2 · 2 H2O[6] | monoklin | P21/n (Nr. 14, Stellung 2) | 6,019 | 8,629 | 5,729 | 92,65° | 2 |
| Co(NO3)2[8] | trigonal | R3 (Nr. 148) | 10,50 | – | 12,84 | 12 | |
Toxikologie[Bearbeiten | Quelltext bearbeiten]
Cobalt(II)-nitrat ist krebserzeugend und erbgutverändernd und steht außerdem unter dem Verdacht, fruchtschädigend zu sein.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Eintrag zu Cobalt(II)-nitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Inorganic Compounds, S. 4-60.
- ↑ Eintrag zu Cobalt dinitrate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 17. Juli 2014.
- ↑ G.J.A. Speijers, E.I. Krajnc, J.M. Berkvens, M.J. van Logten: Acute oral toxicity of inorganic cobalt compounds in rats. In: Food and Chemical Toxicology. Band 20, Nr. 3, Juni 1982, S. 311–314, doi:10.1016/S0278-6915(82)80298-6.
- ↑ a b B. Ribár, N. Milinski, R. Herak, I. Krstanovič, S. Djurič: The crystal structure of cobalt nitrate dihydrate, Co(NO3)2 · 2 H2O. In: Zeitschrift für Kristallographie 1976, 144 (1-6), S. 133–138. doi:10.1524/zkri.1976.144.1-6.133.
- ↑ Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-540-60035-0, S. 386 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ G.A. Tikhomirov, K.O. Znamenkov, I.V. Morozov, E. Kemnitz, S.I. Troyanov: Anhydrous nitrates and nitrosonium nitratometallates of manganese and cobalt, M(NO3)2, NO(Mn(NO3)3), and (NO)2(Co(NO3)4): synthesis and crystal structure. In: Zeitschrift für anorganische und allgemeine Chemie, 628, 2002, S. 269–273, doi:10.1002/1521-3749(200201)628:1<269::AID-ZAAC269>3.0.CO;2-P.
- Brandfördernder Stoff
- Gesundheitsschädlicher Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Einatmen
- Sensibilisierender Stoff
- Ätzender Stoff
- Krebserzeugender Stoff
- Erbgutverändernder Stoff
- Stoff mit reproduktionstoxischer Wirkung
- Umweltgefährlicher Stoff (chronisch wassergefährdend)
- CMR-Stoff
- SVHC-Stoff
- Cobaltverbindung
- Nitrat
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 30
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 28

![{\displaystyle \mathrm {\ \!\ {\Biggr ]}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c9fd9553a0b623f5f669641be907d9186e35b739)
![{\displaystyle \mathrm {\ \!\ {\Biggr ]}_{2}^{-}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9256af4564b238218bfa888448b20ebf4d44e6dc)





