Derivat (Chemie)
Als Derivat (von lateinisch derivare ‚ableiten‘) oder Abkömmling einer Stammverbindung (Grundsubstanz, Muttersubstanz) kann in der organischen Chemie eine Substanz dann bezeichnet werden, wenn sie eine Struktureinheit besitzt, die der funktionellen Gruppe der Stammverbindung ähnlich ist und ein Strukturelement dieser funktionellen Gruppe im gleichen Oxidationszustand enthält. Häufig können Derivate aus der jeweiligen Stammverbindung in einem einzigen Reaktionsschritt hergestellt werden.[1][2] Diesem einen Reaktionsschritt kann eine Aktivierung der funktionellen Gruppe der Stammverbindung vorgeschaltet sein. Man spricht dann von reaktiven Derivaten der betreffenden Stammverbindung, die man bei Bedarf auch isolieren kann und aus denen sich weitere Derivate dann leicht herstellen lassen. Als reaktive Derivate von Carbonsäuren gut bekannt sind die Carbonsäurehalogenide. Chemische Reaktionen zur Herstellung von Derivaten bezeichnet man als Derivatisierung.
Bei komplexen Verbindungen mit mehreren gleichen oder unterschiedlichen funktionellen Gruppen ist eine gezielte Derivatisierungsreaktion an einer bestimmten funktionellen Gruppe häufig nicht möglich, ohne vorher die anderen funktionellen Gruppen mit Schutzgruppen zu blockieren.
Entsprechend der Definition sind die Stammverbindung und ihre Derivate strukturell eng verwandt. An Stelle der funktionellen Gruppe der Stammverbindung findet sich im Derivat zwar eine neue funktionelle Gruppe, die aber ein strukturelles Teilelement der funktionellen Gruppe der Stammverbindung im gleichen Oxidationszustand besitzt. Wegen der neuen funktionellen Gruppe haben Derivate meist deutlich andere chemische und physikalische Eigenschaften als die Stammverbindungen, können aber mit geeigneten Reaktionen in die Stammverbindung rücküberführt werden.
Abgrenzung des Begriffs Derivat
[Bearbeiten | Quelltext bearbeiten]Entgegen der in der Einleitung formulierten strengen Definition des Begriffs Derivat wird er im allgemeinen Sprachgebrauch häufig ganz allgemein im Sinne von struktureller Abkömmling einer Grundsubstanz benutzt. Als Derivate der Grundsubstanz werden dann Substanzen bezeichnet, die eine ähnliche Struktur aufweisen oder die Struktur der Grundsubstanz als Teilstruktur besitzen. Der Begriff Derivat wird in diesen Fällen in der Absicht gebraucht, auf diese Ähnlichkeiten oder auf die teilweise strukturelle Identität des Abkömmlings mit der Struktur einer eventuell gut bekannten Stammverbindung hinzuweisen.
Beispiele für Derivate
[Bearbeiten | Quelltext bearbeiten]Carbonsäurederivate
[Bearbeiten | Quelltext bearbeiten]Die Gruppe der Carbonsäurederivate bietet die beste Möglichkeit zu erkennen, welche Verbindungen die in der Einleitung formulierten strengen Bedingungen für ein Derivat erfüllen. Carbonsäurederivate sind Carbonsäurehalogenide, Carbonsäureanhydride, Carbonsäureester, Carbonsäureamide, Carbonsäurehydrazide und Carbonsäureazide. Die Carbonsäurederivate unterscheiden sich von der zugrunde liegenden Stammverbindung Carbonsäure formal dadurch, dass nur die OH-Gruppe der Carboxygruppe durch eine andere, mit einem Heteroatom (meist: Hal, O, S, N) beginnende Gruppe ersetzt (substituiert) wurde. Die Carbonylgruppe der Carboxygruppe bleibt als wesentliches Strukturelement der funktionellen Carboxygruppe im gleichen Oxidationszustand erhalten und kann auch das Reaktionsverhalten der Carbonsäurederivate mitbestimmen. In allen Fällen können die Derivatisierungsreaktionen zur Herstellung der Derivate durch Hydrolysereaktionen wieder rückgängig gemacht werden.[3] Die relative Reaktivität der Carbonsäurederivate nimmt dabei in der unten dargestellten Reihenfolge ab. Dies lässt sich damit begründen, dass die Elektronegativität der blau gekennzeichneten Substituenten in dieser Reihenfolge auch abnimmt, was mit einem abnehmenden Austrittsvermögen verbunden ist.[4]
Weitere Beispiele für Derivate
[Bearbeiten | Quelltext bearbeiten]Typische Beispiele für Derivate gemäß der Definition in der Einleitung:
- Chloroform ist formal gesehen gemäß der Oxidationsstufe des einen C-Atoms ein Derivat der Ameisensäure, bzw. des instabilen Formylchlorids.
- Ethanol bzw. Ethanal sind formal gesehen und nur gemäß ihrer Oxidationsstufen Derivate von Monochlorethan bzw. von 1,1-Dichlorethan.
- Diethylether ist ein Derivat von Ethanol, in dem die OH-Gruppe ersetzt wurde durch eine O-Alkyl-Gruppe (OR-Gruppe) ohne Änderung des Oxidationszustandes. Bei der Bildung des Derivats (Derivatisierungsreaktion) mit H2SO4 wird zunächst ein Alkylsulfat als reaktive Zwischenstufe gebildet.
- Imine und Oxime sind Derivate von Aldehyden und Ketonen, gebildet durch deren Reaktionen mit Aminen oder Hydroxylamin.
- Hydrazone sind Derivate von Aldehyden und Ketonen, gebildet durch deren Reaktionen mit Hydrazin oder dessen Abkömmlingen.
- Disaccharide sind Derivate von zwei Monosacchariden. Polysaccharide, wie z. B. Stärke sind Derivate von Monosacchariden, z. B. Glucosederivate. Bei der Bildung von glycosidischen Bindungen wird eine OH-Gruppe durch eine O-Alkyl-Gruppe ersetzt, ohne Änderung des Oxidationszustandes. Auch die OH-Gruppen in Polysacchariden wie Stärke können mit reaktiven Carbonsäurederivaten,z. B. mit Acetylchlorid, derivatisiert werden. Die entstehenden Produkte nennt man derivatisierte oder Modifizierte Stärke.
- Fette sind als Carbonsäureester Derivate von Glycerin und werden dementsprechend als Triglyceride bezeichnet. Daneben sind Fette auch Derivate der Carbonsäuren, die für das jeweilige Fett typisch sind.
- Fette, die das Strukturelement des phosphorylierten Glycerins enthalten, werden als Phosphoglycerinderivate (Phosphoglyceride) bezeichnet.
- Lipide, die das Strukturelement Sphingosin (ein einfach ungesättigter Aminoalkohol) enthalten, werden als Sphingosinderivate oder als Sphingomyeline bezeichnet.
Beispiele für strukturelle Abkömmlinge
[Bearbeiten | Quelltext bearbeiten]Typische Beispiele für strukturelle Abkömmlinge, bei denen es sich nicht um Derivate im Sinne der obigen Definition handelt, die jedoch im allgemeinen Sprachgebrauch mitunter auch als Derivate bezeichnet werden.
Strukturelle Abkömmlinge von Methan und Ethan
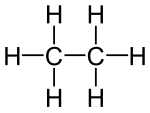
[Bearbeiten | Quelltext bearbeiten]- Chloroform ist ein struktureller Abkömmling von Methan, weil beide Verbindungen ein einziges C-Atom enthalten und weil drei H-Atome durch Cl-Atome ersetzt wurden. Das C-Atom in beiden Verbindungen befindet sich jedoch in einem unterschiedlichen Oxidationszustand.
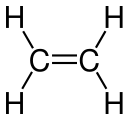
- Ethanol, Ethanal, Ethen, Ethin, Essigsäure, Chlorethan sind strukturelle Abkömmlinge von Ethan, da alle Verbindungen zwei verknüpfte C-Atome enthalten. Tatsächlich sind die C-Atome in den strukturellen Abkömmlingen in höheren, unterschiedlichen Oxidationszuständen als im Ethan selbst. Alle Verbindungen lassen sich nicht durch Derivatisierungsreaktionen aus Ethan herstellen, sondern nur durch mehr oder weniger aufwändige Synthesen, die immer auch mit einer Oxidation des Ethans verbunden sind.
Die gezeigten Verbindungen sind gemäß der strengen Definition in der Einleitung keine Derivate des Ethans, obwohl sie alle zwei C-Atome haben. Die Verbindungen sind eigenständige Verbindungen mit neuen funktionellen Gruppen, mit den C-Atomen meist in höheren Oxidationszuständen im Vergleich zum Ethan. Die Herstellungen dieser Verbindungen aus Ethan sind keine Derivatisierungsreaktion, sondern Synthesen.
Strukturelle Abkömmlinge von Phenol
[Bearbeiten | Quelltext bearbeiten]Im allgemeinen Sprachgebrauch werden mitunter das in Chili enthaltene Capsaicin und das gut riechende Himbeerketon als Derivate des Phenols bezeichnet, da diese Verbindungen die Phenol-Teilstruktur enthalten. Da jedoch beide Verbindungen zusätzliche funktionelle Gruppen enthalten und die ursprüngliche OH-Gruppe von Phenol unverändert vorliegt, handelt es sich nicht um Derivate gemäß obiger Definition, sondern nur um strukturell verwandte Verbindungen.
Weitere Beispiele für eine irreführende Verwendung des Begriffs Derivat
[Bearbeiten | Quelltext bearbeiten]- Mitunter wird Phenylhydrazin als eine chemische Verbindung aus der Gruppe der Hydrazin-Derivate bezeichnet. Tatsächlich ist Phenylhydrazin eine eigenständige Verbindung, so wie auch Anilin als eigenständiges Amin keine Verbindung aus der „Gruppe der Ammoniak-Derivate“ ist.
- Es wird mitunter behauptet, α-Aminocarbonsäuren und α-Chlorcarbonsäuren seien Derivate von Carbonsäuren, weil beide Verbindungsklassen als wichtiges Strukturelement die für Carbonsäuren typische funktionelle Carboxygruppe enthalten. Tatsächlich aber handelt es sich um unterschiedliche Verbindungsklassen mit jeweils zwei funktionellen Gruppen, von denen eine identisch ist. Daher sind Aminocarbonsäuren und Chlorcarbonsäuren besser als strukturelle Abkömmlinge von Carbonsäuren zu bezeichnen. Hingegen kann man Aminocarbonsäuren als Derivate von Chlorcarbonsäuren bezeichnen, denn es ist zumindest in einer formalen Derivatisierungsreaktion möglich, die funktionelle Gruppe C-Cl in der Chlorcarbonsäure durch Reaktion mit Ammoniak NH3 zu ersetzen durch die neue funktionelle Gruppe C-NH2 im gleichen Oxidationszustand.
Die Bedeutung der Derivatisierung
[Bearbeiten | Quelltext bearbeiten]Derivate können zu bestimmten Zwecken ganz gezielt aus den Stammverbindungen (Grundsubstanz) mit Hilfe von Derivatisierungsreaktionen hergestellt werden. Dann sollen Derivate bestimmte zusätzliche Anforderungen erfüllen, die von der Grundsubstanz nicht erfüllt werden. Man kann folgende Einsatzgebiete abgrenzen:
- Pharmazie: Derivate sollen im Falle von Wirkstoffen eine bessere Verträglichkeit oder Wirksamkeit als die Grundsubstanz haben.
- Trennung: Derivate sollen eine bessere oder schlechtere Löslichkeit haben, um sie durch Filtration oder Zentrifugation von anderen Substanzen abtrennen zu können.
- Analytik, Trennung, Identifizierung: Derivate sollen höhere Flüchtigkeiten haben als die Grundsubstanzen, damit man sie z. B. mittels Gaschromatographie analytisch trennen und identifizieren kann. Derivate sollen farbig sein, damit man sie bei der Dünnschichtchromatographie erkennen kann. Derivate sollen fest sein und definierte Schmelzpunkte besitzen, damit man die zugehörigen Stammverbindungen eindeutig identifizieren kann.
- Synthese: Derivate sollen, eine höhere Reaktivität als die Stammverbindungen haben, damit mit diesen sog. reaktiven Derivaten einfacher als aus den Stammverbindungen besser neue Bindungen geknüpft und neue Substanzen synthetisiert werden können.
Pharmazie
[Bearbeiten | Quelltext bearbeiten]In der Pharmazie kann die Derivatisierung von besonderer Bedeutung sein, um vorhandene Arzneimittel wirksamer oder verträglicher zu machen. So kann man z. B. die Acetylsalicylsäure sowohl als ein Derivat der Essigsäure (ein Ester) bezeichnen, als auch als Derivat der phenolischen OH-Gruppe der Salicylsäure. Durch die Acetylierung, d. h. durch die Überführung in ein Derivat der Essigsäure, konnte die unzureichende schmerzstillende Wirkung der Salicylsäure verbessert werden.
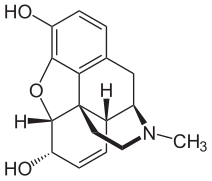
Ein weiteres Beispiel für die Veränderung der Wirksamkeit eines Arzneistoffes durch Derivatisierung ist die Umwandlung von Morphin in Heroin, das als 3,6-Diacetylmorphin ein Essigsäurederivat des Morphins ist und durch (Acetylierung) aus Morphin gewonnen wird.
Chromatographie
[Bearbeiten | Quelltext bearbeiten]In der gesamten chromatographischen Analytik spielt die Derivatisierung eine bedeutende Rolle.
In der Gaschromatographie und Gaschromatographie mit Massenspektrometrie-Kopplung werden Derivate meist eingesetzt, um nicht oder nur schwer verdampfbare Analyte in leichter flüchtige Derivate umzuwandeln, die der Chromatographie in der Gasphase zugänglich sind.
In der HPLC-Analytik werden häufig chromophore und/oder fluoreszierende Derivate eingesetzt, um die sensitive und spezifische Detektion im sichtbaren bzw. ultravioletten Spektralbereich zu ermöglichen.[2] In der Dünnschichtchromatographie können Substanzen mit Nachweisreagenzien unter Bildung gefärbter Derivate sichtbar gemacht werden. Man bezeichnet dies als postchronmatographische Derivatisierung.[5] Dabei werden die Derivatisierungsreagenzien auf die DC-Platten aufgesprüht oder die DC-Platten mit dem Derivatisierungsreagenz bedampft oder in damit getaucht.
Gängige Derivatisierungreagenzien in der Chromatographie sind
- Ninhydrin zum Nachweis von Aminosäuren
Charakterisierung von Verbindungen
[Bearbeiten | Quelltext bearbeiten]Historische Bedeutung hat die Derivatisierung in der Analytik und Charakterisierung organischer Verbindungen:[6]
- Durch Umsetzung von Carbonylverbindungen mit 2,4-Dinitrophenylhydrazin erhält man die besonders gut kristallisierenden Hydrazone.
- Die Methode der Identifizierung von Monosacchariden durch Derivatisierung mit Phenylhydrazin zu den Osazonen wurde von Emil Fischer 1884 entwickelt.
Homologe Reihen
[Bearbeiten | Quelltext bearbeiten]Vom Begriff Derivat abgegrenzt werden muss der Begriff Homologon. Homologa sind Stoffe, die sich nur durch die Kettenlänge ihrer Grundbausteine unterscheiden; in der Organischen Chemie sind dies die Kohlenwasserstoffketten etwa von Alkanen, Alkenen, Alkoholen oder Carbonsäuren. Glieder dieser homologen Reihen sind in ihren chemischen und physikalischen Eigenschaften oft sehr ähnlich.[7] Homologa sind in aller Regel keine Derivate.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Karl Blau, Graham S. King (Hrsg.): Handbook of Derivatives for Chromatography. Heyden & Son Ltd., London 1977, ISBN 0-85501-206-4.
- R. W. Frei, J. F. Lawrence (Hrsg.): Chemical Derivatization in Analytical Chemistry. Band 1: Chromatography. Plenum Press, New York & London 1981, ISBN 0-306-40608-X.
- Eintrag zu Derivate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- Daniel R. Knapp: Handbook of Analytical Derivatization Reactions. J. Wiley & Sons, New York 1997, ISBN 0-471-03469-X.
- Kurt Peter C. Vollhardt: Organische Chemie. (= Organic chemistry, structure and function). 3. Auflage. Wiley-VCH, Weinheim 2000, ISBN 3-527-29819-3 (Kap. 15, 19 und 20).
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Brockhaus ABC Chemie. VEB F. A. Brockhaus Verlag Leipzig 1965, S. 276.
- ↑ a b Eintrag zu Derivatisierung. In: Römpp Online. Georg Thieme Verlag, abgerufen am 8. November 2018.
- ↑ Oliver Reiser: Organische Chemie : Studieren kompakt. Hrsg.: Paula Y. Bruice. 5. Auflage. Pearson Studium, München 2011, ISBN 978-3-86894-102-9, S. 658.
- ↑ K. Peter C. Vollhardt, Neil E. Schore: Organische Chemie. Hrsg.: Holger Butenschön. 5. Auflage. Wiley-VCH, Weinheim 2011, ISBN 978-3-527-32754-6, S. 991–993.
- ↑ DocCheck Flexikon: Derivatisierung, abgerufen am 20. November 2018.
- ↑ Hans Beyer, Wolfgang Walter: Lehrbuch der organischen Chemie. 18. Auflage. S. Hirzel Verlag, Stuttgart 1978, ISBN 3-7776-0342-2.
- ↑ Brockhaus ABC Chemie. VEB F. A. Brockhaus Verlag Leipzig 1965, S. 551.