Luminol
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
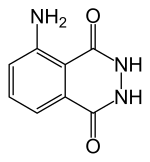
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Luminol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H7N3O2 | ||||||||||||||||||
| Kurzbeschreibung |
blassgelbes kristallines Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 177,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Luminol ist eine gelblich bis grün schimmernde, in Wasser unlösliche feste chemische Verbindung, die sich formal von Anilin, Phthalsäure und Hydrazin ableitet.
Gewinnung und Herstellung
[Bearbeiten | Quelltext bearbeiten]Die Herstellung von Luminol erfolgt über die Nitrierung von Phthalsäure zu 3-Nitrophthalsäure, deren Umsetzung mit Hydrazin zu 3-Nitrophthalsäurehydrazid und nachfolgender Reduktion mit Natriumdithionit zum Luminol.

Alternativ ist die Synthese von 3-Nitrophthalhydrazid aus 3-Nitrophthalsäureanhydrid möglich, welche bessere Ausbeuten liefert.[6]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Kriminalistik
[Bearbeiten | Quelltext bearbeiten]
Luminol wird in der Kriminalistik zur Spurensuche verwendet, selbst geringste Mengen von Blut lassen sich hiermit nachweisen. Der Nachweis beruht darauf, dass Luminol mit Oxidationsmitteln (meist Wasserstoffperoxid) unter Emission von bläulichem Licht (Chemolumineszenz) reagiert. Diese Reaktion verläuft nur bei Anwesenheit eines Katalysators (hier komplex gebundenes Fe2+ oder Fe3+) ausreichend schnell, d. h. in der Praxis ist bei der Abwesenheit von Katalysatoren keine Reaktion bzw. keine Chemolumineszenz zu beobachten.
Zur Spurensuche werden zwei Lösungen hergestellt: Eine Lösung von Luminol in Natronlauge und eine verdünnte Wasserstoffperoxid-Lösung. Diese werden kurz vor der Anwendung zusammengegeben und die zu untersuchenden Flächen eingesprüht. Befinden sich darauf Blutspuren, so katalysiert das Häm (ein Eisenkomplex) des Blutfarbstoffs Hämoglobin die unten beschriebene Reaktion. Es kommt also zu einer bläulichen Chemolumineszenz. Der Test ist empfindlich genug, um winzige Blutmengen im Urin nachzuweisen, wodurch Urinflecken ebenfalls „positiv“ erscheinen. Allerdings wird die Reaktion auch durch Kupferionen katalysiert, welche diesen Test somit stören.
Durch Zugabe von weiteren Substanzen kann die Empfindlichkeit variiert werden: In einer Testreihe konnte nachgewiesen werden, dass Wirkstoffe in dem Geschirrspülmittel Fit die Lumineszenz intensivieren, zugleich aber auch verkürzen.[7] Ursache hierfür könnten Detergentien im Reinigungsmittel sein, die die Plasmamembranen der Erythrozyten durchlässiger machen, wodurch das Luminol schneller mit dem Fe2+ in Kontakt kommt.[8]
Luminol ermöglicht weiterhin Tests zur Speziesidentifizierung und Blutgruppenbestimmung. Zudem hat Luminol keine zerstörerischen Effekte auf DNA, sodass diese mittels PCR analysierbar bleibt.[9]
Eine Weiterentwicklung auf der Basis von Luminol stellt das BlueStar® Forensic dar, das die DNA der zu untersuchenden Probe in keiner Weise verändert, eine stärker ausgeprägte Chemolumineszenz besitzt und selbst Blutspuren erkennen lässt, die schon zuvor weggewischt oder mit Wasser ausgewaschen worden sind und für das bloße Auge nicht mehr erkennbar waren.[10]
Biochemische und medizinische Analytik
[Bearbeiten | Quelltext bearbeiten]Eine weitere Anwendung findet die Luminol-Chemolumineszenz in der biochemischen und medizinischen Analytik. Hier werden z. B. sogenannte Reaktive Sauerstoffspezies (ROS) in Geweben, Extrakten und Körperflüssigkeiten direkt durch die Intensität der Luminol-Chemolumineszenz bestimmt. Eine weitere wichtige Analysemethode beruht darauf, dass auch Peroxidasen in der Lage sind, die Luminol-Reaktion zu katalysieren. Auf diesem Prinzip werden zahlreiche Immunoassays aufgebaut, mit denen sich extrem geringe Mengen an Toxinen, Krankheitserregern, Peptiden und Proteinen nachweisen lassen.[11] Die wichtigste hierfür verwendete Peroxidase ist die Meerrettichperoxidase (HRP, horseradish peroxidase). Die katalytische Wirkung der Meerrettichperoxidase kann man selbst testen, indem man einige Tropfen einer alkalischen Luminol/Wasserstoffperoxid Lösung auf ein Stück frischen Meerrettich tropft.
Chemolumineszenzreaktion
[Bearbeiten | Quelltext bearbeiten]
Bei der Chemolumineszenz-Reaktion handelt es sich bei Luminol als Ausgangsstoff um eine Dicarbonylverbindung, ein so genanntes 1,4-Dion.
Der Stoff wird zunächst in Natronlauge gelöst, wobei Luminol als Säure unter H+-Abspaltung mit den Hydroxidionen der Natronlauge reagiert. Bei dieser Reaktion handelt es sich um eine reversible Gleichgewichtsreaktion.
Die entstandenen Dianionen werden durch Mesomerie stabilisiert.
Die eigentliche Reaktion beginnt mit der Oxidation der Dianionen durch Wasserstoffperoxid oder ein anderes Oxidationsmittel. Dabei entsteht neben molekularem Stickstoff ein Phthalat, das 3-Aminophthalat-Dianion, als instabiles Intermediat im angeregten Triplett-Zustand (T1). Der Triplett-Zustand liegt aufgrund von zwei Elektronen mit identischem Spin in einem Orbital eines Sauerstoffatoms vor (2S+1=3 bei S=1=2*1/2, siehe Multiplizität). Durch einen strahlungslosen Übergang geht das Molekül mit einem Spin-Flip in einen isoenergetisch angeregten Singulett-Zustand (S1) über.
Das energiereiche oxidierte Luminol-Molekül dient bei dieser Chemolumineszenz gleichzeitig als Sensibilisator. Durch den Übergang des Elektrons aus dem höher angeregten Singulettzustand in den Singulettgrundzustand (S0) wird ein Photon im blauen Bereich des Lichtspektrums emittiert.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Arnold Willmes: Taschenbuch chemische Substanzen Elemente - Anorganika - Organika - Naturstoffe - Polymere.3., vollständig überarbeitete und erweiterte Auflage, Deutsch, Frankfurt am Main 2007, ISBN 978-3-8171-1787-1.
- ↑ Eintrag zu 3-Aminophthalhydrazide bei Thermo Fisher Scientific, abgerufen am 13. Oktober 2023.
- ↑ a b c Mary Eagleson: Concise Encyclopedia Chemistry. de Gruyter, Berlin 1994, ISBN 978-3-11-011451-5, S. 607.
- ↑ a b Eintrag zu 5-Amino-1,2,3,4-tetrahydrophthalazin-1,4-dion in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ National Academy of Sciences, National Research Council, Chemical-Biological Coordination Center, Review., 5(11), 1953.
- ↑ H. D. K. Drew, F. H. Pearman: Chemiluminescent organic compounds. Part II. The effect of substituents on the closure of phthalhydrazides to 5- and 6-membered rings. In: Journal of the Chemical Society. 1937, S. 26–33, doi:10.1039/JR9370000026.
- ↑ Katrin Heuser, Martin Oehmen, Nadine Kühner, Mark Benecke: Wirkung des Spülmittels „Fit“ auf die Luminol-Fluoreszenz. In: Archiv für Kriminologie. Nr. 217, 2006, S. 137–145 (Online).
- ↑ Katrin Heuser, Martin Oehmen, Nadine Kühner, Mark Benecke: Wirkung des Spülmittels "Fit" auf die Luminol-Fluoreszenz. In: Archiv für Kriminologie. Nr. 217, 2006, S. 144 (Online).
- ↑ Neha Passi, Rakesh Kumar Garg, Mukesh Yadav, Ram Sarup Singh, Magdy A. Kharoshah: Effect of luminol and bleaching agent on the serological and DNA analysis from bloodstain. In: Egyptian Journal of Forensic Sciences. Band 2, Nr. 2, 2012, S. 54–61, doi:10.1016/j.ejfs.2012.04.003.
- ↑ M. Dawn Watkins, King C. Brown: Blood Detection − A comparison of visual enhancement chemicals study for the recovery of possible blood stains at the crime scene. Luminol vs. BLUESTAR®. (als PDF) − verkürzte Fassung in: Evidence Technology Magazine. März/ April 2006, Band 4, Nr. 2.
- ↑ Steffen Albrecht, Herbert Brandl, Thomas Zimmermann: Chemilumineszenz: Reaktionssysteme und ihre Anwendung unter besonderer Berücksichtigung von Biochemie und Medizin. Hüthig, Heidelberg 1996, ISBN 3-7785-2501-8.
