Pseudojonon
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
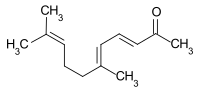
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Pseudojonon | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C13H20O | ||||||||||||
| Kurzbeschreibung |
gelbliches Öl[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 192,30 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Dichte |
0,8951 g·cm−3 (20 °C)[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
265,4 °C[2] | ||||||||||||
| Dampfdruck | |||||||||||||
| Löslichkeit |
| ||||||||||||
| Brechungsindex |
1,5335 (20 °C)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||
Pseudojonon ist eine zu den Terpenen zählende chemische Verbindung. Es liegt als gelbliches Öl vor.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Pseudojonon ist eine in der Natur vorkommende Verbindung. Sie wurde in Tabakpflanzen nachgewiesen. Beim Verdau von Lycopin (z. B. aus Tomaten) bildet der Mensch Pseudojonon. In Pflanzen ist es ein Zwischenprodukt in der Biosynthese von Lycopin. Pseudojonon könnte daher in vielen Blütenpflanzen und damit weit verbreitet in der Natur angetroffen werden.[2]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Da Pseudojonon in der Natur nur in geringen Mengen vorkommt, wird es fast ausschließlich synthetisch hergestellt.
Zur Darstellung wird beispielsweise Citral im basischen Milieu mit Aceton kondensiert.

Technisch wird Pseudojonon heute meist aus Acetessigester und Dehydrolinalool durch Erhitzen auf 160 °C hergestellt. Hierbei fällt ein Gemisch von zwei verschiedenen Diastereomeren.

Hierbei cyclisiert auch ein erheblicher Teil (bis zu 40 %) des Zwischenprodukts. Dies kann aber durch Anpassen der Reaktionsbedingungen verhindert werden.

Pseudojonon zählt zu den chemischen Substanzen, die in großen Mengen hergestellt werden („High Production Volume Chemical“, HPVC) und für die von der Organisation für wirtschaftliche Zusammenarbeit und Entwicklung (OECD) eine Datensammlung zu möglichen Gefahren („Screening Information Dataset“, SIDS) angefertigt wurde.[2]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
In saurer Lösung cyclisiert Pseudojonon zu α- und β-Jonon. Bei der Verwendung von Phosphorsäure entsteht hauptsächlich α-Jonon; mit Schwefelsäure entsteht hauptsächlich β-Jonon.

Verwendung[Bearbeiten | Quelltext bearbeiten]
Pseudojonon wird Hauptsächlich zur Synthese von α- und β-Jonon verwendet.
Biologische Bedeutung[Bearbeiten | Quelltext bearbeiten]
Pseudojonon wirkt aufgrund der ähnlichen Struktur zu Juvenilhormon III bei Insekten als Juvenilhormon. Diese steuern die Ausbildung der Larvenmerkmale bzw. legen das Ziel der Häutung fest.

Literatur[Bearbeiten | Quelltext bearbeiten]
- Lexikoneintrag: Pseudojonon. In: Chemikalien-Lexikon. Stand: 6. Januar 2000. (abgerufen am 20. September 2006)
- W. Walter, W. Francke, Lehrbuch der Organischen Chemie, 23. Auflage, 1998, S. Hirzel Verlag Stuttgart - Leipzig
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c Eintrag zu Pseudojonon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Mai 2014.
- ↑ a b c d e f g OECD: Screening Information Dataset (SIDS) Initial Assessment Report (SIAR) für 3,5,9-Undecatrien-2-one, 6,10-dimethyl-, abgerufen am 3. Oktober 2014.
- ↑ a b Datenblatt Pseudoionone, technical, mixture of isomers, ≥90% (GC) bei Sigma-Aldrich, abgerufen am 29. Mai 2011 (PDF).