Selendioxid
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
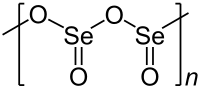
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Selendioxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | SeO2 | |||||||||||||||
| Kurzbeschreibung |
weiße, hygroskopische Nadeln[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 110,96 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte | ||||||||||||||||
| Sublimationspunkt | ||||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
löslich in Wasser (384 g·l−1 bei 14 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,02 mg·m−3[2] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Selendioxid (SeO2) ist ein Feststoff, der ab 315 °C sublimiert.[2] Es bildet sich z. B. bei der Verbrennung von elementarem Selen (Se) mit Sauerstoff.
Andere Oxide des Selens sind Selenmonoxid (SeO) und Selentrioxid (SeO3).
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Selendioxid bildet glänzende, weiße, sublimierbare Nadeln. Es kristallisiert tetragonal, Raumgruppe P42/mbc (Raumgruppen-Nr. 135) mit den Gitterparametern a = 8,36 und b = 5,06 Å bei 286 K.[5] Beim Erhitzen unter Druck bildet sich eine orangegelbe Schmelze.
Selendioxid ist gut wasserlöslich und wirkt hygroskopisch. Mit Wasser bildet es dabei Selenige Säure (H2SeO3), eine mittelstarke Säure, deren Salze Selenite oder Oxoselenate(IV) genannt werden. Diese wirkt weniger reduzierend als die verwandte Schweflige Säure, im sauren Milieu ist sie dagegen ein Oxidationsmittel:
Ebenso leicht löslich ist Selendioxid in Alkohol und konzentrierter Schwefelsäure.
Mit konzentrierten, starken Säuren kann Selendioxid hydrolyseempfindliche Selen(IV)-Verbindungen wie z. B. Selenoxychlorid (SeOCl2) bilden.
Herstellung
[Bearbeiten | Quelltext bearbeiten]Selen(IV)-oxid wird direkt aus den Elementen Selen und Sauerstoff hergestellt oder durch Wasserentzug aus Seleniger Säure.[6]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Selendioxid wird als Oxidationsmittel bei der Synthese organischer Substanzen wie z. B. der Riley-Oxidation eingesetzt.
Wenn schwere Formen von Schuppen vorliegen, wird Selendioxid als Zusatz in Shampoos verwendet.
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Selendioxid ist wie Selen und seine Verbindungen stark giftig. Der MAK-Wert beträgt 0,02 mg/m³ (gemessen als einatembarer Aerosolanteil).[2] Seine Aufnahme kann durch die intakte Haut erfolgen. Erforderlicher Arbeitsschutz: Staubschutzmaske, Gummihandschuhe, Absaugung und Belüftung am Arbeitsplatz.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Eintrag zu Selendioxid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. Juli 2014.
- ↑ a b c d e f g Eintrag zu Selendioxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ avantorinc: MSDS Selenium dioxide
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Selenverbindungen mit Ausnahme von Cadmiumsulfoselenid, soweit in diesem Anhang nicht gesondert aufgeführt im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 10. Januar 2023. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ K. Stahl, J.P. Legros, J. Galy: The crystal structure of SeO2 at 139 and 286 K. In: Zeitschrift für Kristallographie, 202, 1992, S. 99–107, doi:10.1524/zkri.1992.202.14.99.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 428–429.





