Aluminiumhydrid
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
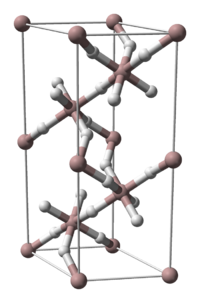
| |||||||||||||||||||
| _ Al3+ _ H− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Aluminiumhydrid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Verhältnisformel | (AlH3)x | ||||||||||||||||||
| Kurzbeschreibung |
farbloses Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 30,01 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,48 g·cm−3 [2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−46,0 kJ/mol[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Aluminiumhydrid (Alan) ist eine chemische Verbindung aus den Elementen Aluminium und Wasserstoff mit der Verhältnisformel (AlH3)x. Es ist ein farbloses Pulver, welches oberhalb von 100 °C in seine Bestandteile zerfällt. Aluminiumhydrid ist außerordentlich feuchtigkeits- und oxidationsempfindlich. Es verbrennt explosionsartig an Luft und kann zur Speicherung von Wasserstoff in wasserstoffbetriebenen Fahrzeugen eingesetzt werden.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Von Aluminiumhydrid kennt man fünf kristalline Phasen (α, γ, δ, ζ), von denen bislang nur die Struktur der α-Phase erforscht wurde. Durch Einbau von Magnesium mit einem Massenanteil (veraltet Gewichtsprozent) von 0,01 bis 3 % kann die Vakuumstabilität von α-Aluminiumhydrid signifikant erhöht werden.[5] Auch kann die Beständigkeit gegenüber Hydrolyse durch Tempern erhöht werden.[6] So behandeltes α-Aluminiumhydrid wurde intensiv als energetischer Zusatz für Raketentreibstoffe und Sprengstoffe untersucht.[7]
Synthese[Bearbeiten | Quelltext bearbeiten]
Die Darstellung von Aluminiumhydrid erfolgt zweckmäßig durch die Umsetzung von Aluminiumchlorid mit Lithiumaluminiumhydrid in Diethylether:[1]
Hierbei wird zunächst eine als Monomer anfallende Verbindung, das Etherat
gebildet, welche sich allmählich in das hochpolymere Aluminiumhydrid umwandelt.
Reaktionsverhalten[Bearbeiten | Quelltext bearbeiten]
Aluminiumhydrid reagiert mit Wasser sehr stark unter Wasserstoff-Freisetzung gemäß:
Zusammen mit anderen Metallhydriden bildet Aluminiumhydrid Alanate. Wichtigster Vertreter ist das Lithiumaluminiumhydrid (Lithiumalanat):
Wegen seiner Unlöslichkeit hat es als Reduktionsmittel kaum Bedeutung.[8]
Das Dimer Al2H6 ist isostrukturell zu Diboran (B2H6) und Digallan (Ga2H6).
Quellen[Bearbeiten | Quelltext bearbeiten]
- ↑ a b Eintrag zu Aluminiumhydrid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 14. Juli 2014.
- ↑ a b A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von Aluminium trihydride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 16. Juli 2018.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- ↑ N. E: Matzek, H. C. Roehrs, US-Patent 3 857 922, 1975, Stabilisation of light metal hydride.
- ↑ A. N. Golubkov, RU Patent 2 175 637, Method of increasing thermal stability of aluminium hydride.
- ↑ V. Weiser, N. Eisenreich, A. Koleczko, E. Roth: On the Oxidation and Combustion of AlH3 a Potential Fuel for Rocket Propellants and Gas Generators. Propellants, Explosives, Pyrotechnics, 2007, 32(3), 213–212; doi:10.1002/prep.200700022.
- ↑ Guttmann/Hengge, Anorganische Chemie, VCH, Weinheim, New York, Basel, Cambridge 1990.





