Extrauteringravidität
| Klassifikation nach ICD-10 | |
|---|---|
| O00.– | Extrauteringravidität |
| O00.0 | Abdominalgravidität |
| O00.1 | Tubargravidität |
| O00.2 | Ovarialgravidität |
| O00.8 | Sonstige Extrauteringravidität |
| O00.9 | Extrauteringravidität, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |

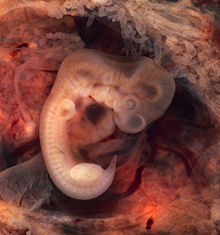
Als Extrauteringravidität (EUG) oder extrauterine Schwangerschaft, auch ektopische Schwangerschaft oder ektope Schwangerschaft, bezeichnet man eine Schwangerschaft, bei der sich das befruchtete Ei außerhalb der Gebärmutterhöhle (Cavum uteri) eingenistet hat. Die meisten extrauterinen Schwangerschaften treten im Eileiter auf und werden daher Eileiterschwangerschaften genannt. Die Implantation des Embryos kann jedoch auch in den Eierstöcken und der Bauchhöhle auftreten. Schwangerschaften im Gebärmutterhals, der Gebärmutterwand (beispielsweise in einer Narbe nach Kaiserschnitt) und im intramuralen Teil des Eileiters werden in der deutschen Übersetzung der ICD-10 als Extrauteringravidität bezeichnet, sind jedoch, streng genommen, intrauterine, aber ektope Schwangerschaften.[1]
Mit Ausnahme der Bauchhöhlenschwangerschaft ist der Embryo bei einer Extrauteringravidität zumeist nicht überlebensfähig. In der Regel stirbt der Embryo nach einigen Wochen durch eine Unterversorgung an Nährstoffen ab, da der Implantationsort keine optimalen Voraussetzungen bietet. Zudem stellt die Extrauteringravidität, auch die Bauchhöhlenschwangerschaft, eine Gefahrensituation für die Mutter dar, da es zu schweren, lebensbedrohlichen inneren Blutungen, etwa durch Zerreißung des Eileiters, kommen kann.
Durch die verbesserten diagnostischen Möglichkeiten lassen sich extrauterine Schwangerschaften heute sehr früh erkennen. Besonders in Ländern mit schlechter Schwangerschaftsbetreuung sind Extrauteringraviditäten jedoch trotz der verbesserten Diagnostik eine bedeutende Ursache mütterlicher Morbidität und Mortalität.[2]
Die Behandlung einer Extrauteringravidität besteht üblicherweise in der operativen Entfernung der Schwangerschaft, heute meist über eine Bauchspiegelung. Alternativ kann in manchen Fällen eine medikamentöse Behandlung erfolgreich sein.
Epidemiologie[Bearbeiten | Quelltext bearbeiten]
Extrauteringraviditäten kommen in einer Häufigkeit von 1 bis 2 auf 100 intrauterine Schwangerschaften vor. In den meisten Fällen handelt es sich um eine Tubargravidität, die in 4/5 der Fälle im ampullären Teil des Eileiters lokalisiert ist.[3] 4 bis 9 % der schwangerschaftsbedingten Mortalität in entwickelten Staaten gehen auf extrauterine Schwangerschaften zurück.[4][2] Die Fertilitätsrate nach Extrauteringravidität beträgt durchschnittlich etwa 55 %. Es besteht jedoch ein Rezidivrisiko von ca. 15 %.[3]
| Alter (Jahre) | Inzidenzrate (%) |
|---|---|
| < 20 | 0,4 |
| 20–30 | 0,7 |
| 30–40 | 1,3–2,0 |
Im letzten Drittel des 20. Jahrhunderts wurde parallel mit einem Anstieg von sexuell übertragenen Infektionen eine Zunahme der Extrauteringraviditäten verzeichnet.[1] In den USA stieg die Zahl der Neuerkrankungen von 17.800 im Jahr 1970 (Inzidenzrate 4,5 je 1.000 Schwangerschaften) auf 88.400 im Jahr 1989 (16,0 je 1.000 Schwangerschaften).[5] Auch danach war ein weiterer Anstieg zu verzeichnen.[6] Die Sterblichkeit an dieser Erkrankung ging jedoch zurück. Sie ist jedoch dort der häufigste Grund für Todesfälle in den ersten drei Schwangerschaftsmonaten und die vierthäufigste Mortalitätsursache in der gesamten Schwangerschaft.[7]
Als weitere Ursache der gestiegenen Inzidenz wird die vermehrte Anwendung der In-vitro-Fertilisation bei Frauen über 30 Jahren angesehen.[1] Sie kann allerdings zudem auch durch die verbesserte Früherkennung und die häufiger durchgeführte intrauterine Kontrazeption (Empfängnisverhütung) mittels Spirale bedingt sein.[4]
Entstehung[Bearbeiten | Quelltext bearbeiten]

In einer normalen Schwangerschaft erreicht der Embryo im Stadium der Blastozyste zwischen dem 5. und 6. Tag nach der Befruchtung die Gebärmutterhöhle und beginnt dort am 6./7. Tag, sich in die Gebärmutterschleimhaut einzunisten. Diesen Vorgang nennt man Nidation oder Implantation.[8]
Während der ersten Tage ist der Embryo demnach völlig vom umgebenden Milieu abhängig. Kommt es im Ablauf des Transports in die Gebärmutterhöhle oder der Nidation zu einer Störung, kann hieraus eine extrauterine Implantation resultieren. Bei einer typischen Extrauteringravidität heftet sich der Embryo an die Eileiterschleimhaut an und wächst in die Schleimhaut hinein. Etwa 1 % der Embryonen siedeln sich außerhalb der Gebärmutterhöhle an.[3]
Ursachen[Bearbeiten | Quelltext bearbeiten]
Es gibt eine ganze Reihe bekannter Risikofaktoren für eine Extrauteringravidität. Jedoch lassen sich in einem Drittel[9] bis zur Hälfte[10] der Fälle keine solchen Faktoren nachweisen.
Zu den Risikofaktoren zählen entzündlich-bedingte Erkrankungen im Beckenbereich (Pelvic Inflammatory Disease), Infertilität, die Nutzung von Intrauterinpessaren, eine frühere Exposition mit Diethylstilbestrol, vorangegangene Eingriffe am Eileiter (Tubenchirurgie), intrauterine Eingriffe (Ausschabungen), Rauchen, frühere ektope Schwangerschaften und eine Sterilisation.[11] Obwohl frühere Publikationen eine Verbindung zwischen Endometriose und ektopen Schwangerschaften vermuteten, ließ sich diese nicht nachweisen.[12]
Eileiterschädigung[Bearbeiten | Quelltext bearbeiten]
Die Flimmerhärchen der Eileiterschleimhaut transportieren die befruchtete Eizelle, die sich dabei durch Teilung zum Embryo entwickelt, zur Gebärmutter. Die Zahl der Zilien war bei Eileiterschwangerschaften zuweilen reduziert, was zur Hypothese eines Zilienschadens führte, der für ektope Schwangerschaften verantwortlich ist.[13] Ein Review aus dem Jahr 2010 unterstützte die Hypothese, dass Eileiterschwangerschaften durch einen gestörten embryo-tubaren Transport und Veränderungen in der Eileiterumgebung verursacht werden, so dass es zu einer frühen Implantation kommt.[14]
Frauen mit entzündlich-bedingten Veränderungen im Becken (Pelvic Inflammatory Disease) haben häufiger eine ektope Schwangerschaften.[15] Dies resultiert aus der Ausbildung von Narbengewebe in den Eileitern, welches die Flimmerhärchen zerstört.[16] Bei einem vollständigen Verschluss beider Eileiter sind Spermien und Eizelle nicht in der Lage, zusammenzutreffen, so dass eine Befruchtung der Eizelle nicht möglich ist, und daher keine Schwangerschaft eintritt. Chirurgische Maßnahmen an den verschlossenen Eileitern haben das Ziel, diese wieder zu eröffnen. Damit wird jedoch der natürliche Schutz aufgehoben und das Risiko einer ektopen Schwangerschaft steigt. Intrauterine Verwachsungen wie beim Asherman-Syndrom können einerseits eine Zervixschwangerschaft verursachen. Verhindern diese Verwachsungen teilweise den Zugang zum Eileiter, kann es andererseits aber auch zu einer Eileiterschwangerschaft kommen.[17][18][19] Das Asherman-Syndrom kann durch intrauterine Eingriffe, wie Kürettagen verursacht werden.[17] Auch eine urogenitale Tuberkulose kann Ursache eines Asherman-Syndroms sein. Zusätzlich entstehen dabei Verwachsungen der Eileiter, die ebenfalls zu einer Extrauteringravidität führen können.[20]
Auch eine Sterilisation kann das Risiko einer Extrauteringravidität erhöhen. 70 % aller Schwangerschaften nach Verödung der Eileiter sind ektope Schwangerschaften, während 70 % der Schwangerschaften nach Eileiterverschluss durch einen Clip intrauterin zu finden sind. Eine Refertilisierung nach Sterilisation birgt ebenfalls das Risiko einer ektopen Schwangerschaft. Dieses ist höher, wenn stärker destruierende Verfahren, wie die Koagulation oder eine Teilentfernung der Eileiter gewählt wurden, als bei weniger destruktiven Methoden, wie dem Clipping. Eine frühere Eileiterschwangerschaft erhöht das Risiko einer erneuten Eileiterschwangerschaft auf 10 %. Dieses Risiko verringert sich auch nicht, wenn der betroffene Eileiter entfernt wurde und der andere unauffällig schien.[16]
Andere Ursachen[Bearbeiten | Quelltext bearbeiten]
Tabakrauchen ist mit einem höheren Risiko für Extrauteringraviditäten verbunden.[16] Ebenso haben Frauen, die intrauterin Diethylstilbestrol (DES) ausgesetzt waren, ein bis zu dreifach erhöhtes Risiko im Vergleich zu Frauen ohne diese Exposition.
Es wurde auch vermutet, dass eine krankhaft vermehrte Bildung von Stickstoffmonoxid, durch erhöhte i-Stickstoffmonoxid-Synthase-Aktivität (iNOS), die Schlagzahl der Flimmerhärchen und die Kontraktion der glatten Muskelzellen reduziert, damit den Embryotransport beeinträchtigt und dadurch zu einer ektopen Schwangerschaft führt.[21]
Obwohl einige Untersuchungen ein höheres Risiko mit zunehmendem Alter zeigten, wird angenommen, dass das Alter eher einen Surrogatmarker für andere Risikofaktoren darstellt.[16]
Klassifikation[Bearbeiten | Quelltext bearbeiten]

N normale Einnistung (Nidation)
a Bauchhöhlenschwangerschaft
b interstitielle oder cornuale Eileiterschwangerschaft
c isthmische Eileiterschwangerschaft
d ampulläre Eileiterschwangerschaft
e infundibuläre Eileiterschwangerschaft
f Ovarschwangerschaft
g Zervixschwangerschaft
h intramurale Schwangerschaft
Die Mehrheit der Extrauteringraviditäten finden sich in einem der beiden Eileiter und wird dann Tubargravidität oder Eileiterschwangerschaft genannt. Ektope Schwangerschaften kommen jedoch auch im Eierstock, dem Gebärmutterhals, der Gebärmutterwand oder in der Bauchhöhle vor. Weitere seltene Lokalisationen sind Schwangerschaften im Ligamentum latum, der Vagina, sowie in einem rudimentären Uterushorn bei angeborenen Fehlbildungen der Gebärmutter. In Einzelfällen kam es auch nach Gebärmutterentfernung (Hysterektomie) zu Schwangerschaften. Kommt es durch die Befruchtung zweier Eizellen zu einer gleichzeitigen intrauterinen und einer ektopen Schwangerschaft, wird dies heterotope Schwangerschaft genannt.
Tubargravidität[Bearbeiten | Quelltext bearbeiten]
Etwa 96 % aller extrauterinen Schwangerschaften sind Eileiterschwangerschaften.[3] Die Schwangerschaft besteht im Eileiter entweder fimbrientrichternah (infundibulär) (5 % aller EUG), im ampullaren Teil (80 %), im Isthmus (12 %) und im cornualen oder interstitiellen Teil des Eileiters (2 %).[16] Die Sterblichkeit bei einer isthmischen oder interstitiellen Eileiterschwangerschaft ist höher, da es bei stärkerer Gefäßversorgung (Vaskularisierung) häufiger zu starken inneren Blutungen, wie aus dem Ramus uterinus der Arteria ovarica, einer Verbindung zur Arteria uterina, im angloamerikanischen Sprachraum auch als Sampson-Arterie bekannt, kommt.
Ovargravidität[Bearbeiten | Quelltext bearbeiten]
Etwa 0,2–2 % aller Extrauteringraviditäten finden sich in einem Eierstock.[4] Eine Ovarschwangerschaft lässt sich von einer Eileiterschwangerschaft durch die Spiegelberg-Kriterien, benannt nach dem deutschen Gynäkologen Otto Spiegelberg (1830–1881), unterscheiden. Danach besteht eine Ovarschwangerschaft, wenn sich
- der Fruchtsack im Eierstock befindet
- die ektope Schwangerschaft durch das Lig. ovarii proprium an die Gebärmutter herangezogen ist
- Eierstockgewebe in der Wand des Fruchtsacks histologisch nachgewiesen werden kann
- der Eileiter der betroffenen Seite intakt ist.[22][23]
Die klinische Symptomatik und die diagnostischen Befunde entsprechen denen der Tubargravidität. In den 1990er Jahren beobachtete man eine Zunahme der Ovargraviditäten, welche mit dem Gamete intrafallopian transfer (GIFT), einem Verfahren der assistierten Reproduktion, bei dem Eizellen und Spermien gemeinsam in den Eileiter eingebracht werden, in Zusammenhang gebracht wurden.[24]
Zervixgravidität[Bearbeiten | Quelltext bearbeiten]
Mit 0,2–0,5 % der ektopen Schwangerschaften ist die Zervixgravidität sehr selten.[4] Aufgrund der engen anatomischen Beziehung kommt es meist frühzeitig zu einem Kontakt zum Stromgebiet der Arteria uterina, so dass es bei einer Kürettage zu massiven, unstillbaren Blutungen kommen kann, die eine Hysterektomie notwendig machen können. Mit der transvaginalen Ultraschalluntersuchung lassen sich Zervixschwangerschaften üblicherweise frühzeitig gut erkennen.[3] Als Diagnosekriterien gelten[25]:
- leere Gebärmutter (Uterus)
- tonnenförmiger Gebärmutterhals (Cervix uteri)
- Gestationssack unter dem Niveau des Orificium internum uteri
- "Sliding Sign": Bei Druckausübung auf die Gebärmutter mit dem Schallkopf ist bei extrauteriner zervikaler Schwangerschaft der Gestationssack verschieblich zum Zervikalkanal. Bei regelrechter Schwangerschaft aufgrund der Verwachsung ist der Gestationssack nicht verschieblich zum Zervikalkanal.
- Blutfluss um den Gestationssack im Farbdoppler
Intramurale Gravidität[Bearbeiten | Quelltext bearbeiten]
Als intramurale Gravidität wird eine Schwangerschaft bezeichnet, die in der Gebärmuttermuskulatur (Myometrium) implantiert und nicht von Dezidua umgeben ist. Risikofaktoren sind die Adenomyosis uteri und vorangegangene Operationen an der Gebärmutter, wie ein Kaiserschnitt, bei denen es zu einer Einnistung in der Narbe kommen kann. Intramurale Schwangerschaften sind mit < 1 % aller Extrauteringraviditäten aber sehr selten.[4]
Bauchhöhlenschwangerschaft[Bearbeiten | Quelltext bearbeiten]
Etwa 1 % der extrauterinen Schwangerschaften ist in der Bauchhöhle lokalisiert.[4] Wegen der oft geringen Symptomatik werden abdominale Schwangerschaften zuweilen erst spät erkannt. Bei fortgeschrittenen Schwangerschaften sitzt die Plazenta auf Bauchorganen oder dem Bauchfell und wurde ausreichend mit Blut versorgt. Dies ist üblicherweise am Darm und Mesenterium der Fall. Es wurde aber auch von anderen Lokalisationen, wie nahe der Nieren-, Leberarterie oder der Aorta berichtet.
Obwohl es in sehr seltenen Fällen Lebendgeburten bei Bauchhöhlenschwangerschaften gibt, sind sie aufgrund des hohen Blutungsrisikos außerordentlich gefährlich. Die meisten Bauchhöhlenschwangerschaften müssen daher nach Diagnosestellung deutlich vor der Überlebensfähigkeit des Feten, in fortgeschrittenem Schwangerschaftsalter durch Laparotomie, entfernt werden.[3][4]
Dabei ist die mütterliche Morbidität und die Mortalität von Mutter und Kind hoch (Mutter 20 %, Kind 80 %[4]), da auch die Entfernung der Plazenta meist zu unkontrollierbaren Blutungen führt.[26][27] Aus diesem Grund werden beispielsweise Darmsegmente zusammen mit der Plazenta entfernt.[28][29][30]
Je nach Lokalisation der Plazenta muss auch erwogen werden, die Plazenta zu belassen, wo sie im Laufe der Zeit kalzifiziert oder resorbiert wird.[3]
Tubarabort[Bearbeiten | Quelltext bearbeiten]
Bei der Nidation kommt es zur Eröffnung von Blutgefäßen mit einer Blutung. Der Eileiter kann sich dabei mit Blut füllen und wird dann als Hämatosalpinx bezeichnet. Bei einer Einnistung in der Nähe des Fimbrientrichters kommt es nach dem Aufbruch der Fruchtkapsel zu Blutungen aus dem Fimbrienende. Das Blut kann zum Herausdrücken der Schwangerschaft aus dem Eileiter führen. Dieser sogenannte Tubarabort ist jedoch selten.[4]
Heterotope Schwangerschaft[Bearbeiten | Quelltext bearbeiten]
In seltenen Fällen kommt es durch die Befruchtung zweier Eizellen zu einer gleichzeitigen intrauterinen und einer ektopen Schwangerschaft. Dies wird heterotope Schwangerschaft genannt. Dabei wird aufgrund der auftretenden Beschwerden häufig die intrauterine Schwangerschaft erst nach der ektopen entdeckt. Da eine Extrauteringravidität frühzeitig operativ entfernt wird, ist die intrauterine Schwangerschaft im Ultraschall häufig noch nicht darstellbar. Bei nach der Operation steigenden hCG-Werten besteht die Möglichkeit einer sich noch entwickelnden normalen Schwangerschaft.
Obwohl heterotope Schwangerschaften sehr selten sind, steigt deren Häufigkeit an. Dies wird der zunehmenden Anwendung der IVF zugeschrieben. Die Überlebensrate des intrauterinen Embryos beträgt etwa 70 %.
Es wurden auch erfolgreiche Schwangerschaften nach Ruptur des Eileiters berichtet, wenn sich die Plazenta auf Bauchorganen oder der Gebärmutteraußenwand ansiedelt.[31][32]
Persistierende Extrauteringravidität[Bearbeiten | Quelltext bearbeiten]
Von einer persistierenden Extrauteringravidität spricht man, wenn nach der organerhaltenden Entfernung der ektopen Schwangerschaft Trophoblastanteile fortbestehen. Bei 15 bis 20 % der Frauen kommt es nach einer solchen Operation zu einem erneuten Wachstum von Trophoblastgewebe, welches teilweise in tieferen Eileiterschichten eingebettet ist. Es bildet neues hCG und kann nach Wochen zu erneuten klinischen Symptomen, wie Blutungen, führen.[33] Daher werden nach ektopen Schwangerschaften die Serum-hCG-Werte kontrolliert, um deren Absinken zu beobachten. Es ist zudem möglich zeitgleich zur Operation Methotrexat zu verabreichen.[4]
Schwangerschaft nach Hysterektomie[Bearbeiten | Quelltext bearbeiten]
In wenigen Einzelfällen wurde über extrauterine Schwangerschaften nach einer Hysterektomie berichtet. Dabei handelte es sich mehrheitlich um frühe Extrauteringraviditäten, die zum Zeitpunkt der Gebärmutterentfernung schon bestanden und nicht erkannt worden waren. Aber selbst mehrere Jahre nach Hysterektomie kam es zu Schwangerschaften, die über Fisteln zwischen Scheide und Bauchhöhle entstanden sein müssen. Auch nach Erhalt des Gebärmutterhalses wurde in Einzelfällen über spätere Extrauteringraviditäten berichtet.[3]
Symptomatik[Bearbeiten | Quelltext bearbeiten]
Frühe Symptome können bei einer Extrauteringravidität sehr milde sein oder gänzlich fehlen. Klinisch zeigt sich eine ektope Schwangerschaft zwischen der 5. und 8. Woche nach Beginn der letzten Menstruationsblutung (durchschnittlich nach 7,2 Wochen). Stehen moderne diagnostische Möglichkeiten nicht zur Verfügung, kommt es häufiger erst zu späteren Entdeckungen einer Extrauteringravidität.
Mögliche Symptome bei einer Extrauteringravidität können sein:
- Brustspannen
- häufiger Harndrang und Dysurie
- ausbleibende Periode (Sekundäre Amenorrhoe)
- Übelkeit, Erbrechen
- Unterbauchschmerzen (meist auf der Seite einer Eileiterschwangerschaft)
- vaginale Blutung, meist von geringer Stärke, die eine Unterscheidung zu einer gestörten Frühschwangerschaft, einer Nidationsblutung oder auch einer normalen Schwangerschaft erschwert
Im weiteren Verlauf kommt meist es zu stärkeren Schmerzen aufgrund der inneren Blutungen und zu vaginalen Blutungen durch fallende Progesteron-Spiegel. Bei der Entstehung der Schmerzen spielen bei einer Extrauteringravidität Entzündungen keine Rolle. Da Entzündungen im Beckenbereich bei einer Schwangerschaft extrem selten auftreten, kann bei positivem Schwangerschaftstest eine Adnexitis nahezu ausgeschlossen werden. Eine Extrauteringravidität kann zudem Symptome verursachen, wie man sie auch bei der Appendizitis, Erkrankungen der Harnwege oder des Magen-Darm-Trakts findet. Der Schmerz wird durch Prostaglandine, die an der Implantationsstelle freigesetzt werden, oder freies Blut in der Bauchhöhle, welches das Bauchfell reizt, hervorgerufen.
Diagnosestellung[Bearbeiten | Quelltext bearbeiten]

Eine Extrauteringravidität muss bei jeder Frau mit Bauchschmerzen oder vaginaler Blutung bei positivem Schwangerschaftstest angenommen werden. Eine Ultraschalluntersuchung, die außerhalb der Gebärmutter einen Fruchtsack mit fetalen Anteilen und Herzaktionen zeigt, ist beweisend für eine Extrauteringravidität.
Ein zu geringer Anstieg des β-hCG im Serum kann ebenfalls ein Hinweis auf eine ektope Schwangerschaft sein. Ab einem β-hCG-Wert von etwa 1500 IU/ml ist eine normale intrauterine Schwangerschaft im Ultraschall mit hoher Wahrscheinlichkeit darstellbar. Zeigt eine hochauflösende transvaginale Sonografie bei einem solchen Wert keine intrauterine Schwangerschaft, muss eine Extrauteringravidität in Betracht gezogen werden.
In den letzten Jahren gewinnt der Einsatz der Progesteronbestimmung immer mehr an Bedeutung, insbesondere bei niedrigen β-HCG-Werten, wo die Ultraschalldiagnostik noch keine Aussage hat. So spricht ein hoher Progesteronwert bei gleichzeitig noch niedrigem β-HCG für eine frühe, jedoch wahrscheinlich intakte intrauterine Schwangerschaft. Ist dieser Progesteronwert jedoch niedrig, so ist die Schwangerschaft gestört und eine ektope Gravidität wahrscheinlicher.[34]
Mittels einer Bauchspiegelung oder Laparotomie lässt sich eine ektope Schwangerschaft visuell darstellen. Dabei kann es nach Tubarabort oder Tubarruptur schwierig sein, das Schwangerschaftsgewebe zu finden. Eine Bauchspiegelung in einer frühen Schwangerschaftswoche kann trotz Eileiterschwangerschaft einen normalen Befund bieten.
Durch eine Punktion des Douglas-Raums (Kuldozentese) wurde früher, vor Einführung des Ultraschalls in die klinische Routine, eine intraabdominale Blutung nachgewiesen. Sie spielt heute in der Diagnostik einer Extrauteringravidität keine Rolle mehr. Das Cullen-Zeichen kann ebenfalls eine rupturierte Eileiterschwangerschaft mit Blutungen in den Bauchraum anzeigen.
Behandlung[Bearbeiten | Quelltext bearbeiten]
Chirurgische Therapie[Bearbeiten | Quelltext bearbeiten]
Bei eingetretener Blutung oder nachgewiesener Herzaktion ist eine chirurgische Behandlung notwendig. Mittels Bauchspiegelung oder per Bauchschnitt kann dann die Schwangerschaft entfernt werden. Dazu ist bei einer Eileiterschwangerschaft häufig eine Eröffnung des Eileiters (Salpingotomie) mit Erhalt des Eileiters erforderlich. Alternativ kann auch der Eileiter komplett entfernt werden (Salpingektomie).[35]
-
Entfernung einer Eileiterschwangerschaft aus dem rechten Eileiter
-
Rechter Eileiter nach Entfernung einer Eileiterschwangerschaft (Wunde durch Pfeil markiert)
-
Operationspräparat eines entfernten Eileiters mit Embryo und Plazenta
Medikamentöse Therapie[Bearbeiten | Quelltext bearbeiten]
Eine frühe ektope Schwangerschaft kann seit 1993 auch durch die systemische oder lokale Gabe von Methotrexat behandelt werden.[36][37] Das Medikament, ein Zytostatikum, hemmt das Wachstum des Embryos und verursacht einen Abort, welcher dann in der Bauchhöhle resorbiert oder vaginal ausgestoßen wird. Kontraindikationen sind Leber-, Nieren- oder Bluterkrankungen, sowie eine ektope Schwangerschaft von > 3,5 cm.
Mögliche Komplikationen[Bearbeiten | Quelltext bearbeiten]
Die häufigste Komplikation einer Extrauteringravidität sind innere Blutungen, die zum hypovolämischen Schock führen. Die Sterblichkeit ist jedoch gering, wenn ein Zugang zu moderner medizinischer Versorgung besteht.
-
Schematische Darstellung einer Tubarruptur
-
Rupturierte cornuale Eileiterschwangerschaft (OP-Präparat)
-
Schematische Darstellung eines Tubaraborts
-
Tubarabort aus dem rechten Eileiter mit Ausbildung einer Hämatosalpinx
Prognose[Bearbeiten | Quelltext bearbeiten]
Die Fertilität nach Extrauteringravidität hängt von mehreren Faktoren ab. Der wichtigste Faktor ist dabei ein unerfüllter Kinderwunsch in der Vergangenheit.[38] Auch die Wahl der Behandlung spielt eine Rolle. So ist die Rate an intrauterinen Folgeschwangerschaften nach Methotrexat-Behandlung höher als nach chirurgischer Therapie.[39] Die Chancen für eine Schwangerschaft sind nach Erhalt des Eileiters besser als nach Entfernung desselben.[39]
Lebendgeburten bei Bauchhöhlenschwangerschaften[Bearbeiten | Quelltext bearbeiten]
Wiederholt wurde über Lebendgeburten bei Bauchhöhlenschwangerschaften berichtet, die durch Bauchschnitt (Laparotomie) geboren wurden.
- 1986 wurde in Deutschland unter dem Verdacht auf eine Uterusruptur ein Bauchschnitt durchgeführt und dabei eine Bauchhöhlenschwangerschaft am Termin entwickelt.[40]
- 1999 wurde in Ogden (Utah), in den USA ein gesundes Mädchen geboren, das sich außerhalb der Gebärmutter entwickelt hatte, was bei geburtshilflicher Sonografie nicht erkannt worden war. Erst bei einem Kaiserschnitt wurde die Lokalisation der Schwangerschaft festgestellt.[41][42]
- Ebenfalls 1999 wurde eine 32-jährige britische Frau von Drillingen entbunden. Dabei hatten sich zwei Kinder in der Gebärmutter entwickelt und das dritte nach Ruptur des Eileiters in der Bauchhöhle.[43]
- 2008 wurde bei einer britischen 37-jährigen Frau eine Schwangerschaft am Omentum majus festgestellt. Das Kind wurde in der 28. Schwangerschaftswoche geboren. Mutter und Kind überlebten.[44]
- 2008 fand man bei einer 34-jährigen australischen Frau in der 38. Schwangerschaftswoche eine Ovarschwangerschaft. Das Mädchen wog 2.800 g und war gesund.[45][46]
- 2011 wurde eine 23-jährige Frau in Saudi-Arabien am Geburtstermin von einem gesunden Kind entbunden. Bei einem Kaiserschnitt wegen Beckenendlage fand sich eine Bauchhöhlenschwangerschaft. Bei den Ultraschalluntersuchungen in der Schwangerschaft war der Verdacht auf einen Uterus bicornis, eine Fehlbildung der Gebärmutter, geäußert worden. Zudem hatte die Frau in der Schwangerschaft über Beschwerden im Unterbauch berichtet.[47]
2008 wurden jedoch in einer Publikation 163 Fälle fortgeschrittener Bauchhöhlenschwangerschaften seit 1946 analysiert. Dabei fand sich eine um 19 % höhere Inzidenz in nicht-industrialisierten Ländern. In nur 45 % der beschriebenen Fälle wurde die Diagnose vor der Operation korrekt gestellt. 72 % der Feten und 12 % der Mütter verstarben.[48]
Veterinärmedizin[Bearbeiten | Quelltext bearbeiten]

Extrauteringraviditäten kommen auch bei anderen Säugetieren, insbesondere allen Haustieren, vor. Dabei sind ektope Schwangerschaften bei Rindern am häufigsten anzutreffen.
Während beim Menschen überwiegend primäre Extrauteringraviditäten auftreten, sich die Schwangerschaft gleich an der falschen Stelle eingenistet hat, handelt es sich bei Tieren meist um sekundäre ektope Schwangerschaften. Dabei gelangt ein Embryo oder Fetus aus der Gebärmutter heraus und nistet sich an anderer Stelle, meist in der freien Bauchhöhle, wieder ein.
Ovargraviditäten sind im Tierreich bislang nicht beschrieben. Eileiterschwangerschaften haben in der Veterinärmedizin ebenfalls keine Bedeutung.[49]
Geschichte[Bearbeiten | Quelltext bearbeiten]
Die Erstbeschreibung einer Extrauteringravidität im Jahr 963 wird Albucasis (936–1013) zugeschrieben. Er berichtete über eine Patientin mit einer Schwellung des Bauches, aus dem Eiter über die Bauchdecke abfloss, in dem sich ein menschliches Skelett fand. Jacob Noierus führte 1591 und 1596 erste chirurgische Eingriffe bei ektoper Schwangerschaft durch, bei denen er durch einen Bauchschnitt den Fetus lediglich herauszog.[50] Der Franzose Jean Riolan (1577–1657) aus Paris berichtete 1604 zuerst über eine rupturierte Eileiterschwangerschaft. Die Patientin war im 4. Monat ihrer achten Schwangerschaft einen Tag nach dem Beginn der Symptomatik verstorben.[50]

1672 veröffentlichte Reinier de Graaf in seinem Werk De mulierum organis in generationi inservientibus tractatus novus. eine bildliche Darstellung nach einer Arbeit des französischen Chirurgen Benoit Vassal über Obduktionsbefunde bei einer 32-jährigen Frau, die bereits elf Kinder geboren hatte und am 6. Januar 1669 an einer Blutung bei einer Eileiterschwangerschaft verstorben war.[51][52] 1693 wurde von Bussière aus Paris eine unrupturierte Eileiterschwangerschaft bei der Obduktion einer exekutierten jungen Frau gefunden. Die erste Ovarschwangerschaft beschrieb der französische Arzt de Saint Maurice aus dem Périgord 1682. Auch bei dieser Frau wurde die Diagnose erst nach dem Tode gestellt.[50]
Die erste erfolgreiche Operation bei einer EUG über einen Bauchschnitt führte der Amerikaner John Bard (1716–1799), der Vater des Geburtshelfers Samuel Bard (1742–1821), 1759 in New York durch. Er entfernte einen toten, aber reifen Fetus bei einer 28-jährigen Frau, die den Eingriff überlebte.[53]
William Baynham (1749–1814) berichtete über zwei Fälle einer EUG, die er operativ behandelte. Dabei war eine bereits 5 Jahre zuvor eingetreten.[54]
Erfolgreich verlief auch die Entfernung einer ektopen Schwangerschaft über die Scheide 1816 durch John King aus South Carolina.[55]
Bis zum Ende des 19. Jahrhunderts wurde die Diagnose durch das Tasten eines Tumors seitlich oder hinter der vergrößerten Gebärmutter, unsicheren Schwangerschaftszeichen, wie Magen- und Brustbeschwerden, Ausbleiben der Menstruation, der verstärkten Durchblutung der Scheide und dem Hin-und-Herschwingen (Ballotieren) des Tumorinhalts gestellt. Da man den ektopen Fetus als Ursache der Sterblichkeit ansah, war das primäre Behandlungsziel ein Abtöten desselben. Dies wurde durch Hungern, Einläufe und Aderlässe bei der Mutter sowie die Anwendung von Strychnin, Elektrotherapie, Galvanotherapie und Injektion von Morphium in den Fruchtsack versucht.[56] Die Prognose war jedoch schlecht. Die Sterblichkeitsrate betrug 72 bis 99 %. Eine Extrauteringravidität war zu der Zeit eine der häufigsten Todesursachen von jungen Frauen.[50][57] Dies besserte sich erst mit Einführung der Eileiterentfernung (Salpingektomie) durch Robert Lawson Tait (1845–1899), der diese 1884 erstmals durchführte.[58][59][60]
Der deutsche Gynäkologe Richard Frommel (1854–1912) setzte sich, im Gegensatz zu der damals geltenden Lehrmeinung, die abwartendes Verhalten empfahl, als einer der Ersten für eine sofortige operative Intervention bei der extrauterinen Schwangerschaft ein.[61][62]
Betrug die Sterblichkeit zwischen 1908 und 1920 noch 12,3 %,[63] sank sie im Zeitraum von 1920 bis 1937 auf 11,7 % und betrug zwischen 1937 und 1947 nur noch 1,7 bis 2,7 %.[64] Dies war das Ergebnis der Einführung von Bluttransfusionen als Routineverfahren, des besseren Verständnisses der Schockmechanismen, der verbesserten Betreuung nach Operationen sowie der früheren Diagnosestellung durch vermehrten Einsatz der Kuldozentese und Schwangerschaftstests.[50]
Als weiteres diagnostisches Verfahren wurde am Anfang der 1960er Jahre die Kuldoskopie genutzt.[65] Die Idee der direkten Betrachtung der Bauchhöhle entstand jedoch schon um den Anfang des 20. Jahrhunderts. Schon 1901 hatte der russische Arzt D. O. Ott über eine Eröffnung des Douglas-Raums (Kuldotomie), Vaginalspiegel und einen Kopfspiegel Becken- und Bauchorgane darstellen können, was er Ventroskopie nannte.[66]
Der Schwede Hans Christian Jacobaeus (1879–1937) beschrieb 1910 als Erster die Technik der Laparoskopie und nutzte diese vor allem zur Diagnostik bei Patienten mit Aszites und Lebererkrankungen.[67][68] 1929 entwickelte der Internist Hans Kalk (1895–1973) ein neuartiges Laparoskop.[69] Es ermöglichte eine exakte Diagnostik und Kalk erkannte bereits, dass „für die Laparoskopie in der Gynäkologie ein großes Indikationsgebiet sich eröffnen würde“,[70] was sich nach der Einführung durch Hans Frangenheim bestätigte.[71][72]
1953 brach W. B. Stromme mit der Praxis der Entfernung des Eileiters, indem er diesen zur Entfernung des Schwangerschaftsprodukts eröffnete und dabei erhalten konnte.[73] Zwanzig Jahre später gelang H. I. Shapiro und D. H. Adler 1973 die laparoskopische Entfernung einer Eileiterschwangerschaft.[74]
Eine heute immer frühere Diagnostik ist durch deutlich verbesserte Schwangerschaftstests, die quantitative Bestimmung des β-hCG und die vaginale Ultraschalluntersuchung möglich geworden.[50]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Jürgen Hucke: Extrauteringravidität. Wissenschaftliche Verlagsgesellschaft, Stuttgart 1997, ISBN 3-8047-1480-3.
- W. Pschyrembel, J. W. Dudenhausen: Praktische Geburtshilfe. 17. Auflage. Walter de Gruyter, Berlin 1991, ISBN 3-11-012881-0, S. 565 ff.
- Peter Oppelt: Extrauteringravidität. In: Manfred Kaufmann, Serban-Dan Costa, Anton Scharl: Die Gynäkologie. 2. Auflage. Springer Verlag, 2006, ISBN 3-540-25664-4, S. 286–301.
- E. Kucera, R. Lehner, Peter Husslein: Extrauteringravidität. In: Henning Schneider, Peter Husslein, Karl Theo M. Schneider: Die Geburtshilfe. 3. Auflage. Springer Verlag, 2006, ISBN 3-540-33896-9, S. 32–39.
- Heinrich Schmidt-Matthiesen, Diethelm Wallwiener: Gynäkologie und Geburtshilfe. Schattauer Verlag, 2007, ISBN 978-3-7945-2618-5, S. 179.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Eileiterschwangerschaft. Informationen der Arbeitsgemeinschaft Gynäkologische Endoskopie e. V. der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe
- Eintrag zu Extrauteringravidität im Flexikon, einem Wiki der Firma DocCheck
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d E. Kucera, R. Lehner, Peter Husslein: Extrauteringravidität. In: Henning Schneider, Peter Husslein, Karl Theo M. Schneider: Die Geburtshilfe. 3. Auflage. Springer Verlag, 2006, ISBN 3-540-33896-9, S. 32–39.
- ↑ a b WHO: Maternal and perinatal health. zuletzt aufgerufen am 9. November 2011.
- ↑ a b c d e f g h Jürgen Hucke, Ulrich Füllers: Extrauterine Schwangerschaft. In: Gynäkologe. 38 (2005), S. 535–552, doi:10.1007/s00129-005-1705-1
- ↑ a b c d e f g h i j J. Lermann, A. Müller, C. Schulze, S. Becker, A. Boosz, S. P. Renner, M. W. Beckmann: Die Extrauteringravidität. In: Frauenheilkunde. up2date 3 (2009), S. 383–402, doi:10.1055/s-0029-1224626
- ↑ Surveillance for Ectopic Pregnancy - United States, 1970–1989. In: MMWR. 42 (1993)(SS-6), S. 73–85, wonder.cdc.gov
- ↑ B. Trabert, V. L. Holt, O. Yu, S. K. Van Den Eeden, D. Scholes: Population-based ectopic pregnancy trends, 1993–2007. In: Am J Prev Med. 40 (2011), S. 556–560, PMID 21496755
- ↑ A. A. Creanga, C. K. Shapiro-Mendoza, C. L. Bish, S. Zane, C. J. Berg, W. M. Callaghan: Trends in ectopic pregnancy mortality in the United States: 1980–2007. In: Obstet Gynecol. 117 (2011), S. 837–843, PMID 21422853.
- ↑ T. Sadler: Medizinische Embryologie. 10. Auflage. Thieme Verlag, Stuttgart 2003, ISBN 3-13-446610-4, S. 25–44.
- ↑ C. M. Farquhar: Ectopic Pregnancy. In: Lancet. 366 (2005), S. 583, PMID 16099295
- ↑ A. K. Majhi, N. Roy, K. S. Karmakar, P. K. J. Banerjee: Ectopic pregnancy - an analysis of 180 cases. In: Indian Med Assoc. 105 (2007), S. 308, 310, 312 passim, PMID 18232175.
- ↑ BestBets: Risk Factors for Ectopic Pregnancy. Abgerufen am 2. Dezember 2011.
- ↑ G. Bogdanskiene, P. Berlingieri, J. G. Grudzinskas: Association between ectopic pregnancy and pelvic endometriosis. In: Int J Gynaecol Obstet. 92 (2006), S. 157–158, doi:10.1016/j.ijgo.2005.10.024
- ↑ R. A. Lyons, E. Saridogan, O. Djahanbakhch: The reproductive significance of human Fallopian tube cilia. In: Hum Reprod Update. Band 12, Nr. 4, 2006, S. 363–372, doi:10.1093/humupd/dml012, PMID 16565155.
- ↑ J. L. Shaw, S. K. Dey, H. O. Critchley, A. W. Horne: Current knowledge of the aetiology of human tubal ectopic pregnancy. Hum Reprod Update 16 (2010), S. 432–444, PMID 20071358, doi:10.1093/humupd/dmp057.
- ↑ J. I. Tay, J. Moore, J. J. Walker: Ectopic pregnancy. In: West J Med. Band 173, Nr. 2, 2000, S. 131–134, doi:10.1136/ewjm.173.2.131, PMID 10924442, PMC 1071024 (freier Volltext).
- ↑ a b c d e L. Speroff, R. H. Glass, N. G. Kase: Clinical Gynecological Endocrinology and Infertility. 6. Auflage. Lippincott Williams & Wilkins, 1999, ISBN 0-683-30379-1, S. 1149 ff.
- ↑ a b J. G. Schenker, E. J. Margalioth: Intra-uterine adhesions: an updated appraisal. In: Fertility and Sterility. Band 37, Nr. 5, 1982, S. 593–610., PMID 6281085.
- ↑ C. Klyszejko, J. Bogucki, D. Klyszejko, W. Ilnicki, S. Donotek, J. Kozma: Cervical pregnancy in Asherman’s syndrome [article in Polish]. In: Ginekol Pol. Band 58, Nr. 1, 1987, S. 46–48, PMID 3583040.
- ↑ D. Dicker, D. Feldberg, N. Samuel, J. A. Goldman: Etiology of cervical pregnancy. Association with abortion, pelvic pathology, IUDs and Asherman’s syndrome. In: J Reprod Med. Band 30, Nr. 1, 1985, S. 25–27, PMID 4038744.
- ↑ O. Bukulmez, H. Yarali, T. Gurgan: Total corporal synechiae due to tuberculosis carry a very poor prognosis following hysteroscopic synechialysis. In: Human Reproduction. Band 14, Nr. 8, 1999, S. 1960–1961, doi:10.1093/humrep/14.8.1960, PMID 10438408.
- ↑ M. Al-Azemi, B. Refaat, S. Amer, B. Ola, N. Chapman, W. Ledger: The expression of inducible nitric oxide synthase in the human fallopian tube during the menstrual cycle and in ectopic pregnancy. In: Fertil. Steril. Band 94, Nr. 3, Mai 2009, S. 833–840, doi:10.1016/j.fertnstert.2009.04.020, PMID 19482272.
- ↑ F. Plotti, A. Di Giovanni, C. Oliva, F. Battaglia, G. Plotti: Bilateral ovarian pregnancy after intrauterine insemination and controlled ovarian stimulation. In: Fertil Steril. 90 (2008), S. 2015, S. e3–e5, PMID 18394622, doi:10.1016/j.fertnstert.2008.02.117
- ↑ Spiegelberg-Kriterien auf whonamedit.com
- ↑ F. Lehmann, N. Baban, B. Harms, U. Gethmann, R. Krech: Ovargravidität nach Gametentransfer (GIFT) Ein Fallbericht. In: Geburtsh Frauenheilk. 51 (1991), S. 945–947, doi:10.1055/s-2008-1026242
- ↑ Diagnosis of ectopic pregnancy with ultrasound. In: Best Practice & Research Clinical Obstetrics & Gynaecology (= Acute Gynaecology Volume 1: Early Pregnancy Complications). Band 23, Nr. 4, August 2009, S. 501–508, doi:10.1016/j.bpobgyn.2008.12.010.
- ↑ H. K. Atrash, A. Friede, C. J. Hogue: Abdominal pregnancy in the United States: frequency and maternal mortality. Obstet Gynecol 69 (1987), S. 333–337.
- ↑ I. Delke, N. P. Veridiano, M. L. Tancer: Abdominal pregnancy: review of current management and addition of 10 cases. In: Obstet Gynecol. 60 (1982), S. 200–204.
- ↑ 'Special' baby grew outside womb. BBC news, 30. August 2005, abgerufen am 14. Juli 2006.
- ↑ Bowel baby born safely. BBC news, 9. März 2005, abgerufen am 10. November 2006.
- ↑ J. Zhang, F. Li, Q. Sheng: Full-term abdominal pregnancy: a case report and review of the literature. In: Gynecol. Obstet. Invest. Band 65, Nr. 2, 2008, S. 139–141, doi:10.1159/000110015, PMID 17957101.
- ↑ K. Talbot, R. Simpson, N. Price, S. R. Jackson: Heterotopic pregnancy. In: J Obstet Gynaecol. 31 (2011), S. 7–12, PMID 21280985
- ↑ Claude Henri Diesch: Heterotope Schwangerschaft – eine aktuelle Literaturübersicht. In: Speculum. 23 (2005), S. 17–21, kup.at (PDF; 285 kB)
- ↑ E. Kemmann, S. Trout, A. Garcia: Can we predict patients at risk for persistent ectopic pregnancy after laparoscopic salpingotomy? In: The Journal of the American Association of Gynecologic Laparoscopists. Band 1, Nr. 2, Februar 1994, S. 122–126, doi:10.1016/S1074-3804(05)80774-1, PMID 9050473.
- ↑ G. Tews, T. Ebner, K. Jesacher: Besonderheiten der ektopen Schwangerschaft. In: Journal für Reproduktionsmedizin und Endokrinologie. Nr. 1 (4), 2004, S. 268–271.
- ↑ eMedicine - Surgical Management of Ectopic Pregnancy: Article Excerpt by R Daniel Braun. Abgerufen am 17. September 2007.
- ↑ U. Mahboob, S. B. Mazhar: Management of ectopic pregnancy: a two-year study. In: Journal of Ayub Medical College, Abbottabad: JAMC. Band 18, Nr. 4, 2006, S. 34–37, PMID 17591007.
- ↑ L. Clark, S. Raymond, J. Stanger, G. Jackel: Treatment of ectopic pregnancy with intraamniotic methotrexate - a case report. In: The Australian & New Zealand journal of obstetrics & gynaecology. Band 29, Nr. 1, 1989, S. 84–85, doi:10.1111/j.1479-828X.1989.tb02888.x, PMID 2562613.
- ↑ Togas Tulandi, Seang Lin Tan: Advances in Reproductive Endocrinology and Infertility: Current Trends and Developments. Informa Healthcare, 2002, ISBN 0-8247-0844-X, S. 240.
- ↑ a b William W. Hurd, Tommaso Falcone: Clinical reproductive medicine and surgery. Mosby/Elsevier, St. Louis, Mo 2007, ISBN 978-0-323-03309-1, S. 724.
- ↑ Michael Böhme, Jürgen Nieder, Wolfgang Weise: Bauchhöhlenschwangerschaft am Termin mit lebendem Kind. In: Zentralbl Gynakol. 108 (1986), S. 516–519, PMID 3727853
- ↑ Registry Reports. (PDF) In: Volume XVI, Number 5. ARDMS The Ultrasound Choice, Ogden, Utah, Oktober 1999, archiviert vom (nicht mehr online verfügbar) am 23. Dezember 2010; abgerufen am 22. Juni 2011 (englisch). Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Miracle baby. Utah News from KSL-TV, Ogden, Utah, 5. August 1999, archiviert vom (nicht mehr online verfügbar) am 30. September 2011; abgerufen am 22. Juni 2011 (englisch). Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Doctors hail 'miracle' baby. In: BBC News. 10. September 2009, abgerufen am 2. Dezember 2011.
- ↑ Laura Collins: Miracle baby Billy grew outside his mother’s womb. In: Daily Mail, London. 31. August 2008, abgerufen am 3. September 2008.
- ↑ Baby Born After Rare Ovarian Pregnancy. Associated Press, 30. Mai 2008, archiviert vom am 3. Juni 2008; abgerufen am 5. September 2012.
- ↑ Rebekah Cavanagh: Miracle baby may be a world first. 30. Mai 2008, archiviert vom (nicht mehr online verfügbar) am 30. Mai 2008; abgerufen am 30. Mai 2008. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Amal A Dahab, Rahma Aburass, Wasima Shawkat, Reem Babgi, Ola Essa, Razaz H Mujallid: Full-term extrauterine abdominal pregnancy: a case report. In: J Med Case Reports. 5 (2011), S. 531, PMID 22040324, jmedicalcasereports.com (PDF; 753 kB).
- ↑ D. Nkusu Nunyalulendho, E. M. Einterz: Advanced abdominal pregnancy: case report and review of 163 cases reported since 1946. In: Rural Remote Health. 8 (2008), S. 1087, rrh.org.au
- ↑ Johannes Richter: Tiergeburtshilfe. Georg Thieme Verlag, 1993, ISBN 3-489-53416-6, S. 146.
- ↑ a b c d e f S. Lurie: The history of the diagnosis and treatment of ectopic pregnancy: a medical adventure. In: Eur J Obstet Gynecol Reprod Biol. 43 (1992), S. 1–7, PMID 1737602, elsevierhealth.com (PDF)
- ↑ Toby E. Huff: Intellectual Curiosity and the Scientific Revolution: A Global Perspective. Cambridge University Press, 2010, ISBN 978-0-521-17052-9, S. 196.
- ↑ Ectopic Pregnancy ( vom 26. Mai 2011 im Internet Archive)
- ↑ John Bard: A Case of Extra-Uterine Foetus. In: Medical Observations and Inquiries of the Society of Physicians of London. Vol. 2 (1764), S. 369–372.
- ↑ Ira M. Rutkow: The History of Surgery in the United States, 1775–1900: Periodicals and pamphlets. Norman Publishing, 1992, ISBN 0-930405-48-X, S. 89.
- ↑ John King: Analysis of the subject of extra-uterine foetation, and of the retroversion of the gravid uterus. Wright, Norwich 1818.
- ↑ Marc A. Fritz, Leon Speroff: Clinical Gynecologic Endocrinology and Infertility. Lippincott, Williams & Wilkins, 2010, ISBN 978-0-7817-7968-5, S. 1384.
- ↑ J. S. Parry, H. C. Lea: Extrauterine pregnancy. In: Am J Obstet Gynecol. 9 (1976), S. 169–170.
- ↑ Robert Lawson Tait: Five cases of extrauterine pregnancy operated upon at the time of rupture. Br Med J 1 (1884), S. 1250.
- ↑ Robert Lawson Tait: Pathology and treatment of extrauterine pregnancy. In: Br Med J. 2 (1884), S. 317.
- ↑ Robert Lawson Tait: Lectures on ectopic pregnancy. Birmingham 1888, S. 23, 25.
- ↑ Historie der Universitätsfrauenklinik Erlangen ( des vom 6. Dezember 2013 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Richard Frommel: Zur Therapie und Anatomie der Tubenschwangerschaft. In: Deutsch Arch Klin Med. 42 (1888), S. 91–102.
- ↑ P. Graffagnino: Ectopic pregnancy. In: Am J Obstet Gynecol 4. (1922), S. 148–158.
- ↑ C. G. Collins, W. D. Beacham, D. W. Beacham: Ectopic pregnancy, mortaiity and morbidity factors. In: Am J Obstet Gynecol. 57 (1949), S. 1144–1154.
- ↑ H. L. Riva, L. A. Kammeraad, P. S. Anderson: Ectopic pregnancy: report of 132 cases and comments on the role of the culdoscope in diagnosis. Obstet Gynecol 20 (1962), S. 189–198.
- ↑ D. O. Ott: Ventroscopic illumination of the abdominal cavity in pregnancy. In: Z Akus i Zhensk Bolez. 15 (1901), S. 7.
- ↑ Hans Christian Jacobaeus: Über die Möglichkeit die Zystoskopie bei Untersuchung seröser Höhlungen anzuwenden. Münch Med Wochenschr 57 (1910), S. 2090–2092.
- ↑ Hans Christian Jacobaeus: Kurze Übersicht über meine Erfahrungen mit der Laparoskopie. Münch Med Wochenschr 58 (1911), S. 2017.
- ↑ Hans Kalk: Erfahrungen mit der Laparoskopie (zugleich mit Beschreibung eines neuen Instrumentes). In: Z Klin Med. 111 (1929), S. 303.
- ↑ Hans Kalk, Egmont Wildhirt: Lehrbuch und Atlas der Laparoskopie und Leberpunktion. Thieme, Stuttgart 1962.
- ↑ Hans Frangenheim: Die Bedeutung der Laparoskopie für die gynäkologische Diagnostik. In: Fortschr Med. 76 (1958), S. 451–452.
- ↑ Hans Frangenheim: Die Laparoskopie und die Culdoskopie in der Gynäkologie. Thieme Verlag, Stuttgart, 1959.
- ↑ W. B. Stromme: Salpingostomy for tubal pregnancy: Report of a successful case. Obstet Gynecol 1 (1953), S. 472–475.
- ↑ H. I. Shapiro, D. H. Adler: Excision of an ectopic pregnancy through the laparoscope. In: Am J Obstet Gynecol. 117 (1973), S. 290–291, PMID 4269637.






