Lipoproteine

Lipoproteine (genauer Plasma-Lipoprotein-Partikel; früher auch Lipoproteide) sind nicht-kovalente Aggregate (Proteide) aus Lipiden und Proteinen, die mizellenähnliche Partikel mit einem unpolaren Kern aus Cholesterinestern und Triacylglyceriden sowie einer zur wässrigen Phase hin gerichteten Hülle mit polaren, hydrophilen Anteilen bilden, bestehend aus Protein, Phospholipiden und den Hydroxygruppen unveresterten Cholesterins.[1]
Funktion[Bearbeiten | Quelltext bearbeiten]
Plasma-Lipoprotein-Partikel dienen in allen Tierklassen dem Transport der wasserunlöslichen Lipide (Fette) sowie des Cholesterins und verschiedener Cholesterylester im Blut. Grundsätzlich beinhalten alle Partikel sowohl Triglyceride als auch Cholesterin und Cholesterylester, allerdings in ganz unterschiedlichen Mengen.
Plasma-Lipoprotein-Partikel werden in ganz bestimmten Zellen hergestellt, in das Blut abgegeben und haben eine Halbwertszeit von nur einigen Tagen. Sowohl ihre Hülle als auch ihr Inhalt sind anfällig für Oxidation durch Radikale und es gibt einige Hinweise, dass die oxidative Modifikation von Low Density Lipoprotein einen wichtigen Schritt in der Pathogenese der Arteriosklerose darstellt.[2]
Zur Abgabe bzw. Aufnahme des jeweils transportierten Stoffes docken sie mittels ihrer Apoproteine an spezifischen Rezeptor-Proteinen der Zielzellen an.
Klassifikation[Bearbeiten | Quelltext bearbeiten]
Lipoproteine werden, wie man anhand der englischen Bezeichnungen erkennen kann, größtenteils aufgrund ihrer physikalischen Dichte unterschieden, wobei sich deren Verschiedenheit im Wesentlichen aus dem unterschiedlichen Protein- und Lipidanteil des jeweiligen Lipoproteins ergibt. Eine Isolierung und Charakterisierung der verschiedenen Lipoproteine erfolgt dementsprechend traditionell über eine Dichtegradienten-Ultrazentrifugation, bei der sich eine Unterteilung in sechs Klassen mit zum Teil weiteren Unterklassen etabliert hat:
So gibt es zunächst die verhältnismäßig großen Chylomikronen, des Weiteren das VLDL und daraus entstehende temporäre IDL sowie LDL (alle drei auch als Betalipoproteine zusammengefasst), das Lipoprotein a und schließlich das inzwischen in 5 weitere Unterklassen unterteilte HDL (auch als Alphalipoprotein bezeichnet).
Die Isolierung des (im Fokus der Arteriosklerose-Forschung stehenden) humanen LDLs aus menschlichem Blutplasma ist durch Ultrazentrifugation (Zentrifugationsdauer: 2 Stunden; Rotor-Geschwindigkeit: 60.000 Umdrehungen/Minute) möglich und in den angeführten Literaturstellen detailliert beschrieben.[3][4]
Eine Trennung oder Charakterisierung von Lipoproteinen ist aber auch mit anderen Methoden, etwa mittels Elektrophorese möglich.
Nach Funktion[Bearbeiten | Quelltext bearbeiten]
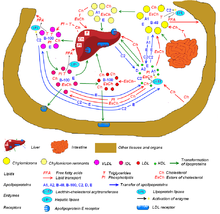
- Chylomikronen werden vermutlich ausschließlich in den Zellen der Darmwand gebildet. Ihre Funktion besteht hauptsächlich darin, Triglyceride aus dem Darm (bzw. der Darmwand) ins Blut und von dort zu den Leber-, Muskel- und Fettzellen zu transportieren.
- Very Low Density Lipoproteine (VLDL) werden ausschließlich in den Leberzellen gebildet und transportieren hauptsächlich (dort gespeicherte und neu synthetisierte) Triglyceride aus den Leberzellen zu den restlichen Körperzellen.
- Intermediate Density Lipoproteine (IDL) sind größenmäßig zwischen den VLDL und LDL liegende temporäre Abbauprodukte der VLDL, die deshalb normalerweise auch nicht im Blut nachweisbar sind.
- Lipoprotein a ist ein in seinem Aufbau große Ähnlichkeit zum LDL besitzender Bestandteil der Blutfette.[5]
- Low Density Lipoproteine (LDL) werden in den Leberzellen gebildet und transportieren hauptsächlich Cholesterin bzw. Cholesterylester aus der Leber zu den restlichen Zellen des Körpers. Man kann diese Klasse weiter in
- small dense LDL kleine dichte LDL-Partikel und
- large buoyant LDL große schwimmfähige LDL-Partikel aufteilen
- High Density Lipoproteine (HDL) werden ebenfalls in den Leberzellen gebildet, transportieren jedoch hauptsächlich Cholesterin aus den übrigen Zellen des Körpers zurück in die Leber, wobei sie außerdem in der Lage sind, sich an LDL-Partikel zu koppeln und einen Teil des in diesen Partikeln transportierten Cholesterins und Cholesterylesters zu übernehmen, aber auch Triglyceride mit ihnen austauschen können.
Nach Dichte[Bearbeiten | Quelltext bearbeiten]
In folgender Tabelle sind die Säuger-Lipoproteine mit einigen ihrer Unterformen aufgeführt:
| Lipoprotein | Durchmesser (nm) | Apolipoproteine | Konzentration bei Männern (g/l) |
Konzentration bei Frauen (g/l) |
|---|---|---|---|---|
| Chylomikronen | < 1000 | ApoB-48, ApoA-I & II, ApoC-II & III, ApoE | < 0,1 | < 0,1 |
| VLDL – Very Low Density Lipoprotein | 50 | ApoB-100, ApoC-II, ApoE | 0,5–2,0 | 0,5–1,5 |
| IDL – Intermediate Density Lipoprotein | 30 | ApoB-100, ApoC-II, ApoE | ||
| Lipoprotein a – Lp(a) | 25 | ApoB-100, Apo(a) | 0,01–0,5 | 0,01–0,5 |
| LDL – Low Density Lipoprotein | 21 | ApoB-100 | 2,0–3,5 | 2,0–3,0 |
| HDL – High Density Lipoprotein | ||||
| HDLE | 12 | ApoA-I & II | <0,05 | <0,05 |
| HDL1 | 10 | ApoA-I & II, C, E | 0,5–1,0 | 0,5–1,0 |
| HDL2 | 10 | ApoA-I & II, C, E | 0,5–1,0 | 0,5–1,0 |
| HDL3 | 8 | ApoA-I & II | 1,0–2,0 | 1,0–2,0 |
| VHDL – Very High Density Lipoprotein | 7 | 0,1–0,2 | 0,1–0,2 | |
Über die Nahrung zugeführtes Cholesterin sowie Triglyceride werden vom Intestinaltrakt aufgenommen und dann in Form von Chylomikronen auf dem Lymphweg über den Ductus thoracicus in venöses Blut abgegeben. Die nach Einwirkung von Lipasen und Abgabe der freigesetzten Fettsäuren in den peripheren Muskel- und Fettzellen verbleibenden so genannten Chylomikronen-Remnants (engl. Überbleibsel) werden schließlich von der Leber aufgenommen und zerlegt.
VLDL, so wie seine Metabolite IDL und vor allem LDL, transportieren vom Körper selbst synthetisiertes Cholesterin und die von den Chylomikronen übernommenen Triglyceride von der Leber zu den peripheren Geweben. HDL (genauer HDL3) nehmen Cholesterin unter Vermittlung des Enzyms Lecithin-Cholesterin-Acyltransferase (LCAT) aus den Geweben, aber auch von anderen Lipoproteinen auf und transportieren es zur Leber zurück (reverser Cholesterintransport). Das transportierte Cholesterin in den Lipoproteinen ist überwiegend mit Fettsäuren verestert.
Über 75 % des Kohlen- und des Wasserstoffes in energieliefernden Substraten im Stoffwechsel sind Lipidbestandteile.
Die Transportproteine werden als Apolipoproteine (ApoLp) bezeichnet. Sie geben den Lipidmizellen Stabilität und bestimmen im Stoffwechsel der Lipidoproteine die Umsatzgeschwindigkeit und dirigieren sie zu bestimmten Zielorganen.
Fettstoffwechselstörungen lassen sich über Lipoproteine im Blut nachweisen. Das sogenannte Lipoprotein a (Lp(a), gesprochen: Lipoprotein klein „a“) gilt als Risikofaktor, da es mit dem Auftreten von Herzinfarkten korreliert.
Zur qualitativen und quantitativen Bestimmung der Lipidanteile der Lipoproteine werden chromatographische Verfahren wie z. B. die Dünnschichtchromatographie und die Gaschromatographie auch in Kopplung mit der Massenspektrometrie eingesetzt.[6][7][8]
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Historische Literatur[Bearbeiten | Quelltext bearbeiten]
- Fritz A. Pezold (Hrsg.): Lipide und Lipoproteide im Blutplasma. Biochemie, Pathophysiologie, Klinik. Springer-Verlag, Berlin/Heidelberg / New York 1961.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Hans-Dieter Jakubke, Hans Jeschkeit: Aminosäuren, Peptide, Proteine, Verlag Chemie, Weinheim, S. 388, 1982, ISBN 3-527-25892-2.
- ↑ D. Steinberg, S. Parthasarathy, T. E. Carew, J. C. Khoo, J. L. Witztum: Beyond Cholesterol. Modifications of low-density lipoprotein that increase its atherogenicity. In: New England Journal of Medicine. Band 320, Nr. 14, 1989, S. 915–924, doi:10.1056/NEJM198904063201407, PMID 2648148.
- ↑ Andreas Giessauf, Ernst Steiner, Hermann Esterbauer: Early destruction of tryptophan residues of apolipoprotein B is a vitamin E-independent process during copper-mediated oxidation of LDL. In: Biochimica et Biophysica Acta – Lipids and Lipid Metabolism. Band 1256, Nr. 2, 1995, S. 221–232, doi:10.1016/0005-2760(95)00024-7.
- ↑ Gieseg S.P. and Waeg G. (1994) Beckman Report 37, issue 77, S. 6
- ↑ Blutfette und Erhöhte Blutfettwerte–Überblick. Abgerufen am 19. Juni 2017.
- ↑ B. Rehlender: Qualitative und quantitative Bestimmung von Lipidfraktionen verschiedener ernährungsphysiologisch relevanter Lipoproteine aus Humanseren, Analysen von Extrelut-Lipid-Extrakten durch kombinierten Einsatz von Dünnschichtchromatographie, Gaschromatographie und Massenspektrometrie, Dissertation TU Berlin, 1983 DNB 840626266
- ↑ Lizenko MV, Regerand TI, Bakhirev AM, Petrovskiĭ VI, Lizenko EI: Content of the main lipid components in blood serum lipoproteins of human and of various animal species] Zh Evol Biokhim Fiziol. 2007 Mar-Apr;43(2):155-61. Russian. PMID 17674708
- ↑ Ooi EM, Watts GF, Barrett PH, Chan DC, Clifton PM, Ji J, Nestel PJ: Dietary plant sterols supplementation does not alter lipoprotein kinetics in men with the metabolic syndrome. Asia Pac J Clin Nutr. 2007;16(4):624-31.PMID 18042521