Zimtsäureethylester
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Allgemeines | ||||||||||
| Name | Zimtsäureethylester | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C11H12O2 | |||||||||
| Kurzbeschreibung |
farblose Flüssigkeit [1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 176,21 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig | |||||||||
| Dichte |
1,05 g·cm−3 (20 °C)[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt | ||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[4] | |||||||||
| Brechungsindex |
1,558[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||
Zimtsäureethylester ist eine farblose Flüssigkeit, gehört zu den Aromaten und ist ein ungesättigter Carbonsäureester mit einer trans-substituierten Kohlenstoff-Kohlenstoff-Doppelbindung in der Seitenkette. Der isomere cis-Zimtsäureethylester hat nur eine geringe Bedeutung. Die Angaben in diesem Artikel beziehen sich nur auf den trans-Zimtsäureethylester.
Vorkommen
Zimtsäureethylester kommt als Aromastoff im Wein vor.
Darstellung
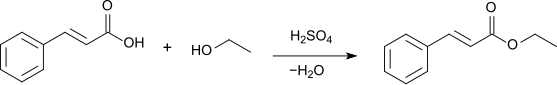
Zimtsäureethylester kann durch Veresterung von Zimtsäure mit Ethanol gewonnen werden, in Gegenwart von Schwefelsäure[5] oder Salzsäure.[6]
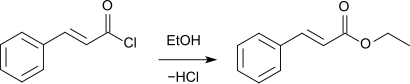
Ein weiterer Weg ist die Reaktion von Zimtsäure mit Thionylchlorid (dabei entsteht intermediär Zimtsäurechlorid) und Ethanol.[7]
Ebenso ist es möglich, Zimtsäureethylester durch eine Claisen-Kondensation aus Benzaldehyd und Ethylacetat herzustellen.[8][5]
Reaktionen
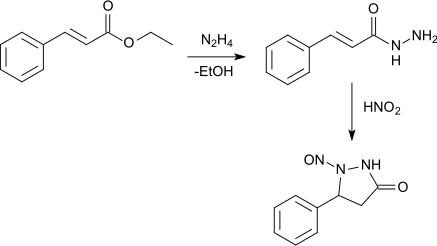
Mit Hydrazinhydrat reagiert Zimtsäureethylester zu Zimtsäurehydrazid. Dieses bildet mit Salpetriger Säure durch eine Ringschlußreaktion 1-Nitroso-5-phenyl-3-pyrazolidon.[9]
Einzelnachweise
- ↑ D. Martinetz und R. Hartwig, Taschenbuch der Riechstoffe, 1. Auflage, Verlag Harri Deutsch, Thun und Frankfurt/Main 1998 ISBN 3-8171-1539-3
- ↑ a b c d e f Datenblatt Ethyl cinnamate bei Sigma-Aldrich (PDF).
- ↑ a b Datenblatt Zimtsäureethylester bei Alfa Aesar (Seite nicht mehr abrufbar).
- ↑ Eintrag zu Zimtsäureethylester bei ChemBlink
- ↑ a b C. S. Marvel, W. B. King: Ethyl Cinnamate In: Organic Syntheses. 9, 1929, S. 38, doi:10.15227/orgsyn.009.0038; Coll. Vol. 1, 1941, S. 252 (PDF).
- ↑ E. Fischer, A. Speier: "Darstellung der Ester" in Berichte der deutschen chemischen Gesellschaft, 1895, 28, S. 3252ff. (Volltext).
- ↑ Autorengemeinschaft: Organikum, 15. Auflage, VEB Deutscher Verlag der Wissenschaften, Berlin 1976, S. 527.
- ↑ L. Claisen: "Zur Darstellung der Zimmtsäure und ihrer Homologen" in Berichte der deutschen chemischen Gesellschaft, 1890, 23, S. 976ff. (Volltext).
- ↑ T. Curtius, P. A. Bleicher: "Über das Hydrazid der m-Nitrozimtsäure und sein Verhalten gegen Salpetrigsäure" in Journal für Praktische Chemie, 1924, 107 (1-4), S. 86–98 (doi:10.1002/prac.19241070106).