Acridingelb
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
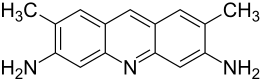
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Acridingelb | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C15H15N3 | ||||||||||||||||||
| Kurzbeschreibung |
Braun-rotes kristallines Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 237,3 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Acridingelb ist ein Acridin-Farbstoff, der in der Molekularbiologie als Fluoreszenzfarbstoff eingesetzt wird. Als mutagenes Klastogen ist es ein Gift, welches Chromosomenaberrationen hervorrufen kann und somit als Karzinogen wirkt.[3][4]
Absorptions- und Emissionsspektrum von Acridingelb in Ethanol[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Datenblatt Acridine Yellow bei Fisher Scientific, abgerufen am 13. Februar 2014 (PDF).
- ↑ a b Datenblatt Acridingelb Dye bei Sigma-Aldrich, abgerufen am 23. Februar 2022 (PDF).
- ↑ Oyeronke A. Odunola, Aliyu Muhammad, Ahsana D. Farooq, Kourosh Dalvandi, Huma Rasheed, Muhammad I. Choudhary, Ochuko L. Erukainure: Comparative assessment of redox-sensitive biomarkers due to acacia honey and sodium arsenite administration in vivo. In: Mediterranean Journal of Nutrition and Metabolism 6, Nr. 2, 2013, S. 119–126, doi:10.1007/s12349-013-0127-1.
- ↑ Erich Gebhart, Ruben M. Arutyunyan: Principles of clastogenic action and its estimation. In: Anticlastogens in Mammalian and Human Cells. Springer Berlin Heidelberg, 1991, S. 7–30.
- ↑ Masahiko Taniguchi, Hai Du, Jonathan S. Lindsey: PhotochemCAD 3: Diverse Modules for Photophysical Calculations with Multiple Spectral Databases. In: Photochemistry and Photobiology. Band 94, Nr. 2, März 2018, S. 277, doi:10.1111/php.12862.
Kategorien:
- Gesundheitsschädlicher Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Hautkontakt
- Gesundheitsschädlicher Stoff bei Einatmen
- Hautreizender Stoff
- Augenreizender Stoff
- Atemwegsreizender Stoff
- Stoff mit Verdacht auf krebserzeugende Wirkung
- Acridin
- Aminoaromat
- Alkylsubstituierter Aromat
- Fluoreszenzfarbstoff

