Achondroplasie
| Klassifikation nach ICD-10 | |
|---|---|
| Q77 | Osteochondrodysplasie mit Wachstumsstörungen der Röhrenknochen und der Wirbelsäule |
| Q77.4 | Achondroplasie |
| ICD-10 online (WHO-Version 2019) | |
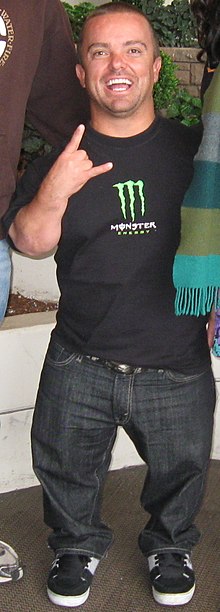
Die Achondroplasie ist die häufigste Form des genetisch bedingten Kleinwuchses. Betroffene fallen vor allem durch stark verkürzte Arme und Beine und einen großen Kopf auf.
Bezeichnung[Bearbeiten | Quelltext bearbeiten]
Im Jahre 1878 wurde der Begriff Achondrodysplasie durch den französischen Arzt Joseph Marie Jules Parrot geprägt.[1]
Die Bezeichnung Achondroplasie (wörtlich: fehlende Knorpelbildung) ist rein historisch bedingt und erklärt weder die Ursache noch die Erscheinungen dieser Störung.[2]
Weitere Bezeichnungen, die jedoch veraltet und nicht mehr gebräuchlich sind, sind Chondrodystrophie, Chondrodystrophia fetalis (oder foetalis), Parrot-Syndrom oder Kaufmann-Syndrom (unter Referenz auf den deutschen Pathologen Eduard Kaufmann).[3][2]
Häufigkeit[Bearbeiten | Quelltext bearbeiten]
Achondroplasie ist die häufigste Form des genetisch bedingten Kleinwuchses. Sie tritt mit einer Inzidenz von 1 auf 20.000 Geburten auf.[4] Damit gehört sie, wie alle Arten von Kleinwuchs, zu den Seltenen Krankheiten.
Ursache[Bearbeiten | Quelltext bearbeiten]
Die Achondroplasie ist das Resultat einer Punktmutation im Fibroblasten-Wachstumsfaktor-Rezeptor-Gen FGFR-3 (englisch: Fibroblast Growth Factor Receptor 3). Diese Mutation führt zu einer Störung der Knorpelbildung; die Knochenwachstumszone (Epiphysenfuge) wird verfrüht verknöchert, was zur Einschränkung des Längenwachstums vor allem der Arme und Beine (Extremitäten) führt (enchondrale Ossifikation). Dadurch entsteht ein dysproportionaler Kleinwuchs, bei dem Rumpf und Kopf relativ länger als die Extremitäten sind.
In 96 % der Fälle liegt eine G(1138)A-Punktmutation im FGFR-3-Gen vor. Dadurch kommt es zu einem Aminosäureaustausch in Position 380 des Proteins, aus Glycin wird Arginin (Gly380Arg). In 3 % der Fälle lässt sich eine G(1138)C-Punktmutation nachweisen, welche ebenfalls einen Glycin-zu-Arginin-Austausch zur Folge hat.
Die Achondroplasie wird autosomal-dominant vererbt, das heißt, sie kann nur von selbst Betroffenen weitervererbt werden. Dies ist bei etwa 20 % der mit Achondroplasie geborenen Kindern der Fall. Bei den restlichen circa 80 % liegt eine Neumutation des FGFR3-Gens vor; der Kleinwuchs entsteht also unabhängig von der Größe der Eltern. Embryos mit homozygoter Mutation (sowohl die väterliche als auch die mütterliche Variante des Gens sind verändert) sind nicht lebensfähig und sterben kurz nach der Geburt oder bereits im Mutterleib (Thanatophore Dysplasie).
Allgemeine Symptome der Mutation[Bearbeiten | Quelltext bearbeiten]
Die Achondroplasie führt zu einem disproportionierten Kleinwuchs. Da die unübliche Knorpelbildung insbesondere in den Röhrenknochen eine regelgerechte Entwicklung nicht möglich werden lässt, sind stark verkürzte Extremitäten bei normaler Rumpfgröße charakteristisch. Das Längenwachstum ist bei dagegen nahezu normalem Dickenwachstum gestört.
Weitere Symptome bei betroffenen Menschen sind:
- vergleichsweise kurze Finger
- vergrößerter Abstand zwischen dem 3. und 4. Finger („Dreizackhand“)
- vergleichsweise kurzer Hals und großer Kopf mit vorgewölbter Stirn und unüblicher Schädelbasis
- schmales Gesicht mit Sattelnase
- häufig Hohlkreuz (Hyperlordose) oder eine Kyphose
- angeborene Enge des Hinterhauptslochs und des gesamten Wirbelkanals (Spinalkanalstenose)
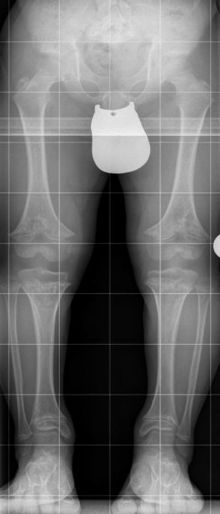
- häufig O-Beine oder X-Beine
- häufige Mittelohrentzündungen (aufgrund verengter Eustachi-Röhre)
- charakteristische Hautfalten (die Haut ist für die verkürzten Extremitäten zu weit)
Aufgrund ihres relativ langen Rumpfes haben von Achondroplasie betroffene Menschen eine fast normale Sitzhöhe. Ausgewachsen erreichen sie eine Körpergröße zwischen 120 und 148 cm.
Diagnose und Differentialdiagnose[Bearbeiten | Quelltext bearbeiten]
Klinisch zur Abgrenzung gegenüber Hypochondroplasie und Pseudoachondroplasie sind wichtige Aspekte der große Kopf (Megalenzephalie) mit Balkonstirn und flacher Nase, Prognathie.
Radiologische Kriterien sind:
- Verbreiterte Metaphysen bei normalen Epiphysen
- Überproportional verkürzter Humerus und Femur
- Schmales Kreuzbein, breite Beckenschaufel mit horizontalem und breitem Pfannendach
- Verschmälerter Abstand der Bogenwurzeln nach kaudal zunehmend, verkürzte Pedikel mit eventueller Spinalstenose, keilförmige Deformierung der Wirbelkörper
- Brachydaktylie mit Dreizackhand[5]
Therapie[Bearbeiten | Quelltext bearbeiten]
Die Therapie orientiert sich an den Symptomen. Bei funktionellen Behinderungen durch die Beinachsen- und Wirbelsäulenstellung sowie bei beginnenden Lähmungen können dekomprimierende und stabilisierende Eingriffe an der Wirbelsäule vorgenommen werden.
Derzeit befinden sich zwei Wirkstoffe in klinischen Studien zur Behandlung von Achondroplasie. Die Firma BioMarin Pharmaceutical Inc. entwickelt ein CNP-Analogon (benannt Vosoritid), welches in die Wirkkaskade des FGFR3-Rezeptors eingreift und eine erhöhte Teilungsrate der Knorpelzellen zur Folge hat.[6] Die Firma BioClin Therapeutics, Inc. entwickelt einen FGFR3-Antikörper sowohl zur Behandlung von Blasenkrebs als auch zur Anwendung bei Achondroplasie.[7][8]
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Literatur[Bearbeiten | Quelltext bearbeiten]
- W. Schuster, D. Färber (Hrsg.): Kinderradiologie. Bildgebende Diagnostik. Springer, 1996, ISBN 3-540-60224-0.
- J. W. Spranger: Bone Dysplasias. Urban & Fischer, 2002, ISBN 3-437-21430-6.
Einzelbelege[Bearbeiten | Quelltext bearbeiten]
- ↑ J. M. Parrot: Les malformations achondrodysplasiques. In: Bulletins de la Société d’anthropologie de Paris, 1878.
- ↑ a b Spranger, Menger, Meinecke, Zabel: Achondroplasie. In: BKMF (Hrsg.): Kleinwuchs - Gelbe Blätter. 1a. Bremen März 2007, S. 2.
- ↑ E. Kaufmann: Untersuchungen über die sogenannte foetale Rachitis (Chondrodystrophia foetalis). Berlin, Reimer, 1892.
- ↑ Bernhard Zabel: FGFR3-Mutationen als Ursache von Skelettdysplasien der Achondroplasie-Gruppe. In: Klaus Mohnike u. a.: Achondroplasie und Hypochondroplasie. 2. Auflage. ABW Wissenschaftsverlag, 2013, ISBN 978-3-940615-41-1, S. 3.
- ↑ F. Hefti: Kinderorthopädie in der Praxis. Springer, 1998, ISBN 3-540-61480-X, S. 651.
- ↑ BioMarin Pharmaceutical BMN-111 phase-II results | Biotechnology Events. In: www.biotechnologyevents.com. Archiviert vom am 13. April 2016; abgerufen am 20. April 2016.
- ↑ BioClin Therapeutics, Inc.: BioClin Therapeutics Initiates Phase 2 Clinical Trial Evaluating B-701 for Treatment of Urothelial Cell Carcinoma. In: www.prnewswire.com. Archiviert vom am 20. April 2016; abgerufen am 20. April 2016.
- ↑ Science | BioClin Therapeutics. In: www.bioclintherapeutics.com. Archiviert vom am 12. Mai 2016; abgerufen am 20. April 2016.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Achondroplasie. In: Online Mendelian Inheritance in Man. (englisch)