Zinn(IV)-iodid
Zur Navigation springen
Zur Suche springen
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
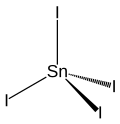
| |||||||||||||||||||
| Keile zur Verdeutlichung der räumlichen Struktur | |||||||||||||||||||
| Raumgruppe |
Pa3 (Nr. 205) | ||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Zinn(IV)-iodid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | SnI4 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 626,328 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
364,5 °C[2] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
2,106[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Zinn(IV)-iodid ist eine anorganische chemische Verbindung des Zinns aus der Gruppe der Iodide.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Zinn(IV)-iodid kann durch direkte Synthese aus den Elementen oder durch Erhitzen einer Zinn(II)-chlorid-Lösung mit Iod gewonnen werden.[1]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
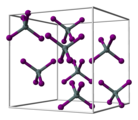
Zinn(IV)-iodid ist ein oranger Feststoff, der in Wasser hydrolysiert.[5] Es besitzt eine kubische Kristallstruktur mit der Raumgruppe Pa3 (Raumgruppen-Nr. 205), dem Gitterparameter a = 1226 pm und acht Formeleinheiten pro Elementarzelle.[6] Dies entspricht ungefähr einer kubisch-dichtesten Kugelpackung von Iod-Atomen, in der 1/8 aller tetraedrischen Lücken mit Zinn-Atomen besetzt sind. Dies führt zu diskreten tetraedrischen SnI4-Molekülen.[7]
-
Zinn(IV)-iodid
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Moeller, T., Edwards, D. C., Brandt, R. L. and Kleinberg, J.: Tin(IV) Iodide (Stannic Iodide). In: Inorganic Syntheses. 4. Jahrgang, 1953, S. 119–121, doi:10.1002/9780470132357.ch40.(eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ a b c d Datenblatt Tin(IV) iodide (PDF) bei Strem, abgerufen am 25. Dezember 2012.
- ↑ a b c Datenblatt Tin(IV) iodide, anhydrous, powder, 99.999% trace metals basis bei Sigma-Aldrich, abgerufen am 4. Mai 2022 (PDF).
- ↑ D'Ans-Lax, Taschenbuch für Chemiker und Physiker. Bd. 3 (1998) ISBN 3-540-60035-3, S. 740.
- ↑ Hickling, G. G.: Gravimetric analysis: The synthesis of tin iodide. In: J. Chem. Educ. 67. Jahrgang, Nr. 8, 1990, S. 702–703, doi:10.1021/ed067p702.
- ↑ F. Meller and I. Fankuchen: The crystal structure of tin tetraiodide. In: Acta Crystallographica. 8. Jahrgang, 1955, S. 343–344, doi:10.1107/S0365110X55001035.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 970.