1,1,1-Trichlorethan
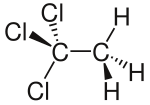
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Keilstrichformel zur Verdeutlichung der Geometrie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,1,1-Trichlorethan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C2H3Cl3 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit etherischem, chloroformähnlichem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 133,42 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,34 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
74 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
schwer in Wasser (1 g·l−1 bei 25 °C)[2] | ||||||||||||||||||
| Brechungsindex |
1,4366[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Treibhauspotential |
193 (bezogen auf 100 Jahre)[6] | ||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
1,1,1-Trichlorethan (veralteter Trivialname Methylchloroform) gehört zur Familie der Chlorkohlenwasserstoffe. Es ist isomer zu 1,1,2-Trichlorethan.
Herstellung[Bearbeiten | Quelltext bearbeiten]
Die Chemikalie wird durch Chlorierung von 1,1-Dichlorethan hergestellt oder durch Addition von Chlorwasserstoff an 1,1-Dichlorethen.[8][9]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
1,1,1-Trichlorethan ist eine farblose Flüssigkeit mit typischem etherischem Geruch (vergleichbar dem Geruch von Chloroform). Sie ist kaum mischbar mit Wasser, also hydrophob und lipophil und ihre Dämpfe sind schwerer als Luft. Wie andere Chlorkohlenwasserstoffe auch, ist es instabil gegenüber Licht, Luft und besonders Feuchtigkeit. Die Stabilisierung erfolgt durch Zugabe von bis 6 % Dioxan oder 2-Butanol bereits bei der Herstellung. Mit Alkali, Erdalkali und anderen Metallpulvern reagiert es explosionsartig. Mangelhaft stabilisiertes 1,1,1-Trichlorethan greift Aluminium an, dabei ist eine explosionsartige Reaktion mit gleichzeitig anwesenden Aromaten möglich.[8]
Sicherheitstechnische Kenngrößen[Bearbeiten | Quelltext bearbeiten]
1,1,1-Trichlorethan bildet entzündliche Dampf-Luft-Gemische. Der Explosionsbereich liegt zwischen 9,5 Vol.‑% (529 g/m3) als unterer Explosionsgrenze (UEG) und 15,5 Vol.‑% (860 g/m3) als oberer Explosionsgrenze (OEG).[2] Mit einer Mindestzündenergie von 4800 mJ ist die Verbindung nur schwer entzündbar.[2] Die Zündtemperatur beträgt 490 °C.[2] Der Stoff fällt somit in die Temperaturklasse T1.
Verwendung[Bearbeiten | Quelltext bearbeiten]
1,1,1-Trichlorethan ist ein Ausgangsstoff für die Synthese polychlorierter organischer Verbindungen durch Additionsreaktionen mit ungesättigten Verbindungen.
Es wurde als Lösemittel in Farben, Klebstoffen, Schneidölen und zur Reinigung von metallischen Werkstücken, Glas, optischen Geräten und Maschinen in der Textilindustrie verwendet. Auch in Korrekturflüssigkeiten kann es enthalten sein. Tipp-Ex enthält 1,1,1-Trichlorethan als Lösungsmittel, wegen der möglichen Gesundheitsgefährdung existiert jedoch auch eine wasserbasierte Variante. Im Zuge der Erkennung der Ozonloch-Problematik hat sich seine Bedeutung als Lösungsmittel verringert.[8]
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Trotz der geringeren Toxizität als Tetrachlormethan wirken die Dämpfe schleimhautreizend. Leber- und Nierenschäden sind durch Aufnahme in den Körper möglich. Gasförmig aufgenommenes Trichlorethan wird fast vollständig wieder durch die Atemluft ausgeschieden, ein kleiner Teil wird im Körper zu Trichloressigsäure und Trichlorethanol metabolisiert (verstoffwechselt). Bei Einhaltung des MAK-Wertes ist eine Fruchtschädigung sehr unwahrscheinlich. Wie viele Lösungsmittel wirkt es auf die Haut in einem schädigenden Ausmaß entfettend. Es kann die Atemwege, Verdauungswege und die Augen reizen. Schwindel, Kopfschmerzen, Benommenheit bis zur Bewusstlosigkeit und andere Hirnfunktionsstörungen können auftreten.
Die durch photochemische Prozesse in der Stratosphäre freigesetzten Chloratome können die Ozonschicht schädigen.[8]
Gesetzliche Regelungen[Bearbeiten | Quelltext bearbeiten]
Zum Schutz der Ozonschicht wurden in der EU Produktion und Inverkehrbringen von 1,1,1-Trichlorethan zum 1. Oktober 2000 durch die Verordnung (EG) Nr. 2037/2000 verboten.[10]
Über den Safe Drinking Water and Toxic Enforcement Act of 1986 besteht in Kalifornien seit dem 21. April 2023 eine Kennzeichnungspflicht für Produkte die 1,1,1-Trichlorethan enthalten.[11]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu TRICHLOROETHANE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- ↑ a b c d e f g h i j k l m n o Eintrag zu 1,1,1-Trichlorethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 5. Mai 2018. (JavaScript erforderlich)
- ↑ Datenblatt 1,1,1-Trichlorethan bei Sigma-Aldrich, abgerufen am 5. März 2011 (PDF).
- ↑ Eintrag zu 1,1,1-trichloroethane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 71-55-6 bzw. 1,1,1-Trichlorethan), abgerufen am 14. Mai 2020.
- ↑ G. Myhre, D. Shindell et al.: Climate Change 2013: The Physical Science Basis. Working Group I contribution to the IPCC Fifth Assessment Report. Hrsg.: Intergovernmental Panel on Climate Change. 2013, Chapter 8: Anthropogenic and Natural Radiative Forcing, S. 24–39; Table 8.SM.16 (ipcc.ch [PDF; 15,5 MB]).
- ↑ a b W. M. Haynes (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-39.
- ↑ a b c d Eintrag zu Trichlorethane. In: Römpp Online. Georg Thieme Verlag, abgerufen am 23. Juli 2015.
- ↑ Franz von Bruchhausen: Hagers Handbuch der Pharmazeutischen Praxis. Springer-Verlag, 1930, ISBN 3-540-52688-9, S. 1039 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Verordnung (EG) Nr. 2037/2000 des europäischen Parlaments und des Rates vom 29. Juni 2000 über Stoffe, die zum Abbau der Ozonschicht führen
- ↑ 1,1,1-Trichloroethane. OEHHA, 21. April 2023, abgerufen am 24. April 2023 (englisch).
