1,3-Propandiol
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
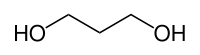
| ||||||||||
| Allgemeines | ||||||||||
| Name | 1,3-Propandiol | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C3H8O2 | |||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 76,10 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig | |||||||||
| Dichte |
1,05 g·cm−3 (20 °C)[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
213 °C[1] | |||||||||
| Dampfdruck | ||||||||||
| Löslichkeit |
mäßig in Wasser (100 g·l−1 bei 20 °C)[1] | |||||||||
| Brechungsindex |
1,4383[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||
1,3-Propandiol (PDO) ist eine chemische Verbindung. Sie besteht aus dem Grundgerüst des Propans, an dessen terminalen Positionen sich jeweils eine Hydroxylgruppe befindet. 1,3-Propandiol gehört zur Gruppe der zweiwertigen Alkohole, der Diole.
Herstellung
1,3-Propandiol ist über eine Vielzahl von Möglichkeiten synthetisch zugänglich. Eine Möglichkeit besteht in der Hydratisierung von Acrolein mit verdünnter Schwefelsäure in Gegenwart von Hydrochinon (verhindert die Polymerisation des Acroleins) und anschließender Hydrierung mit Raney-Nickel als Katalysator.[3]
Eine biochemische Synthese kann durch die Vergärung von Glycerin durch Bakterien der Gattung Citrobacter und Aerobacter bewerkstelligt werden.[3]
Eigenschaften
Es handelt sich um eine farblose Flüssigkeit mit nur schwachem Eigengeruch, die bei 213 °C siedet.
Verwendung
1,3-Propandiol kann zur Einführung von Schutzgruppen an Aldehyden und Ketonen genutzt werden.[4] Aus der eingesetzten Carbonylverbindung wird so ein Derivat von 1,3-Dioxan, ein Acetal beziehungsweise Ketal, gebildet. Dieses ist stabil gegenüber basischen Bedingungen und kann wenn sie nicht mehr benötigt wird durch Einwirkung von Brønsted- oder Lewis-Säuren in Anwesenheit von Wasser wieder gespalten werden.
Auch die Synthese von 1,3-Dioxan selbst gelingt durch Umsetzung von 1,3-Propandiol mit Formaldehyd und Phosphorsäure.[5] Diese Reaktion kann auch unter Verwendung von Salzsäure und Urotropin durchgeführt werden.[6]
Einzelnachweise
- ↑ a b c d e f g Eintrag zu CAS-Nr. 504-63-2 in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ M. Bergmann, A. Miekeley, E. v. Lippmann: Zur Chemie assoziierender Lactolide: Über Umwandlungen der Aldole, in: Chem. Ber., 1929, 62, S. 1467–1474; doi:10.1002/cber.19290620616.
- ↑ a b C. H. Werkman, G. F. Gillen: Bacteria Producing Trimethylene Glycol, in: J. Bacteriol., 1932, 23, S. 167–182.
- ↑ E. J. Salmi: Untersuchungen über ätherartige Verbindungen, I. Mitteil.: Zur Darstellung der Acetale und Ketale, in: Chem. Ber., 1938, 71, S. 1803–1808; doi:10.1002/cber.19380710905.
- ↑ R. Leutner: Zur Hydrolysegeschwindigkeit zyklischer Azetale, in: Monatsh. Chem., 1932, 60, S. 317–352; doi:10.1007/BF01538573
- ↑ US-Patent ICI, US 2021680, 1930.
