Hydrochinon
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Hydrochinon | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C6H6O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser, kristalliner Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 110,11 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
286 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| pKS-Wert | ||||||||||||||||||||||
| Löslichkeit |
löslich in Wasser: 72 g·l−1 (20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK |
| |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Hydrochinon (1,4-Dihydroxybenzol) ist ein Phenol und neben Brenzcatechin (1,2-Dihydroxybenzol) und Resorcin (1,3-Dihydroxybenzol) das dritte mögliche Dihydroxybenzol. Hier befinden sich die beiden Hydroxygruppen in der para-Stellung.
Entdeckung[Bearbeiten | Quelltext bearbeiten]
Friedrich Wöhler erhielt 1844 bei der trockenen Destillation (> 280 °C) der Chinasäure ein Produktgemisch, das neben Benzol, Benzoesäure und Salicylsäure als Hauptbestandteil eine neue farblose Verbindung enthielt. Nach Lösen des Destillats in Wasser, Abfiltrieren der unlöslichen Anteile und Abdestillieren der leichter flüchtigen Komponenten, kristallisierte er aus der zurückbleibenden Lösung zunächst Benzoesäure und aus deren Mutterlauge letztendlich Hydrochinon aus, das er durch wiederholte Umkristallisation in Form von farblosen, sechsseitigen Prismen rein erhielt.[9]
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Hydrochinon kommt als ca. 10%ige Lösung zusammen mit 28%igem Wasserstoffperoxid in Abwehrdrüsen der Bombardierkäfer vor. Im Verteidigungsfall wird dem Gemisch Katalase zugemischt und dem Angreifer als 100 °C heißes, ätzendes Abwehrmittel entgegengespritzt.[10][11][12] Die Blätter der Bärentraube wie auch Birnen enthalten das Glycosid Arbutin, bei dem es sich um Hydrochinon-β-D-Glucosid, also eine Verbindung von Hydrochinon mit Glucose handelt. Doppelfüßer aus der Ordnung Spirobolida können aus seitlich am Körper angelegten Drüsen Wehrsekrete ausstoßen, die teilweise Hydrochinon enthalten.
Darstellung[Bearbeiten | Quelltext bearbeiten]
Hydrochinon kann durch die Elbs-Oxidation aus Phenol synthetisiert werden.[13]
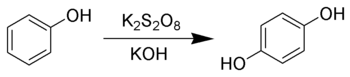
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Hydrochinon ist ein farbloser Feststoff, der in vier polymorphen Kristallformen auftreten kann. Unter Normaldruck existieren die α-, β- und γ-Form.[14][15] Die α- und β-Form kristallisieren in einem hexagonalen Kristallgitter,[3][4] die γ-Form in einem monoklinen Gitter.[15][5] Bei Raumtemperatur ist die α-Form die thermodynamisch stabile Form.[16] Die β- und γ-Form sind metastabil und können sich spontan in die α-Form umwandeln.[16] Der α-Form entspricht das kommerzielle Produkt. Die β-Form kann aus Clathraten mit kleinen Molekülen wie Methanol erhalten werden.[17][18][19][4] Die γ-Form kann über eine Sublimation[15] oder schnelle Verdampfung[5] gewonnen werden. Bei höheren Drücken oberhalb von 40 MPa kann die δ-Form als vierte Kristallform nachgewiesen werden.[16] Der Schmelzpunkt der δ-Form liegt bei 78,5 MPa bei 191 °C.[16] Der Tripelpunkt zwischen α-, δ- und flüssiger Phase liegt bei 176 °C und 15,7 MPa.[16]
Hydrochinon ist ein stärkeres Reduktionsmittel als Brenzcatechin, da das aus Brenzcatechin entstehende o-Benzochinon energiereicher und somit ein stärkeres Oxidationsmittel ist. Ursache für Letzteres ist die elektrostatische Abstoßung der benachbarten Carbonylgruppen.
Es lässt sich durch Oxidation in Benzochinon (Chinon) überführen:

Bei dieser Reaktion entsteht als Zwischenprodukt der tieffarbige, schwer wasserlösliche Charge-Transfer-Komplex Chinhydron (nicht abgebildet).
Reaktionen[Bearbeiten | Quelltext bearbeiten]
Die einfache Bromierung von Hydrochinon mit Kaliumbromid und Brom in Tetrachlorkohlenstoff führt zum Bromhydrochinon.[20]
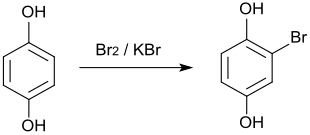
Vollständige Bromierung zum analytischen Nachweis liefert das 2,5-Dibromhydrochinon,[21] dessen Schmelzpunkt bei 186 °C liegt.[22] Ebenfalls bekannt ist das Tetrabromhydrochinon, welches jedoch aus Benzochinon dargestellt wird.
Methylierung mit Dimethylsulfat ergibt das 1,4-Dimethoxybenzol, dessen Schmelzpunkt bei 56 °C liegt.

Eine direkte Nitrierung des Hydrochinons ist nicht möglich, da es dabei zerfällt.[23] Die Hydroxygruppen müssen daher durch Reaktion mit Essigsäureanhydrid und Schwefelsäure als Katalysator[24] mit Acetylgruppen geschützt werden, dann findet eine Nitrierung an den Positionen 2 und 6 statt. Die Verseifung des entstehenden Dinitrodiacetylhydrochinons führt schließlich zu 2,6-Dinitrohydrochinon (Schmelzpunkt 135–136 °C).[23]
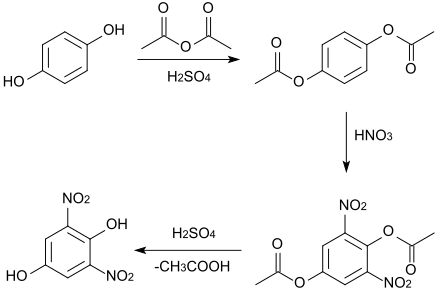
Verwendung[Bearbeiten | Quelltext bearbeiten]
In der Fotolabortechnik wird Hydrochinon als Reduktionsmittel zum Entwickeln von Filmen und Bildern eingesetzt. Wegen der Gefahren für Umwelt und Gesundheit gibt es Bestrebungen, die Substanz für diese Anwendungen nach Möglichkeit durch weniger riskante Stoffe zu ersetzen. Es wird auch als Inhibitor für Radikalreaktionen genutzt, um die Bildung von Etherperoxiden zu verhindern.
Hydrochinon ist im Annex II (Liste der unerlaubten Stoffe) der Kosmetikverordnung aufgeführt,[25] somit ist die kosmetische Verwendung – etwa in Hautcremes zur Hautaufhellung – in den Ländern der EU verboten.[26]
Toxikologie[Bearbeiten | Quelltext bearbeiten]
Es gibt keine Studien zur direkten Toxizität von Hydrochinon im Menschen. Allerdings wurde in mehreren Studien an Tieren gezeigt, dass Hydrochinon für die Niere toxisch ist.[27][28] Außerdem ist Hydrochinon immunotoxisch und spielt vermutlich auch bei der Immunotoxizität von Benzen eine bedeutende Rolle.[29]
Wenn Hydrochinon dermal aufgetragen wird, kann es zu allergischen und auch systematischen allergischen Reaktionen kommen.[30]
Kanzerogenität[Bearbeiten | Quelltext bearbeiten]
Zum Menschen liegen zwei Kohortenstudien vor, einmal von dänischen Lithographen und von Industriearbeitern, in denen der Zusammenhang zwischen einer Exposition mit Hydrochinon und dem Auftreten von Krebs allgemein und auch spezifischen Tumoren untersucht wurde. In keiner der beiden Studien konnte ein Zusammenhang festgestellt werden, auch wenn sich unter den Lithographen eine erhöhte Inzidenz an Melanomen zeigte.[31][32]
In Rattenversuchen konnte bei wiederholter Gabe von Hydrochinon ein erhöhtes Auftreten bestimmter Tumore in der Leber und der Niere gezeigt werden.[33]
Es wird daher angenommen, dass Hydrochinon, wie auch andere Dihydroxybenzene (z. B. Catechol) karzinogen und genotoxisch ist.[29]
Mögliche Wirkmechanismen[Bearbeiten | Quelltext bearbeiten]
In Versuchen an Leberzellen führte Hydrochinon zu einer Depletion von Antioxidanzien in der Zelle, konkret von Glutathion. Außerdem konnte in der Zellkultur gezeigt werden, dass Hydrochinon DNA-Addukte bildet und die Bildung von 8-OHdG, einem Standardmarker für DNA-Schäden, erhöht. Es wird angenommen, dass diese DNA-Schäden im Zusammenhang mit der Bildung von ROS stehen.[34][33][35][36]
Metabolismus[Bearbeiten | Quelltext bearbeiten]
Hydrochinon wird im Menschen hauptsächlich zu Sulfat- und Glucoronidkonjugaten verstoffwechselt. Im Rahmen dieser Stoffwechselwege entsteht neben reaktiven Intermediaten, wie zum Beispiel Semichinone und ROS, auch 1,4-Benzochinon. Diese Verstoffwechselung wird durch eine Reihe von Oxidasen katalysiert.[37][38][39] Damit ist der Metabolismus von Hydrochinon dem von Catechol ähnlich.
Gefahrenbewertung[Bearbeiten | Quelltext bearbeiten]
Hydrochinon wurde 2012 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Hydrochinon waren die Besorgnisse bezüglich der Einstufung als CMR-Stoff, Verbraucherverwendung, hoher (aggregierter) Tonnage, hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) und weit verbreiteter Verwendung. Die Neubewertung fand ab 2012 statt und wurde von Italien durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[40][41]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu HYDROQUINONE in der CosIng-Datenbank der EU-Kommission, abgerufen am 14. Mai 2020.
- ↑ a b c d e f g h i Eintrag zu Hydrochinon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. Januar 2024. (JavaScript erforderlich)
- ↑ a b S. C. Wallwork, H. M. Powell: The crystal structure of the α form of quinol. In: J. Chem. Soc. Perkin Trans. Band 2, 1980, S. 641–646, doi:10.1039/P29800000641.
- ↑ a b c S. V. Lindemann, V. E. Shklover, Yu. T. Struchkov: The β-modification of hydroquinone, C6H6O2. In: Cryst. Struct. Commun. Band 10, 1981, S. 1173–1179.
- ↑ a b c K. Maartmann-Moe: The crystal structure of γ-hydroquinone. In: Acta Cryst. Band 21, 1966, S. 979–982, doi:10.1107/S0365110X66004286.
- ↑ a b Eintrag zu Hydrochinon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. August 2018.
- ↑ Eintrag zu Hydroquinone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 123-31-9 bzw. Hydrochinon), abgerufen am 2. November 2015.
- ↑ F. Wöhler: Ueber das Chinon. In: Pharmaceutisches Centralblatt. Nr. 39, 1844, S. 609–615. (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ H. Schildknecht, K. Holoubekal: Die Bombardierkäfer und ihre Explosionschemie. In: Angewandte Chemie. 73 (1), 1961, S. 1–7. doi:10.1002/ange.19610730102.
- ↑ Werner Nachtigall, A. Wisser: Biologisches Design. 1. Auflage. Springer-Verlag, Berlin 2005, ISBN 3-540-22789-X. (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Gerhard G. Habermehl: Gift-Tiere und ihre Waffen. 5., aktual. und erweit. Auflage. Springer-Verlag, Berlin 1994, ISBN 3-540-56897-2. (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ K. Elbs: Ueber Nitrohydrochinon. In: J. Prakt. Chem. 48, 1893, S. 179–185. doi:10.1002/prac.18930480123.
- ↑ W. A. Caspari: The crystal structure of quinol. Part I. In: J. Chem. Soc. 1926, S. 2944–2248. doi:10.1039/JR9262902944.
- ↑ a b c W. A. Caspari: The crystal structure of quinol. Part II. In: J. Chem. Soc. 1927, S. 1093–1095. doi:10.1039/JR9270001093.
- ↑ a b c d e M. Naoki, T. Yoshizawa, N. Fukushima, M. Ogiso, M. Yoshino: A New Phase of Hydroquinone and Its Thermodynamic Properties. In: J. Phys. Chem. B 103, 1999, S. 6309–6313. doi:10.1021/jp990480k.
- ↑ D. E. Palin, H. M. Powell: Hydrogen Bond Linking of Quinol Molecules. In: Nature. Band 156, 1948, S. 334. doi:10.1038/156334a0.
- ↑ D. E. Palin, H. M. Powell: The structure of molecular compounds. Part III. Crystal structure of addition complexes of quinol with certain volatile compounds. In: J. Chem. Soc. 1947, S. 208–221. doi:10.1039/JR9470000208.
- ↑ D. E. Palin, H. M. Powell: The structure of molecular compounds. Part VI. The β-type clathrate compounds of quinol. In: J. Chem. Soc. 1948, S. 815–821. doi:10.1039/JR9480000815.
- ↑ Autorengemeinschaft: Organikum. 19. Auflage. Johann Ambrosius Barth, Leipzig/ Berlin/ Heidelberg 1993, ISBN 3-335-00343-8, S. 331.
- ↑ M. Kohn, L. W. Guttmann: Zur Kenntnis der Bromsubstitionsprodukte des Hydrochinons. In: Monatshefte für Chemie. 45 (10), 1924, S. 573–588. doi:10.1007/BF01524599.
- ↑ Autorengemeinschaft: Organikum. 19. Auflage. Johann Ambrosius Barth, Leipzig/ Berlin/ Heidelberg 1993, ISBN 3-335-00343-8, S. 653.
- ↑ a b Gustav Walther: Methylether des 2,6-Dinitrohydrochinons und einige Derivate. Dissertation. Universität Basel, 1904.
- ↑ H. Bock, S. Nick, C. Näther, J. W. Bats: Dinatrium- und Dikalium-Nitranilate: Die Cyanin-Verzerrung der Kohlenstoff-Sechsringe. In: Zeitschrift für Naturforschung B. 49, 1994, S. 1021–1030 (PDF, freier Volltext).
- ↑ Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates vom 30. November 2009 über kosmetische Mittel: Annex II - Liste der Stoffe, die in kosmetischen Mitteln verboten sind (html, pdf), abgerufen am 4. April 2023.
- ↑ I. Winterhagen: Harmlos – aber störend, Deutsche Apothekerzeitung, Nr. 33, S. 48, 18. August 2016
- ↑ National Toxicology Program: NTP Toxicology and Carcinogenesis Studies of Hydroquinone (CAS No. 123-31-9) in F344/N Rats and B6C3F1 Mice (Gavage Studies). In: National Toxicology Program Technical Report Series. Band 366, Oktober 1989, S. 1–248, PMID 12692638.
- ↑ Masa-Aki Shibata, Masao Hirose, Hikaru Tanaka, Emiko Asakawa, Tomoyuki Shirai: Induction of Renal Cell Tumors in Rats and Mice, and Enhancement of Hepatocellular Tumor Development in Mice after Long-term Hydroquinone Treatment. In: Japanese Journal of Cancer Research. Band 82, Nr. 11, 1991, S. 1211–1219, doi:10.1111/j.1349-7006.1991.tb01783.x, PMID 1752780, PMC 5918322 (freier Volltext).
- ↑ a b International Agency for Research on Cancer.: Re-evaluation of some organic chemicals, hydrazine and hydrogen peroxide. World Health Organization, International Agency for Research on Cancer, Lyon, Frankreich 1999, ISBN 978-92-832-1271-3.
- ↑ A. Barbaud, P. Modiano, M. Cocciale, S. Reichert, J.-L. Schmutz: The topical application of resorcinol can provoke a systemic allergic reaction. In: British Journal of Dermatology. Band 135, Nr. 6, 1996, S. 1014–1015, doi:10.1046/j.1365-2133.1996.d01-1121.x.
- ↑ J. W. Pifer, F. T. Hearne, F. A. Swanson, J. L. O’Donoghue: Mortality study of employees engaged in the manufacture and use of hydroquinone. In: International Archives of Occupational and Environmental Health. Band 67, Nr. 4, 1995, S. 267–280, doi:10.1007/BF00409409, PMID 7591188.
- ↑ Bd Carlton, H Shah: Re: "Malignant melanoma among lithographers" by H Nielsen, L Henriksen, JH Olsen. Scand J Work Environ Health 1996;22:108--11. In: Scandinavian Journal of Work, Environment & Health. Band 23, Nr. 4, August 1997, S. 308, doi:10.5271/sjweh.224.
- ↑ a b U. Stenius, M. Warholm, A. Rannug, S. Walles, I. Lundberg: The role of GSH depletion and toxicity in hydroquinone-induced development of enzyme-altered foci. In: Carcinogenesis. Band 10, Nr. 3, März 1989, S. 593–599, doi:10.1093/carcin/10.3.593, PMID 2564322.
- ↑ Junzo Suzuki, Yuichiro Inoue, Shizuo Suzuki: Changes in the urinary excretion level of 8-hydroxyguanine by exposure to reactive oxygen-generating substances. In: Free Radical Biology and Medicine. Band 18, Nr. 3, 1. März 1995, S. 431–436, doi:10.1016/0891-5849(94)00152-A (sciencedirect.com [abgerufen am 30. Juni 2020]).
- ↑ G. Lévay, W. J. Bodell: Role of hydrogen peroxide in the formation of DNA adducts in HL-60 cells treated with benzene metabolites. In: Biochemical and Biophysical Research Communications. Band 222, Nr. 1, 6. Mai 1996, S. 44–49, doi:10.1006/bbrc.1996.0695, PMID 8630072.
- ↑ G. Levay, K. Pongracz, W. J. Bodell: Detection of DNA adducts in HL-60 cells treated with hydroquinone and p-benzoquinone by 32P-postlabeling. In: Carcinogenesis. Band 12, Nr. 7, Juli 1991, S. 1181–1186, doi:10.1093/carcin/12.7.1181, PMID 2070482.
- ↑ World Health Organization: Hydroquinone. In: World Health Organization (Hrsg.): Environmental Health Criteria. Band 157. Genf 1994.
- ↑ B. A. Hill, H. E. Kleiner, E. A. Ryan, D. M. Dulik, T. J. Monks: Identification of multi-S-substituted conjugates of hydroquinone by HPLC-coulometric electrode array analysis and mass spectroscopy. In: Chemical Research in Toxicology. Band 6, Nr. 4, Juli 1993, S. 459–469, doi:10.1021/tx00034a012, PMID 8374043.
- ↑ Vangala V. Subrahmanyam, Prema Kolachana, Martyn T. Smith: Metabolism of hydroquinone by human myeloperoxidase: Mechanisms of stimulation by other phenolic compounds. In: Archives of Biochemistry and Biophysics. Band 286, Nr. 1, 1. April 1991, S. 76–84, doi:10.1016/0003-9861(91)90010-G (sciencedirect.com [abgerufen am 30. Juni 2020]).
- ↑ Europäische Chemikalienagentur (ECHA): Substance Evaluation Conclusion and Evaluation Report.
- ↑ Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Hydroquinone, abgerufen am 26. März 2019.



