2-Chlorpropansäure
| Strukturformel | ||||||||
|---|---|---|---|---|---|---|---|---|

| ||||||||
| (R)-Form (links) und (S)-Form (rechts) | ||||||||
| Allgemeines | ||||||||
| Name | 2-Chlorpropansäure | |||||||
| Andere Namen |
α-Chlorpropionsäure | |||||||
| Summenformel | C3H5ClO2 | |||||||
| Kurzbeschreibung |
farblos bis gelbliche fast geruchlose Flüssigkeit[1] | |||||||
| Externe Identifikatoren/Datenbanken | ||||||||
| ||||||||
| Eigenschaften | ||||||||
| Molare Masse | 108,52 g·mol−1 | |||||||
| Aggregatzustand |
flüssig | |||||||
| Dichte |
1,26 g·cm−3[1] | |||||||
| Schmelzpunkt |
−12 °C[1] | |||||||
| Siedepunkt |
186 °C[1] | |||||||
| Dampfdruck | ||||||||
| pKS-Wert |
2,8[2] | |||||||
| Löslichkeit | ||||||||
| Brechungsindex |
1,4380 (20 °C)[4] | |||||||
| Sicherheitshinweise | ||||||||
| ||||||||
| Toxikologische Daten | ||||||||
| Thermodynamische Eigenschaften | ||||||||
| ΔHf0 |
−522,5 kJ/mol[6] | |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||
2-Chlorpropionsäure ist eine chemische Verbindung aus der Gruppe der Propionsäurederivate.
Wenn in diesem Text oder in der wissenschaftlichen Literatur „2-Chlorpropionsäure“ ohne weiteren Namenszusatz (Präfix) erwähnt wird, ist racemische 2-Chlorpropionsäure [Synonyme: DL-2-Chlorpropionsäure, (±)-2-Chlorpropionsäure und (RS)-2-Chlorpropionsäure] gemeint, also ein 1:1-Gemisch der beiden Enantiomeren.
Gewinnung und Darstellung
2-Chlorpropionsäure kann durch Chlorierung von Propionsäure mit PCl3, S2Cl2 oder Chlorsulfonsäure gewonnen werden. Das L-Enantiomer wird aus D-Milchsäure und Thionylchlorid hergestellt.[3]
Eigenschaften
2-Chlorpropionsäure ist eine farblose bis gelbliche, fast geruchlose Flüssigkeit. Oberhalb von 60 °C beginnt sie sich zu zersetzen, wobei Chlorwasserstoff, Kohlenstoffmonoxid und Kohlenstoffdioxid entstehen.
Verwendung
2-Chlorpropionsäure wird zur Herstellung von Farbstoffen, Arzneimitteln und Herbiziden verwendet.[1] Die Phenoxypropionsäurederivate wie Clodinafop, Fenoxaprop, Fluazifop, Haloxyfop, Isoxapyrifop, Quizalofop sowie die Phenoxycarbonsäuren Dichlorprop, Fenoprop, Flamprop, Mecoprop und das Acetylalanin Benalaxyl werden ausgehend von 2-Chlorpropionsäure dargestellt.[7]
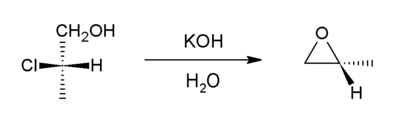
Die Reduktion von (S)-2-Chlorpropionsäure mit Lithiumaluminiumhydrid ergibt (S)-2-Chlorpropanol, den einfachsten Chloralkohol, welcher mit Kaliumhydroxid weiter zu (R)-Methyloxiran reagiert.[8]
Verwandte Verbindungen
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu 2-Chlorpropionsäure in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ Bernd Engels, Carsten Schmuck, Tanja Schirmeister, Reinhold Fink: Chemie für Mediziner. Pearson Deutschland GmbH, 2008, ISBN 3-8273-7286-0, S. 553 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Toxikologische Bewertung von α-Chlorpropionsäure und Natrium-α-Chlorpropionat (PDF) bei der Berufsgenossenschaft Rohstoffe und chemische Industrie (BG RCI)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-112.
- ↑ Eintrag zu 2-chloropropionic acid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA) Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-23.
- ↑ Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 1030 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Koppenhoefer, B. und Schurig, V.: (R)-Alkyloxiranes of High Enantiomeric Purity from (S)-2-Chloroalkanoic Acids via (S)-2-Chloro-1-Alkanols: (R)-Methyloxirane In: Organic Syntheses. 66, 1988, S. 160, doi:10.15227/orgsyn.066.0160; Coll. Vol. 8, 1993, S. 434 (PDF).