Tagatose
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Fischer-Projektion, offenkettige Darstellung | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name |
| |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C6H12O6 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 180,16 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
löslich in Wasser[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Tagatose ist ein Monosaccharid mit sechs Kohlenstoff-Atomen. Dieser Zucker gehört zur Gruppe der Ketohexosen. D-Tagatose eignet sich als Süßstoff, da er – verglichen mit Fructose – bei 92 % Süßkraft nur 38 % des physiologischen Brennwerts besitzt.
Wie bei jedem Zucker (außer Dihydroxyaceton) gibt es zwei enantiomere Formen, die sich wie Bild und Spiegelbild verhalten.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
D-Tagatose kommt in der Natur – wenn auch in geringer Menge – in einigen Milchprodukten vor.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Kommerziell wird D-Tagatose aus Lactose gewonnen. Dabei wird das Disaccharid zuerst hydrolytisch zu Glucose und Galactose gespalten. Nach der Auftrennung des Gemisches wird die Galactose unter alkalischen Bedingungen zur D-Tagatose isomerisiert.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
In wässriger Lösung kommt es zu einem intramolekularen Ringschluss, sodass sich ein Gleichgewicht zwischen der Ketoform (weniger als 1 %) und den beiden Ringformen (Furanose-Form und Pyranose-Form) einstellt. Die Lage des Gleichgewichts ist von der Temperatur abhängig und beeinflusst auch die Süßungskraft des Zuckers. Bei 27 °C stellt sich folgendes Gleichgewicht ein:
- α-Pyranose-Form: 79 % β-Pyranose-Form: 16 %
- α-Furanose-Form: 1 % β-Furanose-Form: 4 %
D-Tagatose – Schreibweisen Keilstrichformel Haworth-Schreibweise 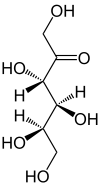

α-D-Tagatofuranose
β-D-Tagatofuranose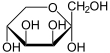
α-D-Tagatopyranose
β-D-Tagatopyranose
In Studien mit Versuchspersonen konnte gezeigt werden, dass D-Tagatose nicht kariogen und damit zahnfreundlich ist. Im Vergleich zu Glucose zeigt es eine sehr geringe Insulinreaktion. In größeren Mengen wirkt es abführend.[2]
Verwendung[Bearbeiten | Quelltext bearbeiten]
D-Tagatose wird im Diät-Trinkeis Diet Slurpee der Firma PepsiCo exklusiv für den amerikanischen Markt in 7-Eleven Geschäften angeboten.[3] In den USA gibt es zudem eine Zulassung für die Verwendung als Überzugsmittel („Frosten“) bei kleiehaltigen Frühstücksflocken, wo es aufgrund der hohen Kristallisationsgeschwindigkeit technologisch von Interesse ist. In Schokolade kann es als alleiniges Süßungsmittel eingesetzt werden.[2] In Europa wurde es 2005 als Novel Food zugelassen.[4]
Derivate[Bearbeiten | Quelltext bearbeiten]
Ein Derivat der Tagatose ist die Fuculose (6-Desoxy-tagatose).
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Datenblatt D-(−)-Tagatose bei Alfa Aesar, abgerufen am 23. Dezember 2019 (Seite nicht mehr abrufbar).
- ↑ a b Kurt Rosenplenter, Gert-Wolfhard von Rymon Lipinski, Ulrich Nöhle: Handbuch Süßungsmittel. Behr’s Verlag, 2007, ISBN 978-3-89947-947-8.
- ↑ Joachim Bröckel: EU-Kartellwächter genehmigen SweetGredients. In: Akzente. Januar 2004, Nordzucker
- ↑ Öffentliche Konsultation: Umrechnungsfaktor für Energiewert von D-Tagatose zu Kennzeichnungszwecken, Europäische Behörde für Lebensmittelsicherheit, 18. Juli 2016.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- W. L. P. Bredie, S. Bachmann, S. M. B. Johansen, G Hansen: The sweetness of D-tagatose - a novel food ingredient. ( vom 15. November 2007 im Internet Archive)




