„Schlaganfall“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
→Literatur: +Wikilinks |
→Epidemiologie: US-Quelle und internationale Quelle ergänzt wegen des Hinweises zu staatslastig. Markierung: 2017-Quelltext-Bearbeitung |
||
| Zeile 18: | Zeile 18: | ||
51 % aller Schlaganfälle betreffen die Altersgruppe der über 75-Jährigen. Mit zunehmendem Alter steigt das Schlaganfallrisiko überproportional.<ref>E. Rupp: [https://edoc.ub.uni-muenchen.de/15751/1/Rupp_Eckart.pdf ''Fortschritte in Behandlung und Diagnostik zentraler neurogener Sprachstörungen.''] (PDF) Dissertation. [[Ludwig-Maximilians-Universität München]], 2. Juli 2010.</ref> |
51 % aller Schlaganfälle betreffen die Altersgruppe der über 75-Jährigen. Mit zunehmendem Alter steigt das Schlaganfallrisiko überproportional.<ref>E. Rupp: [https://edoc.ub.uni-muenchen.de/15751/1/Rupp_Eckart.pdf ''Fortschritte in Behandlung und Diagnostik zentraler neurogener Sprachstörungen.''] (PDF) Dissertation. [[Ludwig-Maximilians-Universität München]], 2. Juli 2010.</ref> |
||
In den USA sind Schlaganfälle die fünfthäufigste Todesursache<ref>{{Literatur |Autor=Emelia J Benjamin und andere für die "American Heart Association Statistics Committee and Stroke Statistics |
|||
Subcommittee" |Titel=Heart Disease and Stroke Statistics—2017 Update |Hrsg= |Sammelwerk=Circulation |Band=135 |Nummer=10 |Auflage= |Verlag= |Ort= |Datum=7.3.2017 |ISBN= |DOI=10.1161/CIR.0000000000000485 |Seiten=e146–e603}}</ref>. Weltweit ist der Schlaganfall eine häufigsten Ursachen für eine Behinderung<ref>{{Literatur |Autor=for the GBD 2013 Stroke Panel Experts Group, Gregory A. Roth, Christopher J. L. Murray, Theo Vos, Catherine O. Johnson |Titel=Stroke Prevalence, Mortality and Disability-Adjusted Life Years in Adults Aged 20-64 Years in 1990-2013: Data from the Global Burden of Disease 2013 Study |Sammelwerk=Neuroepidemiology |Band=45 |Nummer=3 |Datum=2015 |ISSN=1423-0208 |DOI=10.1159/000441098 |PMID=26505983 |Seiten=190–202 |Online=https://www.karger.com/Article/FullText/441098 |Abruf=2018-12-23}}</ref>. |
|||
== Formen eines Schlaganfalls – Minderdurchblutung oder Blutung == |
== Formen eines Schlaganfalls – Minderdurchblutung oder Blutung == |
||
Version vom 23. Dezember 2018, 16:26 Uhr
Ein Schlaganfall (auch Gehirnschlag, Hirnschlag, Apoplexie,[1] zerebraler Insult, apoplektischer Insult, Apoplexia cerebri, Ictus apoplecticus, veraltet Schlagfluss, umgangssprachlich Schlag, in der medizinischen Umgangssprache häufig auch Apoplex oder Insult) ist eine plötzlich („schlagartig“) auftretende zerebrovaskuläre Erkrankung des Gehirns, die oft zu einem länger anhaltenden Ausfall von Funktionen des Zentralnervensystems führt und durch kritische Störungen der Blutversorgung des Gehirns verursacht wird.
Begriffsklärung
Die Terminologie des Schlaganfalls wurde[2] und wird nicht einheitlich benutzt. Gleichbedeutend zum Begriff Schlaganfall sind auch die englischen Termini Stroke, Cerebrovascular accident (CVA) und Cerebrovascular Insult (CVI).[3] Diese Bezeichnungen werden häufig als Oberbegriff für unterschiedliche neurologische Krankheitsbilder benutzt, deren wichtigste Gemeinsamkeit plötzliche Symptome nach einer auf das Gehirn begrenzten Durchblutungsstörung sind, wobei der Funktionsverlust definitionsgemäß[4] nicht auf primäre Störungen der Erregbarkeit von Nervenzellen zurückzuführen sein darf (konvulsive Störung, siehe Epilepsie).
Epidemiologie
Geschätzt gibt es in Deutschland jährlich etwa 270.000 Schlaganfallneuerkrankungen.[5] Jährliche Häufigkeiten in Deutschland:[6]
- durch Minderdurchblutung primär ischämische Hirninfarkte (Inzidenz 160–240 Ereignisse/100.000 Einwohner)
- Hirnblutungen (24/100.000)
- Einblutungen in den das Gehirn umgebenden Liquorraum, sogenannte Subarachnoidalblutungen (6/100.000)
- Schlaganfälle ungeklärter Ursache (8/100.000)
Der Schlaganfall gehört zu den häufigsten schweren Erkrankungen in Deutschland, hat eine 1-Jahres-Mortalität von 20 bis 30 % und ist auch eine häufige Todesursache in Deutschland: 2015 stellte das Statistische Bundesamt 56.982 Todesfälle durch zerebrovaskuläre Krankheiten fest, was einem Anteil von 6,2 % entspricht.[7]
Darüber hinaus ist der Schlaganfall mit einer Invaliditätsrate von 30 bis 35 % die häufigste Ursache für mittlere und schwere Behinderung.
51 % aller Schlaganfälle betreffen die Altersgruppe der über 75-Jährigen. Mit zunehmendem Alter steigt das Schlaganfallrisiko überproportional.[8] In den USA sind Schlaganfälle die fünfthäufigste Todesursache[9]. Weltweit ist der Schlaganfall eine häufigsten Ursachen für eine Behinderung[10].
Formen eines Schlaganfalls – Minderdurchblutung oder Blutung
Dem Schlaganfall liegt ein plötzlicher Mangel der Nervenzellen an Sauerstoff und anderen Substraten zugrunde. Grob unterscheiden lassen sich die plötzlich auftretende Minderdurchblutung (Ischämischer Schlaganfall oder Hirninfarkt) und die akute Hirnblutung (hämorrhagischer Infarkt oder Insult), die sekundär aufgrund ihrer raumfordernden Wirkung bzw. aufgrund des Fehlens des Bluts in nachgeordneten Regionen ebenfalls zu einer Ischämie führt. Bei primär ischämischen Infarkten kann es ebenfalls zu sekundären Blutungen im Infarktgebiet (hämorrhagische Infarzierung) kommen.[11]
Die Unterscheidung zwischen Minderdurchblutung und Blutung ist erst durch bildgebende Verfahren wie die Computertomographie (CT) oder Magnetresonanztomographie (MRT, englisch MRI) sicher möglich, wobei in den ersten Stunden beide Bildgebungsmethoden noch unauffällig sein können, dies insbesondere beim primär ischämischen Hirninfarkt. Die Verdachtsdiagnose einer Subarachnoidalblutung, welche infolge einer geplatzten Arterie (zum Beispiel aufgrund eines Aneurysmas) entsteht, kann - insbesondere bei nur milder Symptomatik (zum Beispiel alleinige Kopfschmerzen) - durch den Nachweis von Blutbestandteilen im Nervenwasser bei der Lumbalpunktion bestätigt werden.
Minderdurchblutungen, die kürzer als 24 Stunden andauern und von bloßem Auge ohne sichtbare Folgen bleiben, wurden früher als transitorische ischämische Attacke (TIA) bezeichnet. In den Leitlinien der Deutschen Gesellschaft für Neurologie von 2005 wird darauf hingewiesen, dass die klassische Differenzierung von transitorisch ischämischen Attacken (TIA) und vollendeten ischämischen Schlaganfällen als überholt gilt. Gleichwohl wird der Unterschied in manchen Lehrbüchern noch erwähnt. Zwei Gründe dafür sind, dass bei vielen Patienten mit einer sogenannten TIA morphologische Hirnverletzungen nachweisbar sind und dass das Risiko für einen Re-Infarkt nach TIA und vollendetem Schlaganfall etwa gleichermaßen erhöht ist. Abgesehen von der Frage der Lyse sollen sowohl vollendete Schlaganfälle als auch früher als TIA bezeichnete Zustände gleich behandelt werden.[12] Der Begriff (prolongiertes) reversibles ischämisches neurologisches Defizit (RIND/PRIND) für länger als 24 Stunden, aber kürzer als drei Wochen anhaltende Befunde soll ebenfalls nicht mehr angewendet werden, da dies bereits einem manifesten Schlaganfall entspricht.[13] Gleiches gilt für die Beschreibung eines partiell reversiblen ischämischen neurologischen Syndroms (PRINS).
Symptome
Als Zeichen eines Schlaganfalls können plötzlich, und je nach Schweregrad auch gleichzeitig, mehrere Symptome auftreten:[14]
- Bewusstseinsstörungen (Somnolenz, Koma), Orientierungsstörungen
- Taubheitsgefühl im Gesicht, in einem Arm, Bein oder einer ganzen Körperhälfte
- Lähmung oder Schwäche im Gesicht, in einem Arm, Bein oder einer ganzen Körperhälfte
- Verwirrung, Sprach- oder Wortfindungs-, Schrift- oder Verständnisstörung
- Schluckstörungen (Dysphagie)
- schmerzlose Sehstörung auf einem oder beiden Augen, einseitige Pupillenerweiterung, Gesichtsfeldausfall, Doppelbilder
- Schwindel, Gangstörung, Gleichgewichts- oder Koordinationsstörung (Ataxie)
- stärkster Kopfschmerz ohne erkennbare Ursache bei evtl. entgleistem (überhöhtem) Blutdruck, Übelkeit, Erbrechen
- Fehlende Wahrnehmung eines Teils der Umwelt oder des eigenen Körpers (Neglect)
Ursachen
- arterielle Embolien durch Blutgerinnsel
- Thrombosen der venösen Abflussgefäße
- Gefäßverengung durch Gefäßverkrampfungen
- Gefäßrisse: entweder spontan oder z. B. infolge hohen Blutdrucks
- Spontanblutungen bei gestörter Blutgerinnung
- Subarachnoidalblutung, sub- oder epidurale Hämatome
Diagnostik
Die Diagnose des Schlaganfalls wird klinisch gestellt, in der Regel durch einen Neurologen. Dieser bedient sich hierfür unterschiedlicher Untersuchungsmethoden, um die zahlreichen unterschiedlichen Funktionen des Gehirns zu überprüfen. Häufig orientieren sich diese Untersuchungen an Scoringsystemen wie der National Institutes of Health Stroke Scale (NIHSS), die eine quantitative Einschätzung der Schwere des Schlaganfalls ermöglicht. Je nach vermuteter Lokalisation des Schlaganfalls im Gehirn können jedoch auch speziellere Untersuchungen, z. B. des Kleinhirns oder der Hirnnerven, indiziert sein. Bei sich erhärtendem oder zumindest nicht mit Sicherheit ausgeschlossenem Verdacht auf Schlaganfall folgt in jedem Fall eine bildgebende Diagnostik.
Bildgebende Verfahren wie die Computertomographie (CT) oder Magnetresonanztomographie (MRT, englisch MRI) ermöglichen die sofortige Diagnose einer Hirnblutung. Beim ischämischen Schlaganfall hingegen kann eine native (d. h. ohne Kontrastmittel) CT- bzw. MRT-Untersuchung während der ersten Stunden unauffällige Bilder liefern. Je nach Ursache, Lokalisation und Schwere des Schlaganfalls können sich eine CT-Angiographie (CTA) und eine CT-Perfusion anschließen. Diffusionsgewichtete Aufnahmen (DW-MRI) ermöglichen in der MRT-Untersuchung schon wenige Minuten nach Beginn des Schlaganfalls eine Darstellung des Infarktgebiets.
Eine feine Subarachnoidalblutung kann unter Umständen in den bildgebenden Verfahren unsichtbar sein. Sie kann dann sensitiver durch den Nachweis von Blutbestandteilen im Nervenwasser durch eine Lumbalpunktion festgestellt werden.
Eine Blutabnahme bei Verdacht auf Schlaganfall ist obligatorisch. Hierbei wird neben einem Blutbild insbesondere der Gerinnungsstatus bestimmt. Blut-Biomarker (z. B. S-100B, NSE, GFAP), die auf Schäden des Gehirns hinweisen können, können die Diagnostik ergänzen, sind jedoch nicht spezifisch für einen Schlaganfall und in der Frühphase bisweilen unauffällig.
Speziell für Rettungsdienstpersonal wurde 1997 die Cincinnati Prehospital Stroke Scale (CPSS) entwickelt.[15][16] Diese wird aus drei Kriterien der NIHSS gebildet und soll als ein einfaches Instrument zur Diagnose eines Schlaganfalls dienen. Auch in der Laien-Ausbildung für Erste Hilfe werden die Kriterien der CPSS oft mit dem englischen Akronym FAST vermittelt (Face, Arms, Speech, Time).[17] Dieser Test besteht aus vier Schritten:
- Face (Gesicht): Die Person auffordern, z. B. breit zu lächeln oder die Zähne zu zeigen, da eine gelähmte Gesichtshälfte ein Symptom eines Schlaganfalls sein kann. Eine andere Methode ist, die betroffene Person die Backen aufblasen zu lassen und darauf leichten Widerstand auszuüben; betroffene Personen können eine Seite nicht aufblasen oder nicht gegen den Widerstand aufgeblasen halten.
- Arms (Arme): Die Person wird aufgefordert, beide Arme mit nach oben geöffneten Handflächen nach vorne zu strecken, sodass die Arme ohne Unterstützung im 90°-Winkel zur Körperachse gehalten werden. Bei einer Lähmung kann ein Arm nicht in die verlangte Position gebracht oder in ihr gehalten werden, sinkt oder dreht sich nach innen.
- Speech (Sprache): Man achtet auf die Aussprache der Person. Sie kann undeutlich oder verlangsamt sein, sich „verwaschen“ anhören, oder die Person scheint Schwierigkeiten zu haben, ihre Gedanken in Worte zu fassen.
- Time (Zeit): Besteht der Verdacht eines Schlaganfalls, muss die betroffene Person so schnell wie möglich mit dem Rettungsdienst in eine geeignete Klinik transportiert werden. Auf langwierige Behandlungen vor Ort („stay and play“) wird verzichtet, hier gilt der Grundsatz „load and go“, weil es keine wirksame präklinische Therapie gibt. Die Behandlung muss binnen kürzester Zeit erfolgen, um Hirnschädigungen so gering wie möglich zu halten. Wichtig ist ein Festhalten des zeitlichen Beginns der Symptome und der zeitliche Verlauf (Verschlechterung bzw. Besserung).
Einschränkungen erfährt die CPSS insbesondere durch ihre Fokussierung auf Symptome eines kortikalen Infarkts. Sie ist damit zwar in der Lage, eine Vielzahl von schweren Schlaganfällen mit relativ hoher Sensitivität zu erkennen, verpasst aber unter Umständen seltenere Schlaganfälle in anderen Bereichen.
Therapie
Schlaganfallpatienten, auch Verdachtsfälle, sollten unverzüglich ärztlich untersucht werden. Die sogenannte „time-to-needle“ (Zeitspanne, innerhalb derer eine etwaige Lyse-Behandlung [s. u.] begonnen sein muss) liegt bei 4,5 Stunden nach dem Schlaganfall.[18] Nach dem unverzüglichen Absetzen eines Notrufs sollte der Patient beobachtet und mit erhöhtem Oberkörper gelagert werden. Keine körperliche Belastung. Nichts trinken, nichts essen, da Aspirationsgefahr besteht. Das bedeutet, dass das Gehirn evtl. den Schluckvorgang nicht mehr richtig steuern kann, und so die Gefahr des Verschluckens besteht. Notfalltransport mit Rettungswagen, eventuell mit Notarzt, in eine Stroke Unit (spezialisierte Abteilung zur Schlaganfall-Behandlung – nicht unbedingt/immer Bestandteil einer neurologischen Klinik) zur genauen Diagnostik, ggf. Lyse-Behandlung und Therapie der Folgen.[19] Auf dem Land – mit einer entsprechend geringen Dichte an Stroke Units – kommt häufig auch ein Rettungshubschrauber zum Einsatz, da mit diesem ein schnellerer Transport in ein weiter entferntes, dafür geeignetes Krankenhaus durchgeführt werden kann. Zum Teil sind die zurückzulegenden Entfernungen so groß, dass selbst nachts der Einsatz eines Intensivtransporthubschraubers (welcher eine wesentlich höhere Vorlaufzeit als ein RTH hat) in Erwägung gezogen werden kann. Auch speziell ausgerüstete Rettungswagen, sogenannte Mobile Stroke Units, kommen hier teilweise zum Einsatz.[20]
Bei hämorrhagischen Schlaganfällen ist die Lyse-Behandlung nicht angezeigt. In vielen Ischämie-Fällen hingegen gelingt es durch die intravenöse Verabreichung von Medikamenten (Thrombolyse), das Blutgerinnsel aufzulösen und das Gehirn vor einem dauerhaften Schaden zu bewahren. Eine frühe Thrombolyse verbessert nachweislich die Prognose der Patienten.[21]
Ein recht neues Verfahren, die Neurothrombektomie, entfernt mechanisch mit einem Katheter (neuro thrombectomy catheter[22]) das Blutgerinnsel im Gehirn.[23] „Mehr als 60 Prozent der Patienten mit großen Schlaganfällen können nach der Katheterbehandlung bereits nach drei Monaten wieder ein eigenständiges Leben führen. Bei der medikamentösen Therapie liegt diese Quote bei nur etwa 15 Prozent“.[24] Insbesondere für Patienten, bei denen das Blutgerinnsel ein großes Gefäß im Gehirn verschließt, ist die Thrombektomie wirkungsvoll. In rund 90 Prozent der Fälle kann das Gefäß wieder eröffnet werden. Die Neurothrombektomie kann allerdings bei nur etwa 10 bis 15 Prozent der ischämischen Schlaganfälle eingesetzt werden. Bislang wird dieses Verfahren in Deutschland in etwa 140 Krankenhäusern angeboten und wird stetig auf neue Kliniken ausgeweitet (Stand Oktober 2017).[25] Im Lauf des Jahrs 2015 zeigten fünf Studien eine Überlegenheit des Katheters gegenüber der medikamentösen Therapie.[26]
Prävention
Der persönliche Lebensstil beeinflusst das Risiko, einen Schlaganfall zu erleiden. Vor allem ein normaler Blutdruck, gute Blutzuckerwerte und Nicotin-Abstinenz können das Schlaganfallrisiko reduzieren. Allein ein Blutdruck im Normbereich vermindert das Schlaganfallrisiko um 60 Prozent. Weitere Aspekte eines gesunden Lebensstils sind die körperliche Aktivität, die Vermeidung von Übergewicht, normale Cholesterin-Werte und eine gesunde Ernährung.[27] Studien zufolge stellt ein hoher Konsum von Salz einen Risikofaktor dar,[28] der Konsum von Kalium hingegen einen Schutzfaktor.[29]
Im Rahmen der Ursachensuche und damit im Sinne der Sekundärprävention nach einem Schlaganfall sollte auch nach einem intermittierenden (paroxysmalen) Vorhofflimmern gesucht werden. Hierbei wird ein Untersuchungszeitraum von 24 bis 72 Stunden empfohlen. Bei Nachweis von auch nur zeitweisem Vorhofflimmern sollte eine Gerinnungshemmung mit Phenprocoumon oder direkten oralen Antikoagulanzien (DOAK) erfolgen.[30]
Rehabilitation

Die medizinische Rehabilitation von Patienten mit zerebrovaskulärer Insuffizienz beginnt idealerweise postakut in einer Stroke Unit. Rehabilitative Ansätze wie das des Bobath-Konzepts erfordern ein hohes Maß an interdisziplinärer Zusammenarbeit und sind bei konsequenter Ausführung für den Rehabilitationsverlauf maßgeblich mitverantwortlich. Ein neuer und wissenschaftlich mehrfach validierter Ansatz ist die „Constraint-Induced Movement Therapy“ (CIMT),[31] bei der durch Immobilisation des gesunden Arms für den Großteil der Wachperiode der Patient zum Gebrauch der erkrankten Hand „gezwungen“ wird, wodurch krankhafte Anpassungsphänomene wie der „erlernte Nichtgebrauch“ verhindert werden können. Diese Therapiemethode ist auch bei schwer betroffenen Patienten und im chronischen Stadium einsetzbar. Die Methode ist im deutschsprachigen Raum auch als „Taubsche Bewegungsinduktion“. bekannt.[32]
Im Zentrum der neurologischen Rehabilitation stehen vor allem Maßnahmen, welche die Körperwahrnehmung des Betroffenen fördern und im besten Falle zur vollständigen Kompensation verlorener Fähigkeiten führen.
So werden beispielsweise zur Wiederherstellung der Gehfähigkeit Gangmuster mit Physiotherapeuten eingeübt. Ergotherapeuten arbeiten gezielt mit den Patienten zur (teilweisen) Wiederherstellung der sensomotorischen Fähigkeiten.
Die Bedeutung einer gezielten Logopädie bereits in der Frühphase und über einen langen Zeitraum wird häufig unterschätzt und nur laienhaft angegangen. Für bestimmte Therapiebereiche gibt es bisher kein ausreichendes Angebot im ambulanten Bereich, wie in der Sprachtherapie v. a. bei Aphasie und Dysarthrie. In der rehabilitativen Therapie ist ein hochfrequentes, repetitives Üben bestimmter Aufgaben sinnvoll, die Teletherapie ermöglicht eine supervidierte Versorgung von Patienten.[33] Eine intensive Behandlung ist im niedergelassenen Setting nicht zu erbringen. Nur durch Nutzung computergestützter Verfahren kann die Intensität so erhöht werden, dass die sich aus den Vorgaben der Metastudie ergebenden Zielgrößen erreicht werden. Machbarkeitsstudien belegen, dass für etwa 50–60 % der aphasischen Patienten Teletherapie sinnvoll ist. Tatsächlich konnte durch die Teletherapiestudie erstmals gezeigt werden, dass die Therapiefrequenz durch supervidierte Teletherapie ohne Qualitätsverlust so angehoben wird, dass Patienten nachweislich davon profitieren.
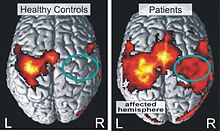
Moderne Ansätze der Neurorehabilitation versuchen krankhafte Hirnaktivität zu beeinflussen. So findet sich bei einigen Patienten eine enthemmte Aktivität der nicht-geschädigten Hemisphäre, welche die motorischen Funktionen der vom Schlaganfall betroffenen Hirnhälfte stört. Eine Reduktion der Überaktivität, zum Beispiel mit Hilfe der transkraniellen Magnetstimulation (TMS), kann bei einem Teil der Patienten zu einer besseren Funktion der gelähmten Hand führen.[34] Derzeit läuft an den National Institutes of Health (NIH) eine Multicenter-Studie zur Wirksamkeit der Magnetstimulationstherapie in Kombination mit einer pharmakologischen Stimulation mit dem Dopamin-Präparat „Levo-DOPA“. Durch Letzteres sollen die TMS-Effekte verstärkt werden. Auch andere Medikamente aus der Gruppe der monoaminergen Substanzen wie Paroxetin (serotonerg), Fluoxetin (serotonerg) oder Reboxetin (adrenerg) können Schlaganfall-Defizite transient verbessern, wie in Placebo-kontrollierten Studien gezeigt werden konnte.[35] Ein neuer technischer Ansatz zur Verbesserung von Ausfällen besteht in der transkraniellen Gleichstrom-Behandlung (transcranial direct current stimulation, tDCS), was derzeit in mehreren Kliniken, unter anderem in Deutschland, überprüft wird.[36]
Siehe auch
Weitere Informationen zu den Symptomen, der Diagnostik und der Therapie finden sich unter:
- Primär ischämischer Hirninfarkt,
- Hirnblutung,
- Subarachnoidalblutung,
- Transitorische ischämische Attacke,
- Stiftung Deutsche Schlaganfall-Hilfe,
- Modifizierte Rankin-Skala als Maß der bleibenden Behinderung nach einem Schlaganfall, und
- European Stroke Conference.
Literatur
- K.-F. Gruber-Gerardy, W. Merz, H. Sonnenberg: Meilensteine aus der Geschichte des Schlaganfalls. Von Apoplexis, Blutegeln und moderner Sekundärprävention. Boehringer Ingelheim, Ingelheim 2005, OCLC 891805882.
- Jörg Braun, Roland Preuss, Klaus Dalhoff: Klinikleitfaden Intensivmedizin. 6. Auflage. Urban & Fischer, München/ Jena 2005, ISBN 3-437-23760-8. (medizinisches Lehrbuch)
- Manio von Maravic: Neurologische Notfälle. In: Jörg Braun, Roland Preuss (Hrsg.): Klinikleitfaden Intensivmedizin. 9. Auflage. Elsevier, München 2016, ISBN 978-3-437-23763-8, S. 311–356, hier: S. 312–324 (Schlaganfall und Stroke Unit).
- Klaus Poeck, Werner Hacke: Neurologie. Mit 85 Tabellen [neue Approbationsordnung], 12. Auflage, Springer, Heidelberg 2006, ISBN 3-540-29997-1. (medizinisches Lehrbuch)
- Patricia M. Davies: Hemiplegie. Ein umfassendes Behandlungskonzept für Patienten nach Schlaganfall und anderen Hirnschädigungen. In: Rehabilitation und Prävention. 2., vollständig überarbeitete Auflage. Springer, Berlin u. a. 2002, ISBN 3-540-41794-X. (Lehrbuch zur krankengymnastischen Rehabilitation nach Schlaganfall)
- Elke Klug: Schlaganfall. Gemeinsam zurück ins Leben. Ein Ratgeber für Angehörige und Freunde. Stiftung Warentest, Berlin 2018, ISBN 978-3-86851-173-4.
Weblinks
- S3-Leitlinie: Schlaganfall, der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF), AWMF-Registernummer 053/011 (Volltext. Stand: 31. Oktober 2012, gültig bis 29. Februar 2016).
- Stiftung Deutsche Schlaganfall-Hilfe.
Einzelnachweise
- ↑ duden.de
- ↑ Irmgard Hort, Axel Karenberg: Überlegungen salernitanischer Magistri zur Apoplexie. In: Würzburger medizinhistorische Mitteilungen. Band 18, 1999, S. 87–92.
- ↑ Gerhard F. Hamann, Mario Siebler, Wolfgang von Scheidt: Schlaganfall: Klinik, Diagnostik, Therapie, Interdisziplinäres Handbuch. ecomed Verlagsgesellschaft, 2002, ISBN 3-609-51990-8.
- ↑ Definition der WHO
- ↑ Manio von Maravic: Neurologische Notfälle. In: Jörg Braun, Roland Preuss (Hrsg.): Klinikleitfaden Intensivmedizin. 9. Auflage. Elsevier, München 2016, ISBN 978-3-437-23763-8, S. 311–356, hier: S. 312–316 (Akute zerebrovaskuläre Erkrankungen).
- ↑ Kommission Leitlinien der Deutschen Gesellschaft für Neurologie: Leitlinien der Deutschen Gesellschaft für Neurologie. 3. Auflage. Georg Thieme, Stuttgart 2005, ISBN 3-13-132413-9.
- ↑ Tabelle "Todesursachenstatistik". Auf: genesis-destatis.de, abgerufen am 1. Juni 2018.
- ↑ E. Rupp: Fortschritte in Behandlung und Diagnostik zentraler neurogener Sprachstörungen. (PDF) Dissertation. Ludwig-Maximilians-Universität München, 2. Juli 2010.
- ↑ Emelia J Benjamin und andere für die "American Heart Association Statistics Committee and Stroke Statistics Subcommittee": Heart Disease and Stroke Statistics—2017 Update. In: Circulation. Band 135, Nr. 10, 7. März 2017, S. e146–e603, doi:10.1161/CIR.0000000000000485.
- ↑ for the GBD 2013 Stroke Panel Experts Group, Gregory A. Roth, Christopher J. L. Murray, Theo Vos, Catherine O. Johnson: Stroke Prevalence, Mortality and Disability-Adjusted Life Years in Adults Aged 20-64 Years in 1990-2013: Data from the Global Burden of Disease 2013 Study. In: Neuroepidemiology. Band 45, Nr. 3, 2015, ISSN 1423-0208, S. 190–202, doi:10.1159/000441098, PMID 26505983 (karger.com [abgerufen am 23. Dezember 2018]).
- ↑ P. L. Kolominsky-Rabas u. a.: A prospective community-based study of stroke in Germany--the Erlangen Stroke Project (ESPro): incidence and case fatality at 1, 3, and 12 months. In: Stroke. 29, 1998, S. 2501–2506. PMID 9836758
- ↑ Kommission Leitlinien der Deutschen Gesellschaft für Neurologie: Leitlinien der Deutschen Gesellschaft für Neurologie. 3. Auflage. Georg Thieme, Stuttgart 2005, ISBN 3-13-132413-9.
- ↑ Clearingbericht „Deutsche Leitlinien zum Schlaganfall“, 2005.
- ↑ Symptome - www.schlaganfall-hilfe.de. Website schlaganfall-hilfe.de. Abgerufen am 29. Mai 2016.
- ↑ M. S. Dittmar, B. Vatankhah, M. Horn: Präklinische neurologische Untersuchung von Schlaganfallpatienten. In: Notarzt. 20(5), 2004, S. 163–167. doi:10.1055/s-2004-828291
- ↑ Illustrierter Test auf der Internetseite der American Stroke Association.
- ↑ schlaganfall-hilfe.de
- ↑ Akuttherapie des ischämischen Schlaganfalls. S1-Leitlinie der DGN, September 2012.
- ↑ Liste von Stroke Units in Deutschland mit einer Zertifizierung seitens der Stiftung Deutsche Schlaganfall-Hilfe
- ↑ Alexandra Jane Oliver: Schlaganfall: Spezial-Rettungswagen beschleunigt Therapie. In: Spiegel Online. 11. April 2012, abgerufen am 12. November 2018.
- ↑ Jeffrey L. Saver: Time to Treatment With Intravenous Tissue Plasminogen Activator and Outcome From Acute Ischemic Stroke. In: JAMA. 309, 2013, S. 2480, doi:10.1001/jama.2013.6959.
- ↑ kurze Patentbeschreibung (Seite nicht mehr abrufbar, festgestellt im Oktober 2018. Suche in Webarchiven) (englisch)
- ↑ www.innovations-report.de
- ↑ Olav Jansen, Präsident der Deutschen Gesellschaft für Neurologische Rehabilitation, Direktor des Instituts für Neuroradiologie am Universitätsklinikum Schleswig-Holstein in Kiel, 2011.
- ↑ Neues Verfahren nach Schlaganfall. Auf: zdf.de, abgerufen am 1. Juni 2018.
- ↑ Die mechanische Thrombektomie: eine Revolution in der Schlaganfalltherapie.
- ↑ A. Kulshreshtha, V. Vaccarino, S. E. Judd, V. J. Howard, W. M. McClellan, P. Muntner, Y. Hong, M. M. Safford, A. Goyal, M. Cushman: Life’s Simple 7 and Risk of Incident Stroke: The Reasons for Geographic and Racial Differences in Stroke Study. In: Stroke. 44, 2013, S. 1909–1914, doi:10.1161/STROKEAHA.111.000352.
- ↑ P. Strazzullo, L. D’Elia, N. B. Kandala, F. P. Cappuccio: Salt intake, stroke, and cardiovascular disease: meta-analysis of prospective studies. In: BMJ (Clinical Research Ed.). Band 339, November 2009, S. b4567, PMID 19934192, PMC 2782060 (freier Volltext).
- ↑ L. D’Elia, G. Barba, F. P. Cappuccio, P. Strazzullo: Potassium intake, stroke, and cardiovascular disease a meta-analysis of prospective studies. In: Journal of the American College of Cardiology. Band 57, Nr. 10, März 2011, S. 1210–1219, doi:10.1016/j.jacc.2010.09.070, PMID 21371638.
- ↑ Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM): Leitlinien Schlaganfall. (PDF) Abgerufen am 27. Dezember 2013.
- ↑ E. Taub, G. Uswatte, R. Pidikiti: Constraint-Induced Movement Therapy: a new family of techniques with broad application to physical rehabilitation--a clinical review. In: J Rehabil Res Dev. 6 (3), Jul 1999, S. 237–251.
- ↑ W. H. R. Miltner, E. Taub, H. Bauder: Behandlung motorischer Störungen nach Schlaganfall – Die Taubsche Bewegungsindikation. Hogrefe, Göttingen 2001, ISBN 3-8017-1464-0.
- ↑ E. Rupp, S. Sünderhauf, J. Tesak: Teletherapie in der Behandlung von Aphasie. In: Aphasie und verwandte Gebiete. Nr. 2, 2008, Internetabruf: 17. Juli 2018 (docplayer.org)/
- ↑ D. A. Nowak, C. Grefkes, G. R. Fink: Modern neurophysiological strategies in the rehabilitation of impaired hand function following stroke. In: Fortschr Neurol Psychiatr. 76(6), Jun 2008, S. 354–360.
- ↑ J. Pariente, I. Loubinoux, C. Carel, J. F. Albucher, A. Leger, C. Manelfe, O. Rascol, F. Chollet: Fluoxetine modulates motor performance and cerebral activation of patients recovering from stroke. In: Ann Neurol. 50 (6), Dez 2001, S. 718–729.
- ↑ F. C. Hummel, B. Voller, P. Celnik, A. Floel, P. Giraux, C. Gerloff, L. G. Cohen: Effects of brain polarization on reaction times and pinch force in chronic stroke. In: BMC Neurosci. 7, 3. Nov 2006, S. 73.