„Herdenschutz (Epidemiologie)“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Aka (Diskussion | Beiträge) K Abkürzung korrigiert |
Ghilt (Diskussion | Beiträge) Schutz gefährdeter Personengruppen |
||
| Zeile 2: | Zeile 2: | ||
[[Datei:Herd immunity.svg|lang=de|mini|hochkant=1.5|Ausbreitung ansteckender Krankheiten in Bevölkerungen mit unterschiedlicher Impfrate.]] |
[[Datei:Herd immunity.svg|lang=de|mini|hochkant=1.5|Ausbreitung ansteckender Krankheiten in Bevölkerungen mit unterschiedlicher Impfrate.]] |
||
Unter '''Herdenimmunität''' (vom engl. ''herd immunity'', vereinzelt übersetzt mit ''Herdimmunität'') werden unterschiedliche Konzepte zur kollektiven immunologischen Wirkung von Infekten und Impfungen verstanden.<ref name="Fine_2011_Rough-Guide">[ https://doi.org/10.1093/cid/cir007 Paul Fine u. a.: “Herd Immunity”: A Rough Guide], Clinical Infectious Diseases,Band 52, Ausgabe 7, 1. April 2011, Seiten 911–916</ref> Weit verbreitet ist die Version, dass Herdenimmunität den Anteil einer [[Population (Biologie)|Population]] bezeichnet, der gegenüber bestimmten übertragbaren [[Infektionskrankheit]]en [[Immunität (Medizin)|immun]] ist.<ref name="Kim">T. H. Kim, J. Johnstone, M. Loeb: ''Vaccine herd effect.'' In: ''Scandinavian journal of infectious diseases.'' Band 43, Nummer 9, September 2011, S. 683–689, {{DOI|10.3109/00365548.2011.582247}}, PMID 21604922, {{PMC|3171704}}.</ref><ref name="John">T. J. John, R. Samuel: ''Herd immunity and herd effect: new insights and definitions.'' In: ''Eur. J. Epidemiol.'', 2000, 16, 7., S. 601–606, PMID 11078115</ref> Nach einigen Autoren ist dies [[synonym]] mit, nach anderen abzugrenzen gegen den Begriff '''Herdeneffekt''',<ref name="Kim" /><ref name="John" /> bei dem die durch [[Impfung]] erzeugte oder durch [[Infektion]] erworbene Immunität gegen einen [[Krankheitserreger]] innerhalb einer Population (der „Herde“) so verbreitet ist, dass in der Population auch nicht-immune Individuen geschützt sind, weil in der Regel die [[Infektkette]] unterbrochen wird und der Erreger sich nicht ausbreiten kann. |
Unter '''Herdenimmunität''' (vom engl. ''herd immunity'', vereinzelt übersetzt mit ''Herdimmunität'') werden unterschiedliche Konzepte zur kollektiven immunologischen Wirkung von Infekten und Impfungen verstanden.<ref name="Fine_2011_Rough-Guide">[ https://doi.org/10.1093/cid/cir007 Paul Fine u. a.: “Herd Immunity”: A Rough Guide], Clinical Infectious Diseases,Band 52, Ausgabe 7, 1. April 2011, Seiten 911–916</ref> Weit verbreitet ist die Version, dass Herdenimmunität den Anteil einer [[Population (Biologie)|Population]] bezeichnet, der gegenüber bestimmten übertragbaren [[Infektionskrankheit]]en [[Immunität (Medizin)|immun]] ist.<ref name="Kim">T. H. Kim, J. Johnstone, M. Loeb: ''Vaccine herd effect.'' In: ''Scandinavian journal of infectious diseases.'' Band 43, Nummer 9, September 2011, S. 683–689, {{DOI|10.3109/00365548.2011.582247}}, PMID 21604922, {{PMC|3171704}}.</ref><ref name="John">T. J. John, R. Samuel: ''Herd immunity and herd effect: new insights and definitions.'' In: ''Eur. J. Epidemiol.'', 2000, 16, 7., S. 601–606, PMID 11078115</ref> Nach einigen Autoren ist dies [[synonym]] mit, nach anderen abzugrenzen gegen den Begriff '''Herdeneffekt''',<ref name="Kim" /><ref name="John" /> bei dem die durch [[Impfung]] erzeugte oder durch [[Infektion]] erworbene Immunität gegen einen [[Krankheitserreger]] innerhalb einer Population (der „Herde“) so verbreitet ist, dass in der Population auch nicht-immune Individuen geschützt sind, weil in der Regel die [[Infektkette]] unterbrochen wird und der Erreger sich nicht ausbreiten kann. |
||
| ⚫ | Besondere Bedeutung besitzt die Herdenimmunität für Personen, die nicht geimpft werden können, beispielsweise Personen mit [[Immunsuppression]] (Erkrankung des Immunsystems wie [[HIV]]-Infektion, [[Lymphom]], [[Knochenmarkkrebs]] oder [[Leukämie]]; [[Chemotherapie]] oder [[Strahlentherapie]]; Einnahme von [[Immunsuppressiva]] nach Organtransplantation),<ref name=pmid24868544>S. Cesaro, M. Giacchino, F. Fioredda, A. Barone, L. Battisti, S. Bezzio, S. Frenos, R. De Santis, S. Livadiotti, S. Marinello, A. G. Zanazzo, D. Caselli: ''Guidelines on vaccinations in paediatric haematology and oncology patients.'' In: ''BioMed research international.'' Band 2014, 2014, S. 707691, {{DOI|10.1155/2014/707691}}, PMID 24868544, {{PMC|4020520}}</ref><ref name=pmid22773718 >R. M. Wolfe: ''Update on adult immunizations.'' In: ''Journal of the American Board of Family Medicine : JABFM.'' Band 25, Nummer 4, 2012 Jul-Aug, S. 496–510, {{DOI|10.3122/jabfm.2012.04.100274}}, PMID 22773718</ref> oder Neugeborene, die noch nicht geimpft werden konnten.<ref name="Smallpox"> {{Webarchiv|text=''History and Epidemiology of Global Smallpox Eradication''. |url=http://www.bt.cdc.gov/agent/smallpox/training/overview/pdf/eradicationhistory.pdf |wayback=20070715234749 |archiv-bot=2018-04-14 17:39:27 InternetArchiveBot }} (PDF; 1,5 MB) From the training course ''Smallpox: Disease, Prevention, and Intervention''. [[Centers for Disease Control and Prevention|CDC]] and [[World Health Organization|WHO]]. Slide 16-17.</ref><ref name=pmid24868544 /><ref name=pmid23910028 >F. M. Munoz: ''Maternal immunization: an update for pediatricians.'' In: ''Pediatric annals.'' Band 42, Nummer 8, August 2013, S. 153–158, {{DOI|10.3928/00904481-20130723-09}}, PMID 23910028.</ref> Bei Neugeborenen können Nebenwirkungen oder eine Unwirksamkeit durch [[passive Immunität]] von den [[Antikörper]]n der Mutter Gründe gegen die Verabreichung einzelner Impfstoffe sein.<ref>''General recommendations on immunization –- recommendations of the Advisory Committee on Immunization Practices (ACIP).'' In: ''MMWR. Recommendations and reports : Morbidity and mortality weekly report. Recommendations and reports.'' Band 60, Nummer 2, Januar 2011, S. 1–64, PMID 21293327.</ref> Bei Menschen mit Immundefekten kann eine Impfung nicht die gewünschte Immunität erzeugen.<ref>S. Esposito, S. Bosis, L. Morlacchi, E. Baggi, C. Sabatini, N. Principi: ''Can infants be protected by means of maternal vaccination?'' In: ''Clinical microbiology and infection : the official publication of the European Society of Clinical Microbiology and Infectious Diseases.'' Band 18 Suppl 5, Oktober 2012, S. 85–92, {{DOI|10.1111/j.1469-0691.2012.03936.x}}, PMID 22862749</ref><ref name=rakel2 >{{cite book|last1=Rakel|first1=D.|last2=Rakel|first2=R. E.|year=2015|title=Textbook of Family Medicine|url=https://books.google.com/books?id=8huMBgAAQBAJ&pg=PA99&pg=PA99#v=onepage&q&f=false|publisher=Elsevier Health Sciences|pages=99, 187|isbn=978-0323313087|accessdate=30 March 2015}}</ref> Daneben können [[Kontraindikation]]en zu einer mangelnden Immunität beitragen.<ref name=pmid24868544 /> Diese Gruppen sind auf einen |
||
== Eigenschaften == |
== Eigenschaften == |
||
| ⚫ | Der Herdeneffekt wirkt ähnlich wie eine [[Brandschneise]] bei einem Feuer, indem die Infektionskette eines Krankheitserregers mittels Impfungen unterbrochen oder mindestens verlangsamt wird. In der Folge kann sich die Krankheit nicht mehr [[Epidemie|epidemisch]] ausbreiten, insofern die Krankheitserreger nur zwischen Menschen übertragen werden ([[Anthroponose]]). Bei Krankheitserregern mit Rückzugsräumen, beispielsweise dem in der Erde vorkommenden [[Bakterium]] ''[[Clostridium tetani]]'' als Auslöser von [[Tetanus]] oder beim von [[Gemeiner Holzbock|Zecken]] auch auf andere Säugetiere übertragenen [[FSME-Virus]], kann eine Herdenimmunität nicht erreicht werden. Schutz vor diesen Krankheiten gibt nur die individuelle Prophylaxe.<ref name="Fine">P. Fine: ''Herd immunity: history, theory, practice''. In: ''Epidemiol Rev'', 15, 2, 1993, S. 265–302. PMID 8174658.</ref> |
||
| ⚫ | Über einem bestimmten Schwellenwert der Immunität in einer Bevölkerung bricht die Population des Krankheitserregers mangels Vermehrung zusammen und die Krankheit kann in dieser Bevölkerung nicht mehr zirkulieren. Dieser Schwellenwert ist im Wesentlichen abhängig von der [[Basisreproduktionszahl]] des jeweiligen Krankheitserregers. Falls der Krankheitserreger Rückzugsräume in anderen Populationen hat, kann er nicht mehr von diesen Rückzugsräumen aus Populationen mit ausreichender Herdenimmunität infizieren. |
||
| ⚫ | |||
| ⚫ | |||
{| class="wikitable" style="float:right; font-size:85%; margin-left:15px; text-align:center;" |
{| class="wikitable" style="float:right; font-size:85%; margin-left:15px; text-align:center;" |
||
|+ '''Für den Herdeneffekt nötiger Mindestanteil Immunisierter<br /> bei einer Auswahl von durch Impfung verhinderbaren Krankheiten<br />(mathematisches Modell für ideale Bedingungen)'''<ref name="Smallpox" /> |
|+ '''Für den Herdeneffekt nötiger Mindestanteil Immunisierter<br /> bei einer Auswahl von durch Impfung verhinderbaren Krankheiten<br />(mathematisches Modell für ideale Bedingungen)'''<ref name="Smallpox" /> |
||
| Zeile 31: | Zeile 21: | ||
|colspan="4" | <small>Die [[Basisreproduktionszahl]] R<sub>0</sub> gibt an, wie viele weitere Personen eine infizierte Person ansteckt,<br /> falls die sie umgebende Population oder Subpopulation weder geimpft noch anderweitig vor Infektionen geschützt wird.</small> |
|colspan="4" | <small>Die [[Basisreproduktionszahl]] R<sub>0</sub> gibt an, wie viele weitere Personen eine infizierte Person ansteckt,<br /> falls die sie umgebende Population oder Subpopulation weder geimpft noch anderweitig vor Infektionen geschützt wird.</small> |
||
|} |
|} |
||
| ⚫ | Der Herdeneffekt wirkt ähnlich wie eine [[Brandschneise]] bei einem Feuer, indem die Infektionskette eines Krankheitserregers mittels Impfungen unterbrochen oder mindestens verlangsamt wird. In der Folge kann sich die Krankheit nicht mehr [[Epidemie|epidemisch]] ausbreiten, insofern die Krankheitserreger nur zwischen Menschen übertragen werden ([[Anthroponose]]). Bei Krankheitserregern mit Rückzugsräumen, beispielsweise dem in der Erde vorkommenden [[Bakterium]] ''[[Clostridium tetani]]'' als Auslöser von [[Tetanus]] oder beim von [[Gemeiner Holzbock|Zecken]] auch auf andere Säugetiere übertragenen [[FSME-Virus]], kann eine Herdenimmunität nicht erreicht werden. Schutz vor diesen Krankheiten gibt nur die individuelle Prophylaxe.<ref name="Fine">P. Fine: ''Herd immunity: history, theory, practice''. In: ''Epidemiol Rev'', 15, 2, 1993, S. 265–302. PMID 8174658.</ref> |
||
| ⚫ | Über einem bestimmten Schwellenwert der Immunität in einer Bevölkerung bricht die Population des Krankheitserregers mangels Vermehrung zusammen und die Krankheit kann in dieser Bevölkerung nicht mehr zirkulieren. Dieser Schwellenwert ist im Wesentlichen abhängig von der [[Basisreproduktionszahl]] des jeweiligen Krankheitserregers. Falls der Krankheitserreger Rückzugsräume in anderen Populationen hat, kann er nicht mehr von diesen Rückzugsräumen aus Populationen mit ausreichender Herdenimmunität infizieren. |
||
| ⚫ | |||
| ⚫ | |||
== Schutz gefährdeter Personengruppen == |
|||
| ⚫ | Besondere Bedeutung besitzt die Herdenimmunität für Personen, die nicht geimpft werden können, beispielsweise Personen mit [[Immunsuppression]] (Erkrankung des Immunsystems wie [[HIV]]-Infektion, [[Lymphom]], [[Knochenmarkkrebs]] oder [[Leukämie]]; [[Chemotherapie]] oder [[Strahlentherapie]]; Einnahme von [[Immunsuppressiva]] nach Organtransplantation),<ref name=pmid24868544>S. Cesaro, M. Giacchino, F. Fioredda, A. Barone, L. Battisti, S. Bezzio, S. Frenos, R. De Santis, S. Livadiotti, S. Marinello, A. G. Zanazzo, D. Caselli: ''Guidelines on vaccinations in paediatric haematology and oncology patients.'' In: ''BioMed research international.'' Band 2014, 2014, S. 707691, {{DOI|10.1155/2014/707691}}, PMID 24868544, {{PMC|4020520}}</ref><ref name=pmid22773718 >R. M. Wolfe: ''Update on adult immunizations.'' In: ''Journal of the American Board of Family Medicine : JABFM.'' Band 25, Nummer 4, 2012 Jul-Aug, S. 496–510, {{DOI|10.3122/jabfm.2012.04.100274}}, PMID 22773718</ref> oder Neugeborene, die noch nicht geimpft werden konnten.<ref name="Smallpox"> {{Webarchiv|text=''History and Epidemiology of Global Smallpox Eradication''. |url=http://www.bt.cdc.gov/agent/smallpox/training/overview/pdf/eradicationhistory.pdf |wayback=20070715234749 |archiv-bot=2018-04-14 17:39:27 InternetArchiveBot }} (PDF; 1,5 MB) From the training course ''Smallpox: Disease, Prevention, and Intervention''. [[Centers for Disease Control and Prevention|CDC]] and [[World Health Organization|WHO]]. Slide 16-17.</ref><ref name=pmid24868544 /><ref name=pmid23910028 >F. M. Munoz: ''Maternal immunization: an update for pediatricians.'' In: ''Pediatric annals.'' Band 42, Nummer 8, August 2013, S. 153–158, {{DOI|10.3928/00904481-20130723-09}}, PMID 23910028.</ref> Bei Neugeborenen können Nebenwirkungen oder eine Unwirksamkeit durch [[passive Immunität]] von den [[Antikörper]]n der Mutter Gründe gegen die Verabreichung einzelner Impfstoffe sein.<ref>''General recommendations on immunization –- recommendations of the Advisory Committee on Immunization Practices (ACIP).'' In: ''MMWR. Recommendations and reports : Morbidity and mortality weekly report. Recommendations and reports.'' Band 60, Nummer 2, Januar 2011, S. 1–64, PMID 21293327.</ref> Bei Menschen mit Immundefekten kann eine Impfung nicht die gewünschte Immunität erzeugen.<ref>S. Esposito, S. Bosis, L. Morlacchi, E. Baggi, C. Sabatini, N. Principi: ''Can infants be protected by means of maternal vaccination?'' In: ''Clinical microbiology and infection : the official publication of the European Society of Clinical Microbiology and Infectious Diseases.'' Band 18 Suppl 5, Oktober 2012, S. 85–92, {{DOI|10.1111/j.1469-0691.2012.03936.x}}, PMID 22862749</ref><ref name=rakel2 >{{cite book|last1=Rakel|first1=D.|last2=Rakel|first2=R. E.|year=2015|title=Textbook of Family Medicine|url=https://books.google.com/books?id=8huMBgAAQBAJ&pg=PA99&pg=PA99#v=onepage&q&f=false|publisher=Elsevier Health Sciences|pages=99, 187|isbn=978-0323313087|accessdate=30 March 2015}}</ref> Daneben können [[Kontraindikation]]en zu einer mangelnden Immunität beitragen.<ref name=pmid24868544 /> Diese Gruppen sind auf einen Herdeneffekt angewiesen.<ref name=pmid24868544 /><ref name=rakel2 /><ref name=tulvar >{{cite book|last1=Tulchinsky|first1=T. H.|last2=Varavikova|first2=E. A.|date=26 March 2014|title=The New Public Health: An Introduction for the 21st Century|url=https://books.google.com/books?id=2hg2IxB9WngC&pg=PA163&pg=PA163#v=onepage&q&f=false|publisher=Academic Press|pages=163–82|isbn=978-0124157675|accessdate=30 March 2015}}</ref> Zusätzlich zur fehlenden Immunität in diesen Personengruppen kann eine Infektion teilweise auch zu schwereren Krankheitsverläufen führen, die durch einen Herdeneffekt vermieden werden könnten.<ref name=pmid24868544 /><ref name=rakel2 /><ref name=tulvar >{{cite book|last1=Tulchinsky|first1=T. H.|last2=Varavikova|first2=E. A.|date=26 March 2014|title=The New Public Health: An Introduction for the 21st Century|url=https://books.google.com/books?id=2hg2IxB9WngC&pg=PA163&pg=PA163#v=onepage&q&f=false|publisher=Academic Press|pages=163–82|isbn=978-0124157675|accessdate=30 March 2015}}</ref> |
||
Ein Herdeneffekt für einen Krankheitserreger, der nur in einer [[Altersgruppe]] vorkommt, kann auch Personen in anderen Altersgruppen vor Erkrankung an diesem Krankheitserreger schützen,<ref name="Kim" /> beispielsweise kann eine ausreichende Herdenimmunität auch ungeimpfte Säuglinge und Kleinkinder<ref name="Kim" /><ref name=rakel2 /><ref name=pmid22862432 >{{Cite journal | pmid = 22862432| year = 2012| last1 = Pittet| first1 = L. F.| title = Pneumococcal vaccines for children: A global public health priority| journal = Clinical Microbiology and Infection| volume = 18 Suppl 5| pages = 25–36| last2 = Posfay-Barbe| first2 = K. M.| doi = 10.1111/j.1469-0691.2012.03938.x}}</ref><ref>{{Cite journal | pmid = 24088009| year = 2013| last1 = Nakagomi| first1 = O| title = Incorporation of a rotavirus vaccine into the national immunisation schedule in the United Kingdom: A review| journal = Expert Opinion on Biological Therapy| volume = 13| issue = 11| pages = 1613–21| last2 = Iturriza-Gomara| first2 = M| last3 = Nakagomi| first3 = T| last4 = Cunliffe| first4 = N. A.| doi = 10.1517/14712598.2013.840285}}</ref><ref>{{Cite journal | pmid = 22749491| year = 2012| last1 = Lopman| first1 = B. A.| title = Post-licensure experience with rotavirus vaccination in high and middle income countries; 2006 to 2011| journal = Current Opinion in Virology| volume = 2| issue = 4| pages = 434–42| last2 = Payne| first2 = D. C.| last3 = Tate| first3 = J. E.| last4 = Patel| first4 = M. M.| last5 = Cortese| first5 = M. M.| last6 = Parashar| first6 = U. D.| doi = 10.1016/j.coviro.2012.05.002| url = https://zenodo.org/record/1258865}}</ref> oder ältere Menschen vor Erkrankung schützen.<ref name="Kim" /><ref name=pmid25003085 >{{Cite journal | pmid = 25003085| pmc = 4083064| year = 2014| last1 = Kim| first1 = T. H.| title = Seasonal influenza and vaccine herd effect| journal = Clinical and Experimental Vaccine Research| volume = 3| issue = 2| pages = 128–32| doi = 10.7774/cevr.2014.3.2.128}}</ref> Bei [[Geschlechtskrankheit]]en erstreckt sich ein Herdeneffekt von einem Geschlecht auf das andere Geschlecht,<ref name=pmid15627236>G. P. Garnett: ''Role of herd immunity in determining the effect of vaccines against sexually transmitted disease.'' In: ''[[The Journal of Infectious Diseases]].'' Band 191 Suppl 1, Februar 2005, S. S97–106, {{DOI|10.1086/425271}}, PMID 15627236.</ref><ref name=pmid22219162 >{{Cite journal | pmid = 22219162| pmc = 3285475| year = 2012| last1 = Lowy| first1 = D. R.| title = Reducing HPV-associated cancer globally| journal = Cancer Prevention Research| volume = 5| issue = 1| pages = 18–23| last2 = Schiller| first2 = J. T.| doi = 10.1158/1940-6207.CAPR-11-0542}}</ref><ref name=pmid23391351 >{{Cite journal | pmid = 23391351| pmc = 3642007| year = 2013| last1 = Lenzi| first1 = A| title = Rome Consensus Conference – statement; human papilloma virus diseases in males| journal = BMC Public Health| volume = 13| pages = 117| last2 = Mirone| first2 = V| last3 = Gentile| first3 = V| last4 = Bartoletti| first4 = R| last5 = Ficarra| first5 = V| last6 = Foresta| first6 = C| last7 = Mariani| first7 = L| last8 = Mazzoli| first8 = S| last9 = Parisi| first9 = S. G.| last10 = Perino| first10 = A| last11 = Picardo| first11 = M| last12 = Zotti| first12 = C. M.| doi = 10.1186/1471-2458-13-117}}</ref><ref name=pmid21962468 >{{Cite journal | pmid = 21962468| year = 2011| last1 = Garland| first1 = S. M.| title = Adolescent and young adult HPV vaccination in Australia: Achievements and challenges| journal = Preventive Medicine| volume = 53 Suppl 1| pages = S29–35| last2 = Skinner| first2 = S. R.| last3 = Brotherton| first3 = J. M.| doi = 10.1016/j.ypmed.2011.08.015}}</ref> mit Ausnahme von Geschlechtskrankheiten bei [[Homosexuell]]en.<ref name=pmid23391351 /> Hochrisikoverhalten beim Geschlechtsverkehr erschwert die Eradikation von Geschlechtskrankheiten,<ref name=pmid15627236 /> wodurch eine Impfung in dieser Personengruppe mit hoher [[Transmission (Medizin)|Übertragungsrate]] vermutlich für einen Herdeneffekt notwendig ist.<ref name=pmid15627236 /><ref name=pmid23391351 /> |
|||
== Eradikation == |
== Eradikation == |
||
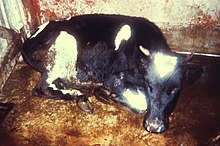
[[Datei:Rinderpest milk fever.jpg|mini|Kuh mit [[Rinderpest]] (1982). Der letzte bekannte Fall war in [[Kenya]] 2001. Die Krankheit wurde 2011 als ausgerottet deklariert.<ref>F. Njeumi, W. Taylor, A. Diallo, K. Miyagishima, P. P. Pastoret, B. Vallat, M. Traore: ''The long journey: a brief review of the eradication of rinderpest.'' In: ''Revue scientifique et technique.'' Band 31, Nummer 3, Dezember 2012, S. 729–746, {{DOI|10.20506/rst.31.3.2157}}, PMID 23520729.</ref>]] |
[[Datei:Rinderpest milk fever.jpg|mini|Kuh mit [[Rinderpest]] (1982). Der letzte bekannte Fall war in [[Kenya]] 2001. Die Krankheit wurde 2011 als ausgerottet deklariert.<ref>F. Njeumi, W. Taylor, A. Diallo, K. Miyagishima, P. P. Pastoret, B. Vallat, M. Traore: ''The long journey: a brief review of the eradication of rinderpest.'' In: ''Revue scientifique et technique.'' Band 31, Nummer 3, Dezember 2012, S. 729–746, {{DOI|10.20506/rst.31.3.2157}}, PMID 23520729.</ref>]] |
||
Im günstigsten Fall kann eine Krankheit so durch ausreichend hohe Impfraten in einer Bevölkerung sogar ausgerottet ([[Eradikation]]) werden, d. h. der Krankheitserreger kommt endemisch nicht mehr vor. Die Eradikation von Infektionskrankheiten ist ein Ziel der [[Gesundheitspolitik]].<ref |
Im günstigsten Fall kann eine Krankheit so durch ausreichend hohe Impfraten in einer Bevölkerung sogar ausgerottet ([[Eradikation]]) werden, d. h. der Krankheitserreger kommt endemisch nicht mehr vor. Die Eradikation von Infektionskrankheiten ist ein Ziel der [[Gesundheitspolitik]].<ref name="Kim" /> Bei den [[Pocken]] konnte genau dies durch ein konsequentes, weltweites Impf- und Bekämpfungsprogramm erreicht werden, so dass 1980 die Welt von der WHO für pockenfrei erklärt werden konnte.<ref>F. Fenner: ''The global eradication of smallpox.'' In: ''Med J Aust.'', 1980 Mai 17,1(10), S. 455. PMID 7412674</ref> Gleiches wurde global inzwischen für [[Polio]] nahezu erreicht – inzwischen gelten nur noch wenige Länder als endemisch für Polioviren ([[Nigeria]], [[Indien]], [[Pakistan]], [[Afghanistan]]).<ref>[http://www.eurosurveillance.org/ViewArticle.aspx?ArticleId=19178 ''Polio situation worldwide in 2008 - update on the progress towards global eradication''.] In: ''[[Eurosurveillance (Zeitschrift)|Eurosurveillance]]'', 2009 Apr 16;14(15), pii: 19178. PMID 19371512</ref> Bei nachlassenden Impfbemühungen in den Nachbarländern kommt es jedoch immer wieder zu Ausbrüchen der Poliomyelitis durch Re-Importe, zuletzt 2006 in [[Namibia]].<ref>Weltgesundheitsorganisation: [http://www.who.int/csr/don/2006_06_07/en/index.html ''Poliomyelitis in Namibia''.] In: WHO – Disease Outbreak News, 6. Juni 2006</ref> Die globale Eliminierung der Masern, ebenfalls von der WHO als Ziel vorgegeben, konnte jedoch bislang nur auf den Kontinenten Amerika und Australien sowie in Skandinavien erreicht werden, da im Rest der Welt die Durchimpfungsraten zu gering sind. In der Folge brechen immer wieder lokale Masernepidemien aus, auch beispielsweise in Deutschland die regional begrenzten Masernepidemien in Hessen, Bayern, Baden-Württemberg und Nordrhein-Westfalen inklusive schwerer Komplikationen und Todesfälle in den Jahren 2005/2006.<ref name="rki_masern">[http://edoc.rki.de/documents/rki_fv/rebX9rKkzYgIQ/PDF/2614gZ347n8OCg2.pdf ''Masern im Jahr 2005 und Ausbrüche in Baden-Württemberg und Nordrhein-Westfalen in der ersten Hälfte des Jahres 2006''.] (PDF) [[Robert Koch-Institut]]: ''Epidemiologisches Bulletin'', Nr. 27, 7. Juli 2006.</ref> |
||
== Probleme == |
== Probleme == |
||
Version vom 16. Oktober 2019, 22:54 Uhr
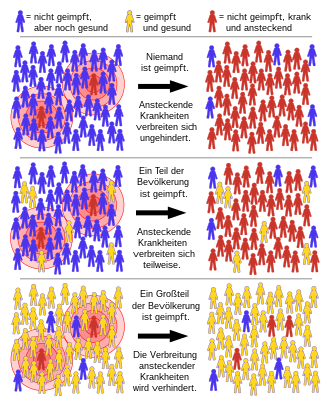
Unter Herdenimmunität (vom engl. herd immunity, vereinzelt übersetzt mit Herdimmunität) werden unterschiedliche Konzepte zur kollektiven immunologischen Wirkung von Infekten und Impfungen verstanden.[1] Weit verbreitet ist die Version, dass Herdenimmunität den Anteil einer Population bezeichnet, der gegenüber bestimmten übertragbaren Infektionskrankheiten immun ist.[2][3] Nach einigen Autoren ist dies synonym mit, nach anderen abzugrenzen gegen den Begriff Herdeneffekt,[2][3] bei dem die durch Impfung erzeugte oder durch Infektion erworbene Immunität gegen einen Krankheitserreger innerhalb einer Population (der „Herde“) so verbreitet ist, dass in der Population auch nicht-immune Individuen geschützt sind, weil in der Regel die Infektkette unterbrochen wird und der Erreger sich nicht ausbreiten kann.
Eigenschaften
| Krankheit | Übertragungsweg | R0 | Mindestanteil Immunisierter |
|---|---|---|---|
| Masern | Tröpfcheninfektion | 12–18 | 83–94 % |
| Mumps | Tröpfcheninfektion | 4–7 | 75–86 % |
| Polio | fäkal-orale Infektion | 5–7 | 80–86 % |
| Röteln | Tröpfcheninfektion | 5–7 | 80–85 % |
| Pocken | Tröpfcheninfektion | 6–7 | 83–85 % |
| Die Basisreproduktionszahl R0 gibt an, wie viele weitere Personen eine infizierte Person ansteckt, falls die sie umgebende Population oder Subpopulation weder geimpft noch anderweitig vor Infektionen geschützt wird. | |||
Der Herdeneffekt wirkt ähnlich wie eine Brandschneise bei einem Feuer, indem die Infektionskette eines Krankheitserregers mittels Impfungen unterbrochen oder mindestens verlangsamt wird. In der Folge kann sich die Krankheit nicht mehr epidemisch ausbreiten, insofern die Krankheitserreger nur zwischen Menschen übertragen werden (Anthroponose). Bei Krankheitserregern mit Rückzugsräumen, beispielsweise dem in der Erde vorkommenden Bakterium Clostridium tetani als Auslöser von Tetanus oder beim von Zecken auch auf andere Säugetiere übertragenen FSME-Virus, kann eine Herdenimmunität nicht erreicht werden. Schutz vor diesen Krankheiten gibt nur die individuelle Prophylaxe.[5]
Über einem bestimmten Schwellenwert der Immunität in einer Bevölkerung bricht die Population des Krankheitserregers mangels Vermehrung zusammen und die Krankheit kann in dieser Bevölkerung nicht mehr zirkulieren. Dieser Schwellenwert ist im Wesentlichen abhängig von der Basisreproduktionszahl des jeweiligen Krankheitserregers. Falls der Krankheitserreger Rückzugsräume in anderen Populationen hat, kann er nicht mehr von diesen Rückzugsräumen aus Populationen mit ausreichender Herdenimmunität infizieren.
Die für einen Herdeneffekt notwendige minimale Herdenimmunität wird aus der Basisreproduktionszahl berechnet:[6]
Schutz gefährdeter Personengruppen
Besondere Bedeutung besitzt die Herdenimmunität für Personen, die nicht geimpft werden können, beispielsweise Personen mit Immunsuppression (Erkrankung des Immunsystems wie HIV-Infektion, Lymphom, Knochenmarkkrebs oder Leukämie; Chemotherapie oder Strahlentherapie; Einnahme von Immunsuppressiva nach Organtransplantation),[7][8] oder Neugeborene, die noch nicht geimpft werden konnten.[4][7][9] Bei Neugeborenen können Nebenwirkungen oder eine Unwirksamkeit durch passive Immunität von den Antikörpern der Mutter Gründe gegen die Verabreichung einzelner Impfstoffe sein.[10] Bei Menschen mit Immundefekten kann eine Impfung nicht die gewünschte Immunität erzeugen.[11][12] Daneben können Kontraindikationen zu einer mangelnden Immunität beitragen.[7] Diese Gruppen sind auf einen Herdeneffekt angewiesen.[7][12][13] Zusätzlich zur fehlenden Immunität in diesen Personengruppen kann eine Infektion teilweise auch zu schwereren Krankheitsverläufen führen, die durch einen Herdeneffekt vermieden werden könnten.[7][12][13]
Ein Herdeneffekt für einen Krankheitserreger, der nur in einer Altersgruppe vorkommt, kann auch Personen in anderen Altersgruppen vor Erkrankung an diesem Krankheitserreger schützen,[2] beispielsweise kann eine ausreichende Herdenimmunität auch ungeimpfte Säuglinge und Kleinkinder[2][12][14][15][16] oder ältere Menschen vor Erkrankung schützen.[2][17] Bei Geschlechtskrankheiten erstreckt sich ein Herdeneffekt von einem Geschlecht auf das andere Geschlecht,[18][19][20][21] mit Ausnahme von Geschlechtskrankheiten bei Homosexuellen.[20] Hochrisikoverhalten beim Geschlechtsverkehr erschwert die Eradikation von Geschlechtskrankheiten,[18] wodurch eine Impfung in dieser Personengruppe mit hoher Übertragungsrate vermutlich für einen Herdeneffekt notwendig ist.[18][20]
Eradikation
Im günstigsten Fall kann eine Krankheit so durch ausreichend hohe Impfraten in einer Bevölkerung sogar ausgerottet (Eradikation) werden, d. h. der Krankheitserreger kommt endemisch nicht mehr vor. Die Eradikation von Infektionskrankheiten ist ein Ziel der Gesundheitspolitik.[2] Bei den Pocken konnte genau dies durch ein konsequentes, weltweites Impf- und Bekämpfungsprogramm erreicht werden, so dass 1980 die Welt von der WHO für pockenfrei erklärt werden konnte.[23] Gleiches wurde global inzwischen für Polio nahezu erreicht – inzwischen gelten nur noch wenige Länder als endemisch für Polioviren (Nigeria, Indien, Pakistan, Afghanistan).[24] Bei nachlassenden Impfbemühungen in den Nachbarländern kommt es jedoch immer wieder zu Ausbrüchen der Poliomyelitis durch Re-Importe, zuletzt 2006 in Namibia.[25] Die globale Eliminierung der Masern, ebenfalls von der WHO als Ziel vorgegeben, konnte jedoch bislang nur auf den Kontinenten Amerika und Australien sowie in Skandinavien erreicht werden, da im Rest der Welt die Durchimpfungsraten zu gering sind. In der Folge brechen immer wieder lokale Masernepidemien aus, auch beispielsweise in Deutschland die regional begrenzten Masernepidemien in Hessen, Bayern, Baden-Württemberg und Nordrhein-Westfalen inklusive schwerer Komplikationen und Todesfälle in den Jahren 2005/2006.[26]
Probleme
Eine Gefahr für die Herdenimmunität stellt insbesondere die Impfmüdigkeit dar. Impfkampagnen, die die notwendige Herdenimmunität nicht erreichen, können unter Umständen die Häufigkeit von Krankheitskomplikationen bei Nicht-Geimpften erhöhen. Wird ein zu geringer Anteil der Bevölkerung geimpft, senkt dies „nur“ die Wahrscheinlichkeit einer Ansteckung bei den Nicht-Geimpften, statt eine Infektion über die Herdenimmunität zu verhindern. Dies bedeutet, dass die Ansteckung, falls sie dann stattfindet, oft nicht mehr im Kindesalter erfolgt, was bei einigen Krankheiten, wie etwa Mumps, Röteln, Polio, Windpocken, gefährlicher ist. Beispielsweise wurde in Griechenland in den frühen 1990er Jahren von einer Zunahme der Fälle von Rötelnembryofetopathie berichtet, nachdem in den gesamten 1980er Jahren die Durchimpfungsrate unter 50 % lag.[27] Aus diesem Grund sollte jede Impfkampagne nicht nur einen Teilschutz der Bevölkerung anstreben, sondern auch die Herdenimmunität sicherstellen. Auch ist es wichtig, dass die Verantwortlichen, welche Impfkampagnen planen, mathematische und epidemiologische Modelle der Medizin verstehen.[28] Aufklärung über den Herdeneffekt kann die Impfmüdigkeit senken.[29] Bei Polio wird die Eradikation durch politisch bedingte Unruhen und Misstrauen gegenüber der modernen Medizin verzögert.[30][31] Eine Impfpflicht könnte die Eradikation beschleunigen.[32][33][34][35]
Weblinks
- Animation und interaktiver Simulator zur Herdenimmunität. impfen-info.de
- Weitere Informationen zum Thema der Wissenschaftlichen Akademie für Vorsorgemedizin Graz
Einzelnachweise
- ↑ [ https://doi.org/10.1093/cid/cir007 Paul Fine u. a.: “Herd Immunity”: A Rough Guide], Clinical Infectious Diseases,Band 52, Ausgabe 7, 1. April 2011, Seiten 911–916
- ↑ a b c d e f T. H. Kim, J. Johnstone, M. Loeb: Vaccine herd effect. In: Scandinavian journal of infectious diseases. Band 43, Nummer 9, September 2011, S. 683–689, doi:10.3109/00365548.2011.582247, PMID 21604922, PMC 3171704 (freier Volltext).
- ↑ a b T. J. John, R. Samuel: Herd immunity and herd effect: new insights and definitions. In: Eur. J. Epidemiol., 2000, 16, 7., S. 601–606, PMID 11078115
- ↑ a b History and Epidemiology of Global Smallpox Eradication. ( des vom 15. Juli 2007 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 1,5 MB) From the training course Smallpox: Disease, Prevention, and Intervention. CDC and WHO. Slide 16-17.
- ↑ P. Fine: Herd immunity: history, theory, practice. In: Epidemiol Rev, 15, 2, 1993, S. 265–302. PMID 8174658.
- ↑ Gregg N. Milligan, Alan D. T. Barrett: Vaccinology. Wiley 2015, ISBN 978-1-118-63628-2. S. 313.
- ↑ a b c d e S. Cesaro, M. Giacchino, F. Fioredda, A. Barone, L. Battisti, S. Bezzio, S. Frenos, R. De Santis, S. Livadiotti, S. Marinello, A. G. Zanazzo, D. Caselli: Guidelines on vaccinations in paediatric haematology and oncology patients. In: BioMed research international. Band 2014, 2014, S. 707691, doi:10.1155/2014/707691, PMID 24868544, PMC 4020520 (freier Volltext)
- ↑ R. M. Wolfe: Update on adult immunizations. In: Journal of the American Board of Family Medicine : JABFM. Band 25, Nummer 4, 2012 Jul-Aug, S. 496–510, doi:10.3122/jabfm.2012.04.100274, PMID 22773718
- ↑ F. M. Munoz: Maternal immunization: an update for pediatricians. In: Pediatric annals. Band 42, Nummer 8, August 2013, S. 153–158, doi:10.3928/00904481-20130723-09, PMID 23910028.
- ↑ General recommendations on immunization –- recommendations of the Advisory Committee on Immunization Practices (ACIP). In: MMWR. Recommendations and reports : Morbidity and mortality weekly report. Recommendations and reports. Band 60, Nummer 2, Januar 2011, S. 1–64, PMID 21293327.
- ↑ S. Esposito, S. Bosis, L. Morlacchi, E. Baggi, C. Sabatini, N. Principi: Can infants be protected by means of maternal vaccination? In: Clinical microbiology and infection : the official publication of the European Society of Clinical Microbiology and Infectious Diseases. Band 18 Suppl 5, Oktober 2012, S. 85–92, doi:10.1111/j.1469-0691.2012.03936.x, PMID 22862749
- ↑ a b c d D. Rakel, R. E. Rakel: Textbook of Family Medicine. Elsevier Health Sciences, 2015, ISBN 978-0-323-31308-7, S. 99, 187 (google.com [abgerufen am 30. März 2015]).
- ↑ a b T. H. Tulchinsky, E. A. Varavikova: The New Public Health: An Introduction for the 21st Century. Academic Press, 2014, ISBN 978-0-12-415767-5, S. 163–82 (google.com [abgerufen am 30. März 2015]).
- ↑ L. F. Pittet, K. M. Posfay-Barbe: Pneumococcal vaccines for children: A global public health priority. In: Clinical Microbiology and Infection. 18 Suppl 5. Jahrgang, 2012, S. 25–36, doi:10.1111/j.1469-0691.2012.03938.x, PMID 22862432.
- ↑ O Nakagomi, M Iturriza-Gomara, T Nakagomi, N. A. Cunliffe: Incorporation of a rotavirus vaccine into the national immunisation schedule in the United Kingdom: A review. In: Expert Opinion on Biological Therapy. 13. Jahrgang, Nr. 11, 2013, S. 1613–21, doi:10.1517/14712598.2013.840285, PMID 24088009.
- ↑ B. A. Lopman, D. C. Payne, J. E. Tate, M. M. Patel, M. M. Cortese, U. D. Parashar: Post-licensure experience with rotavirus vaccination in high and middle income countries; 2006 to 2011. In: Current Opinion in Virology. 2. Jahrgang, Nr. 4, 2012, S. 434–42, doi:10.1016/j.coviro.2012.05.002, PMID 22749491 (zenodo.org).
- ↑ T. H. Kim: Seasonal influenza and vaccine herd effect. In: Clinical and Experimental Vaccine Research. 3. Jahrgang, Nr. 2, 2014, S. 128–32, doi:10.7774/cevr.2014.3.2.128, PMID 25003085, PMC 4083064 (freier Volltext).
- ↑ a b c G. P. Garnett: Role of herd immunity in determining the effect of vaccines against sexually transmitted disease. In: The Journal of Infectious Diseases. Band 191 Suppl 1, Februar 2005, S. S97–106, doi:10.1086/425271, PMID 15627236.
- ↑ D. R. Lowy, J. T. Schiller: Reducing HPV-associated cancer globally. In: Cancer Prevention Research. 5. Jahrgang, Nr. 1, 2012, S. 18–23, doi:10.1158/1940-6207.CAPR-11-0542, PMID 22219162, PMC 3285475 (freier Volltext).
- ↑ a b c A Lenzi, V Mirone, V Gentile, R Bartoletti, V Ficarra, C Foresta, L Mariani, S Mazzoli, S. G. Parisi, A Perino, M Picardo, C. M. Zotti: Rome Consensus Conference – statement; human papilloma virus diseases in males. In: BMC Public Health. 13. Jahrgang, 2013, S. 117, doi:10.1186/1471-2458-13-117, PMID 23391351, PMC 3642007 (freier Volltext).
- ↑ S. M. Garland, S. R. Skinner, J. M. Brotherton: Adolescent and young adult HPV vaccination in Australia: Achievements and challenges. In: Preventive Medicine. 53 Suppl 1. Jahrgang, 2011, S. S29–35, doi:10.1016/j.ypmed.2011.08.015, PMID 21962468.
- ↑ F. Njeumi, W. Taylor, A. Diallo, K. Miyagishima, P. P. Pastoret, B. Vallat, M. Traore: The long journey: a brief review of the eradication of rinderpest. In: Revue scientifique et technique. Band 31, Nummer 3, Dezember 2012, S. 729–746, doi:10.20506/rst.31.3.2157, PMID 23520729.
- ↑ F. Fenner: The global eradication of smallpox. In: Med J Aust., 1980 Mai 17,1(10), S. 455. PMID 7412674
- ↑ Polio situation worldwide in 2008 - update on the progress towards global eradication. In: Eurosurveillance, 2009 Apr 16;14(15), pii: 19178. PMID 19371512
- ↑ Weltgesundheitsorganisation: Poliomyelitis in Namibia. In: WHO – Disease Outbreak News, 6. Juni 2006
- ↑ Masern im Jahr 2005 und Ausbrüche in Baden-Württemberg und Nordrhein-Westfalen in der ersten Hälfte des Jahres 2006. (PDF) Robert Koch-Institut: Epidemiologisches Bulletin, Nr. 27, 7. Juli 2006.
- ↑ Takis Panagiotopoulos, Ioanna Antoniadou, Eleni Valassi-Adam: Increase in congenital rubella occurrence after immunisation in Greece: retrospective survey and systematic review. In: BMJ, 319, 1999, S. 1462–1467.
- ↑ W. John Edmunds: Health professionals do not understand mathematical models. In: BMJ, 320, 2000, S. 581
- ↑ J. Logan, D. Nederhoff, B. Koch, B. Griffith, J. Wolfson, F. A. Awan, N. E. Basta: ‘What have you HEARD about the HERD?‘ Does education about local influenza vaccination coverage and herd immunity affect willingness to vaccinate? In: Vaccine. Band 36, Nummer 28, 06 2018, S. 4118–4125, doi:10.1016/j.vaccine.2018.05.037, PMID 29789242, PMC 6008254 (freier Volltext).
- ↑ P. Fine, K. Eames, D. L. Heymann: "Herd immunity": a rough guide. In: Clinical Infectious Diseases. Band 52, Nummer 7, April 2011, S. 911–916, doi:10.1093/cid/cir007, PMID 21427399.
- ↑ K. A. Smith: Smallpox: can we still learn from the journey to eradication? In: The Indian journal of medical research. Band 137, Nummer 5, Mai 2013, S. 895–899, PMID 23760373, PMC 3734679 (freier Volltext).
- ↑ A Perisic, C. T. Bauch: Social contact networks and disease eradicability under voluntary vaccination. In: PLoS Computational Biology. 5. Jahrgang, Nr. 2, 2009, S. e1000280, doi:10.1371/journal.pcbi.1000280, PMID 19197342, PMC 2625434 (freier Volltext).
- ↑ F Fu, D. I. Rosenbloom, L Wang, M. A. Nowak: Imitation dynamics of vaccination behaviour on social networks. In: Proceedings of the Royal Society B: Biological Sciences. 278. Jahrgang, Nr. 1702, 2011, S. 42–49, doi:10.1098/rspb.2010.1107, PMID 20667876, PMC 2992723 (freier Volltext) – (harvard.edu [PDF]).
- ↑ S Wicker, H. C. Maltezou: Vaccine-preventable diseases in Europe: Where do we stand? In: Expert Review of Vaccines. 13. Jahrgang, Nr. 8, 2014, S. 979–87, doi:10.1586/14760584.2014.933077, PMID 24958075.
- ↑ E. Fukuda, J. Tanimoto: Impact of Stubborn Individuals on a Spread of Infectious Disease under Voluntary Vaccination Policy. Springer, 2014, ISBN 978-3-319-13359-1, S. 1–10 (google.com [abgerufen am 30. März 2015]).


