Borneole
Die Borneole sind eine in der Natur vorkommende Gruppe chemischer Verbindungen. Die isomeren Vertreter sind feste, farblose Substanzen, die strukturell einwertige, sekundäre Alkohole aus der Stoffklasse der bicyclischen Monoterpene sind.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Als sekundäre Pflanzenstoffe sind die Borneole Bestandteile vieler ätherischer Öle, wie Salbei (Salvia officinalis), Plectranthus barbatus, Rosmarin (Rosmarinus officinalis), Baldrian (Valeriana officinalis), Koriander (Coriandrum sativum), Waldkiefern (Pinus sylvestris), Thai-Ingwer (Alpinia galanga), Behaarter Zweizahn (Bidens pilosa), Ingwer (Zingiber officinale), Oregano (Origanum vulgare), Winter-Bohnenkraut (Satureja montana), Mutterkraut (Tanacetum parthenium) und Eukalyptus (Eucalyptus grandis).[1] (+)-Borneol/(D)-Borneol (Borneo Camper) findet man hauptsächlich im ätherischen Öl von Drybalanops camphora, einem auf Sumatra und Borneo heimischen Baum, sowie Muskatnuss ( Myristica fragrans ),[2] Amomum (Amomum compactum, Amomum xanthioides ),[3] Boswellia sacra,[3] Zitwerwurzel (Curcuma zedoaria),[3] Ingwer (Zingiber officinale),[3] Rosmarin, Lavendel und Olibanumöl. Hingegen findet man (–)-Borneol/(L)-Borneol (Ngai Camper) in Pinaceae,[4] Citronellöl,[4] Hanf (Cannabis sativa), Korianderöl (Coriandrum sativum), Mutterkraut (Chrysanthemum parthenium, Tanacetum parthenium), Zitronengras (Cymbopogon nardus), Schwarz-Fichte (Picea mariana), Baldrianöl (Valeriana officinalis), Citronellöl, Thujaöl (Thuja occidentalis) und anderen ätherischen Ölen.[5][6][7]
-
Ingwer
-
Salbei
-
Rosmarin
-
Muskatnuss
-
Lavendel
Isoborneole findet man unter anderem in Baldrian (Valeriana officinalis), Salbei (Salvia officinalis), Thymian (Thymus cilicicus), Oregano/Dost (Origanum vulgare, Origanum minutiflorum), Gemeiner Schafgarbe (Achillea millefolium), Bohnenkräuter (Satureja cilicica, Satureja odora), Bergminzen (Micromeria croatica), Kurkuma (Curcuma longa) und Rosmarin (Rosmarinus officinalis).[8]
-
Bergminze
-
Kurkuma
-
Gemeine Schafgarbe
-
Thymian
Vertreter[Bearbeiten | Quelltext bearbeiten]
Die Molekülstruktur der Borneole enthält chirale Kohlenstoffatome und kommt daher in zwei diastereomeren Formen vor, die üblicherweise Borneol und Isoborneol genannt werden. Da jede dieser beiden Formen ein (enantiomeres) Spiegelbild hat, existieren insgesamt vier Stereoisomere, von denen jeweils zwei enantiomer zueinander sind und die Racemate (±)-Borneol und (±)-Isoborneol bilden:
| Name | (+)-Borneol | (−)-Borneol | (+)-Isoborneol | (−)-Isoborneol | |||
| IUPAC-Name | (1R,2S,4R)-1,7,7-Trimethyl- bicyclo[2.2.1]heptan-2-ol |
(1S,2R,4S)-1,7,7-Trimethyl- bicyclo[2.2.1]heptan-2-ol |
(1S,2S,4S)-1,7,7-Trimethyl- bicyclo[2.2.1]heptan-2-ol |
(1R,2R,4R)-1,7,7-Trimethyl- bicyclo[2.2.1]heptan-2-ol | |||
| andere Namen | endo-Borneol (±)-Borneol |
exo-Isoborneol (±)-Isoborneol | |||||
| 2-Borneol 2-Bornylalkohol | |||||||
| Strukturformel | 
|

|

|
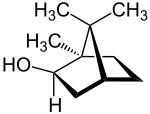
| |||
| CAS-Nummer | 464-43-7 | 464-45-9 | 16725-71-6 | 10334-13-1 | |||
| 507-70-0 (Racemat) | 124-76-5 (Racemat) | ||||||
| PubChem | 6552009 | 1201518 | 6321405 | ? | |||
| ? (Racemat) | 24900674 (Racemat) | ||||||
| FL-Nummer | 02.016 (Racemat) | 02.059 (Racemat) | |||||
| Summenformel | C10H18O | ||||||
| Molare Masse | 154,25 g·mol−1 | ||||||
| Aggregatzustand | fest | ||||||
| Kurzbeschreibung | farbloser, geruchloser Feststoff[9] | kristalliner, weißer Feststoff[10] | kristalliner, weißer Feststoff[11] mit angenehmem[11] Geruch nach Vanille und Holz[12] | ||||
| Schmelzpunkt[13] | 208–209 °C | 208–209 °C | 212–214 °C | 212–214 °C | |||
| 212 °C Racemat | 210–215 °C Racemat | ||||||
| Optischer Drehwert [α]D | + 37,7°[14] | − 37,7°[14] | + 34,1°[15] | − 33,6°[15] | |||
| Löslichkeit | unlöslich in Wasser[9] | unlöslich in Wasser[10] | unlöslich in Wasser[11] | ||||
| GHS- Kennzeichnung |
|
|
| ||||
| H-Sätze | 228 | 228 | 315‐319‐335 | ||||
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | |||||
| P-Sätze | 210‐280[9] | 210‐240‐241‐280‐370+378[10] | 261‐302+352‐305+351+338‐321[11] | ||||
| Toxikologische Daten | 5800 mg·kg−1 (LD50, Ratte, oral)[10] |
1750 mg·kg−1 (LD50, Maus, oral)[11] | |||||
Herstellung[Bearbeiten | Quelltext bearbeiten]
Borneol kann durch Meerwein-Ponndorf-Verley-Reduktion von Campher erhalten werden.[16] Bei der Reduktion von Campher mit Natriumborhydrid oder Lithiumaluminiumhydrid hingegen entsteht vorwiegend das Stereoisomer Isoborneol:[17]
- Diastereoselektivität der Reduktion von (1R,4R)-(+)-Campher zu (1R,2R,4R)-Isoborneol (ca. 95 %) und (1R,2S,4R)-Borneol (ca. 5 %).
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Borneol kann mit Chromsäure oder Salpetersäure zu Campher oxidiert werden. Dehydratation mit verdünnten Säuren führt zu Camphen.
Mit Acetanhydrid kann es zum Bornylacetat verestert werden.
Die bakterielle Biosynthese von 2-Methylisoborneol haben Forscher der TU Braunschweig mit dem Helmholtz-Zentrum für Infektionsforschung in Braunschweig und der Uni Saarbrücken erforscht.[18]
Verwendung[Bearbeiten | Quelltext bearbeiten]

Als Bestandteil von ätherischen Ölen ist Borneol mitverantwortlich für Geruch und Geschmack diverser Gewürze. Dergestalt wird es auch in Kosmetika eingesetzt. In der Inhaltsstoffliste wird es als BORNEOL (INCI)[19] aufgeführt.
Derivate des Borneols, wie (2S)-(−)-exo-(Dimethylamino)isoborneol (DAIB) werden in der modernen asymmetrischen Synthese genutzt.[20]
Struktur[Bearbeiten | Quelltext bearbeiten]
-
Stäbchenmodell von (S)-Borneol
-
Stäbchenmodell von (S)-Isoborneol
Literatur[Bearbeiten | Quelltext bearbeiten]
- H. Surburg, J. Panten: Common Fragrance and Flavor Materials: preparation, properties, and uses. Wiley-VCH, Weinheim 2006, ISBN 3-527-31315-X.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ BORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ (+)-BORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ a b c d D-BORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ a b Karl‐Georg Fahlbusch, Franz‐Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg: Flavors and Fragrances. In: Ullmann’s Encyclopedia of Industrial Chemistry. Band 15, 2012, S. 73–198, doi:10.1002/14356007.a11_141.
- ↑ Albert Gossauer: Struktur und Reaktivität der Biomoleküle, Verlag Helvetica Chimica Acta, Zürich, 2006, ISBN 3-906390-29-2, S. 206.
- ↑ (−)-BORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ L-BORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ ISOBORNEOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ a b c d Datenblatt (+)-Borneol (PDF) bei Carl Roth, abgerufen am 29. April 2010.
- ↑ a b c d e Datenblatt (–)-Borneol bei Alfa Aesar, abgerufen am 29. April 2010 (Seite nicht mehr abrufbar).
- ↑ a b c d e f g Datenblatt (±)-Isoborneol bei Alfa Aesar, abgerufen am 29. April 2010 (Seite nicht mehr abrufbar).
- ↑ Datenblatt (±)-Isoborneol bei Sigma-Aldrich, abgerufen am 29. April 2011 (PDF).
- ↑ Eintrag zu Borneole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. April 2011.
- ↑ a b Albert Gossauer: Struktur und Reaktivität der Biomoleküle. Verlag Helvetica Chimica Acta, Zürich 2006, ISBN 3-906390-29-2, S. 60.
- ↑ a b Hamada, Hiroki. In: Bull. Chem. Soc. Jpn., 1988, 61, S. 869–878.
- ↑ Ashok Pandey: Industrial Biorefineries & White Biotechnology. Elsevier, 2015, ISBN 978-0-444-63464-1, S. 132 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Jonathan Clayden, Nick Greeves, Stuart Warren, Peter Wothers: Organic Chemistry. Oxford University Press, 2001, ISBN 0-19-850346-6, S. 862.
- ↑ Biosynthesis of the Off-flavor 2-Methylisoborneol by the Myxobacterium Nannocystis exedens in: Angew. Chem. 2007, 119, 8436–8439.
- ↑ Eintrag zu BORNEOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 1. Oktober 2021.
- ↑ James D. White, Duncan J. Wardrop, and Kurt F. Sundermann: (2S)-(−)-exo-(dimethylamino)isoborneol [(2S)-(−)-DAIB] In: Organic Syntheses. 79, 2002, S. 130, doi:10.15227/orgsyn.079.0130 (PDF).












