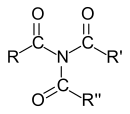
Carbonsäureamide
Carbonsäureamide sind Derivate des Ammoniaks oder Derivate von primären und sekundären Aminen, bei denen ein oder mehrere Wasserstoffatome am Stickstoff durch Acylgruppen (R–CO–) ersetzt sind. Als Carbonsäure-Derivate sind sie auch eine Untergruppe der Amide.
Carbonsäureamide bilden sich bei der Reaktion von reaktiven Carbonsäurederivaten, wie z. B. Carbonsäurechloriden oder Carbonsäureanhydriden mit Ammoniak oder mit geeigneten Aminen. Normale, nicht aktivierte Carbonsäuren reagieren mit den Basen Ammoniak oder Aminen nur zu den jeweiligen Ammoniumsalzen, jedoch nicht ohne weiteres zu Carbonsäureamiden.
Nomenklatur[Bearbeiten | Quelltext bearbeiten]
Die IUPAC-Nomenklatur unterscheidet bei Carbonsäureamiden entsprechend der Anzahl der Acylsubstituenten am Stickstoff zwischen primären (ein Acylsubstituent), sekundären (zwei Acylsubstituenten) und tertiären (drei Acylsubstituenten) Amiden.[1] Da jedoch nur für die unsubstituierten Mono- und Diacylderivate des Ammoniaks die Bezeichnung „primäres“, bzw. „sekundäres Amid“ eindeutig ist und im allgemeinen Sprachgebrauch primäre Amide mit einer Acylgruppe und zwei Kohlenwasserstoffsubstituenten am Stickstoff „tertiäre Amide“ genannt werden, wird die Klassifizierung in primäre, sekundäre und tertiäre Amide nicht empfohlen.[2][3]
Diacylsubstituierte Amide – insbesondere solche die sich von Dicarbonsäuren ableiten – werden Imide genannt. Amide mit ein oder zwei Alkylgruppen am Stickstoffatom nennt man N-Alkylamide, bzw. N,N-Dialkylamide. Cyclische Amide werden als Lactame bezeichnet. Peptide und Proteine bestehen aus durch Amidbindungen verknüpften Aminosäuren. Diese Form der Bindung wird oft Peptidbindung genannt. Technisch sehr bedeutend sind die Polyamidfasern Nylon und Perlon.[2]
Darstellung[Bearbeiten | Quelltext bearbeiten]
Amide werden hauptsächlich aus der Reaktion von Carbonsäurederivaten mit Ammoniak oder einem Amin gewonnen. Im einfachsten Fall handelt es sich bei dem Carbonsäurederivat um ein Carbonsäurechlorid. Das freigesetzte Chlorwasserstoff (HCl) reagiert mit dem Amin zu einem Hydrochlorid, sodass das Amin in doppelter Menge eingesetzt werden muss:
Die Aminolyse von Carbonsäureestern liefert Carbonsäureamide und Alkohole:
Carbonsäuren selbst reagieren mit Aminen zu den entsprechenden Salzen:
Bei starkem Erhitzen dissoziieren die Salze aber teilweise zu Amin und Carbonsäure, die dann unter Wasserabspaltung das Amid ergeben:
Weitere wichtige Verfahren zur Synthese von Amiden sind die Ritter-Reaktion, die Hydrolyse von Nitrilen, die Beckmann-Umlagerung und die Haller-Bauer-Spaltung.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]



Die Säureamide sind mesomeriestabilisiert. Sowohl das Carbonyl-Kohlenstoff-, als auch das Stickstoff-Atom sind sp2-hybridisiert, alle drei Atome der Amidgruppe, sowie deren Nachbaratome liegen in einer Ebene. Die C-N-Bindung ist wesentlich kürzer (132 pm) als in anderen Kohlenstoff-Stickstoffverbindungen (147 pm), so dass man vom Vorliegen eines konjugierten Systems ausgehen kann, in dem durch Delokalisierung von π-Elektronen ein partieller Doppelbindungscharakter vorliegt.
Wegen der sp2-Hybridisierung des Stickstoffs ist dessen freies Elektronenpaar kein protonierbares n-Elektronenpaar, sondern (wie z. B. im Pyrrol) ein zur Konjugation beitragendes π-Elektronenpaar. Daher sind Amide äußerst schwache Basen und bilden nur mit konzentrierten Säuren Salze, die leicht hydrolytisch gespalten werden.
Die Säureamide verhalten sich wie schwache Säuren. Sie werden durch starke Basen wie Natriumamid zu Amidaten deprotoniert. Die Alkalisalze der Amidate werden durch Wasser leicht zersetzt.[4] Die Bildung des Amidat-Ions durch Deprotonierung des Amids ist der erste Schritt bei der Hofmann-Umlagerung.[5]
Eine tautomere Form der Amide sind die Imidsäuren.[6]
Als Ursache für die verhältnismäßig hohen Siedepunkte und Schmelzpunkte von Carbonsäureamiden im Vergleich zu den Carbonsäuren wird deren partieller Zwitterionencharakter (siehe Abbildung) und die Ausbildung von Wasserstoffbrücken (siehe Abbildung) angesehen.[7]

Beispiele[Bearbeiten | Quelltext bearbeiten]
| Carbonsäureamide | ||
| Name | Struktur | Anmerkungen |
| Formamid |  |
Das einfachste Amid, abgeleitet von der Ameisensäure und Ammoniak |
| N,N-Dimethylformamid (DMF) |  |
Verwendet als aprotisches Lösungsmittel in der organischen Chemie und leitet sich von Dimethylamin und Ameisensäure ab. |
| Acetamid (Ethanamid) |  |
Amid der Essigsäure |
| Harnstoff |  |
Ein Diamid, abgeleitet von der Kohlensäure. |
| ε-Caprolactam |  |
Ein cyclisches Carbonsäureamid. Ein Ausgangsstoff für Polyamid 6. |
| Phthalimid |  |
Das cyclische Imid der Phthalsäure. |
| N-Benzoylphthalimid | 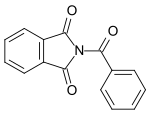 |
Benzoyliertes Phthalimid. |
| Weitere Beispiele siehe Kategorie:Amid, Kategorie:Lactam und Kategorie:Imid | ||
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Amides and Imides. Rule C-821. In: IUPAC Nomenclature of Organic Chemistry. Advanced Chemistry Development, Inc., abgerufen am 11. Mai 2019.
- ↑ a b Eintrag zu Amide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 23. Februar 2019.
- ↑ Amides, imides, and hydrazides. R-5.7.8 (Fußnote). In: IUPAC Nomenclature of Organic Chemistry, Recommendations 1993. Advanced Chemistry Development, Inc., abgerufen am 14. Mai 2019.
- ↑ Hans Beyer, Wolfgang Walter: Lehrbuch der organischen Chemie. 18. Auflage. S. Hirzel Verlag, Stuttgart 1978, ISBN 3-7776-0342-2, S. 225.
- ↑ Kurt Peter C. Vollhardt, Neil Eric Schore: Organische Chemie. 5. Auflage. Wiley-VCH, 2011, ISBN 978-3-527-32933-5 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eintrag zu Imidsäuren. In: Römpp Online. Georg Thieme Verlag, abgerufen am 23. Februar 2019.
- ↑ Joachim Buddrus, Bernd Schmidt: Grundlagen der Organischen Chemie, 5. Auflage, de Gruyter Verlag, Berlin, 2015, S. 572, ISBN 978-3-11-030559-3.