Hybridorbital

Ein Hybridorbital ist ein Orbital, das rechnerisch aus einer Linearkombination der Wellenfunktionen der grundlegenden Atomorbitale entsteht. Diesen Modellierungsvorgang nennt man Hybridisierung (früher vereinzelt auch Bastardisierung) der Orbitale. Das Konzept wurde von Linus Pauling um 1931 entwickelt und ist Teil der Valenzbindungstheorie.
Vorgehen[Bearbeiten | Quelltext bearbeiten]

Die in der Quantenmechanik berechenbaren Aufenthaltswahrscheinlichkeiten der von den Elektronen besetzten Orbitale in einem freien Atom sind zum Teil anders geformt, als aus den chemischen Eigenschaften des Atoms zu schließen ist. Das einzelne Kohlenstoffatom zum Beispiel ist in der äußeren Elektronenschale mit zwei s- und zwei p-Elektronen besetzt. Dementsprechend müssten diese Orbitale bei den vier C-H-Bindungen im Methan (CH4) zu unterschiedlich starken Bindungen führen. Tatsächlich jedoch sind die vier Bindungen gleichartig und nicht unterscheidbar. Dies kann man durch sp3-Hybridisierung modellieren: Das doppelt besetzte, kugelförmige 2s-Orbital wird mit den hantelförmigen 2p-Orbitalen (2 einfach besetzt, eins unbesetzt) zu vier gleichen, keulenförmigen sp3-Hybridorbitalen kombiniert, die tetraedrisch im Raum ausgerichtet und mit je einem Elektron besetzt sind. Daraus errechnet sich zwar für das Atom zunächst eine etwas höhere Energie, aber die Geometrie der Bindungen wird korrekt dargestellt. Werden diese Atomorbitale des Kohlenstoffatoms nun mit jeweils einem Atomorbital eines Wasserstoffatoms kombiniert, so erhält man vier Molekülorbitale, die mit den vier Elektronen der Wasserstoffatome und den vier Elektronen der vier sp3-Hybridorbitale besetzt sind. Diese Anordnung weist eine geringere Gesamtenergie auf als die vier Hybrid-Atomorbitale. Es sei betont, dass die Hybridisierung kein physikalischer Vorgang, sondern ein Vorgehen bei der Modellierung ist, mit dem sich die vorhandenen Atomorbitale als Basisfunktionen so linear kombinieren lassen, dass für das Methanmolekül die experimentell bestimmbare Geometrie und die spektroskopischen Eigenschaften errechnet werden.
Carbokationen (Carbeniumionen) werden grundsätzlich als sp2-Hybridorbitale (s. Abbildung) modelliert, damit das leere Orbital 100 % p-Charakter hat und somit kein s-Anteil „verschwendet“ wird (Bentsche Regel). Die erste chemische Bindung zwischen zwei Atomen wird als σ-Bindung (Sigma-Bindung) bezeichnet, Doppel- und Dreifachbindungen als π-Bindung (Pi-Bindung). Während bei der σ-Bindung die Elektronendichte rotationssymmetrisch entlang der Bindungsachse (z-Achse) verteilt ist, kommt es bei der π-Bindung zu einer Verteilung der Elektronendichte ober- und unterhalb der Bindungsachse.[1] Bei der π-Bindung interagieren die auf der y-Achse liegenden Orbitale.[2]
Physikalische Interpretation[Bearbeiten | Quelltext bearbeiten]
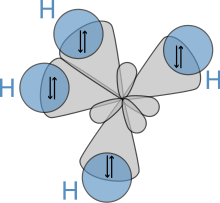

Orbitale, die sich in der Quantenmechanik als Eigenfunktionen des Einelektronenproblems (Wasserstoffatom) ergeben, haben jeweils einen bestimmten Drehimpuls und sind daher nicht in einer bestimmten räumlichen Richtung konzentriert. Dabei sind die Orbitale aus der gleichen Hauptschale bezüglich des Drehimpulses entartet. Das bedeutet, jede Überlagerung von Wellenfunktionen der gleichen Schale ist wieder eine Eigenfunktion und beschreibt somit ein mögliches Orbital zur selben Energie. Ein räumlich gerichtetes Orbital kann sich ergeben, wenn Orbitale mit unterschiedlichen Drehimpulsen überlagert werden. Solche Orbitale bilden im Sinne der Störungsrechnung die angepasste Nullte Näherung in Gegenwart von elektrischen Feldern. In Molekülen hebt der Einfluss der elektrischen Felder der Nachbaratome die Entartung dieser ausgerichteten Orbitale auf. Als energetisch günstigste Eigenfunktionen ergeben sich solche Überlagerungen von Orbitalen, in denen die Aufenthaltswahrscheinlichkeit des Elektrons in einer räumlichen Richtung konzentriert ist. Dies sind die Hybridorbitale, die stets aus Komponenten mit unterschiedlichem Bahndrehimpuls aufgebaut sind.
Wie alle an Atombindungen beteiligten Orbitale bilden auch die Hybridorbitale eines Atoms durch Mischung mit den Orbitalen der Nachbaratome Molekülorbitale.
Mathematische Betrachtung[Bearbeiten | Quelltext bearbeiten]
Zur Lösung der Einelektronen-Schrödingergleichung wird üblicherweise ein Produktansatz gemacht, ein Verfahren, das sich häufig zur Lösung von Differentialgleichungen 2. Ordnung eignet. Die Wellenfunktion , die sich zuerst beliebig aus Kugelkoordinaten zusammensetzt, wird als Produkt angeschrieben.
Dadurch gehen alle Lösungen verloren, die sich nicht als derartiges Produkt schreiben lassen. Lösungen, die beim Produktansatz verloren gehen, können durch Linearkombination der erhaltenen Lösung rückgewonnen werden. Beliebige Linearkombinationen zur gleichen Energie (und damit gleichen Hauptquantenzahl) sind wegen der Linearität des Hamiltonoperators auch exakte Lösungen der Einelektronen-Schrödingergleichung. Sie werden als Hybridorbitale bezeichnet.
Seien , und die Wellenfunktionen eines s-, p- bzw. d-Orbitals gleicher Quantenzahl. Die Wellenfunktion eines Hybridorbitals wird dann folgendermaßen gebildet.
Die hochgestellten Zahlen geben den quadrierten Anteil des Atomorbitals am Hybridorbital wieder.
Die Wellenfunktionen in komplexeren Systemen verhalten sich ähnlich. Dort werden jedoch auch Wellenfunktionen unterschiedlicher Hauptquantenzahl kombiniert. Ähnliche Energie ist entscheidend.
Soll ein ganzer Satz von Hybridorbitalen gebildet werden, ist zu beachten, dass die Transformationsmatrix eine unitäre Matrix (reeller Spezialfall: Orthogonalmatrix) sein muss. Das bedeutet, dass die Hybridorbitale wieder eine Orthonormalbasis bilden müssen. Das zugehörige Skalarprodukt ist:
Beispiele[Bearbeiten | Quelltext bearbeiten]
| sp (linear) |
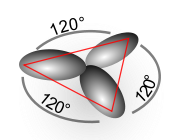
sp2 (trigonal-planar) |
sp3 (tetraedrisch) | |
|---|---|---|---|
| Beispiele von Kohlenwasserstoffen | Ethin (C2H2) | Ethen (C2H4) | Methan (CH4) |
| Darstellung der o. g. Kohlenwasserstoffe in Keilstrichform | 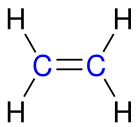
|

| |
| Darstellung des jeweiligen hybridisierten C-Atoms der o. g. Kohlenwasserstoffe | 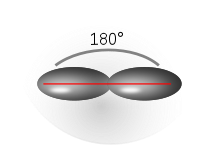
|
|

|

|

|

|

| Klassifikation | spx-Hybridisierung | sdx-Hybridisierung | spxdy-Hybridisierung |
|---|---|---|---|
| Hauptgruppe/ Übergangsmetalle |
nur Übergangsmetalle | ||
| AX2 |
|
||
| AX3 |
|
||
| AX4 |
|
|
|
| AX6 |
|
| |
| Interorbitalwinkel | |||
| Klassifikation | Hauptgruppe |
|---|---|
| AX5 | trigonal-bipyramidal |

| |
| AX6 | oktaedrisch |
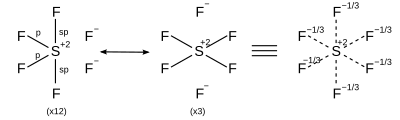
| |
| AX7 | pentagonal-bipyramidal |
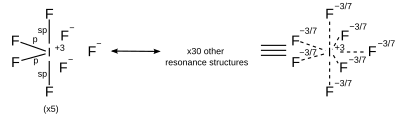
|
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Wolfgang Demtröder: Experimentalphysik 3. Atome, Moleküle und Festkörper. 3. Auflage. Springer-Verlag, Berlin/Heidelberg 2000, ISBN 3-540-66790-3.
- Erwin Riedel: Anorganische Chemie. 4. Auflage. Walter de Gruyter, New York 2002, ISBN 3-11-016602-X.
- Henry A. Bent: An Appraisal of Valence-bond Structures and Hybridization in Compounds of the First-row elements. In: Chemical Reviews. Band 61, Nr. 3, 1961, S. 275–311, doi:10.1021/cr60211a005.
- Weinhold, Frank; Landis, Clark R.: Valency and bonding: A Natural Bond Orbital Donor-Acceptor Perspective. Cambridge University Press, Cambridge 2005, ISBN 0-521-83128-8.
- Craig Bayse, Michael Hall: Prediction of the Geometries of Simple Transition Metal Polyhydride Complexes by Symmetry Analysis. In: Journal of the American Chemical Society. Band 121, Nr. 6, 1999, S. 1348–1358, doi:10.1021/ja981965+.
- David L. Cooper, Terry P. Cunningham, Joseph Gerratt, Peter B. Karadakov, Mario Raimondi: Chemical Bonding to Hypercoordinate Second-Row Atoms: d Orbital Participation versus Democracy. In: J. Am. Chem. Soc. Band 116, Nr. 10, 1994, S. 4414–4426, doi:10.1021/ja00089a033.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Michael Binnewies, Maik Finze, Manfred Jäckel, Peer Schmidt, Helge Willner, Geoff Rayner-Canham: Allgemeine und Anorganische Chemie. Springer-Verlag, 2016, ISBN 978-3-662-45067-3. S. 116.
- ↑ Rodney Cotterill: Biophysik. John Wiley & Sons, 2008, ISBN 978-3-527-40686-9, S. 22.










