Citral
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 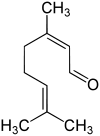
| ||||||||||
| links Geranial (Citral A), rechts Neral (Citral B) | ||||||||||
| Allgemeines | ||||||||||
| Name | Citral | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C10H16O | |||||||||
| Kurzbeschreibung |
hellgelbe Flüssigkeit mit zitronenähnlichem Geruch[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 152,24 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig | |||||||||
| Dichte |
0,89 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
225 °C[1] | |||||||||
| Dampfdruck | ||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (420 mg·l−1 bei 20 °C)[1] | |||||||||
| Brechungsindex |
1,4898 (20 °C)[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||
Citral ist das Gemisch aus den cis-trans-Isomeren Geranial (Citral A) und Neral (Citral B). Geranial ist als Duftstoff u. a. in Tomaten zu geringen Anteilen als Abbauprodukt von Lycopen zu finden. Citral ist Hauptbestandteil vom Lemongrasöl. Es ist Alarmpheromon der Blattschneiderameise.
Eigenschaften
Die CAS-Nummer von Citral ist 5392-40-5, die des Nerals 106-26-3[7] und die des Geranials 141-27-5.[8] Citral bzw. Neral und Geranial zählen chemisch zur Gruppe der acyclischen Monoterpen-Aldehyde. Citral ist eine schwach gelbliche Flüssigkeit mit intensiv frischem Zitronenduft. Das Gemisch siedet bei 228 °C, in Wasser ist es nahezu unlöslich. Citral wirkt in reiner Form sowie im Gemisch in Konzentrationen ab 1 % reizend auf die Haut.[1]
Verwendung
Citral wird als Duft- und Aromastoff verwendet.[9] Gemäß der 7. Ergänzung der EU Kosmetikrichtline 76/768/EEC muss es aufgrund allergenen Potenzials als kosmetischer Inhaltsstoff deklariert werden.
Die Auswirkungen von Citral auf die menschliche Gesundheit und die Umwelt werden unter REACH im Jahr 2015 im Rahmen der Stoffbewertung von Schweden geprüft.[10]
Reaktionen
Neral und Geranial lassen sich durch Dehydrierung aus Nerol und Geraniol herstellen. Citral reagiert mit Aceton im alkalischen Milieu (zum Beispiel Bariumhydroxid) zuerst unter Wasserabgabe zum Pseudoionon. Dieses kann dann unter Anwesenheit von Säuren und höheren Temperaturen in das Isomer Ionon überführt werden.[11][12]
Im alkalischen Milieu kann es auch in Acetaldehyd und 2-Methylhept-2-en-6-on zerfallen (Retro-Aldol-Reaktion).
Die heterogen katalysierte Hydrierung in Gegenwart von Palladiumkatalysatoren führt über die Zwischenstufe Citronellal mit etwa 86 % Ausbeute zum Dihydrocitronellal.[13]
Einzelnachweise
- ↑ a b c d e f g h Eintrag zu Citral in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-118.
- ↑ Eintrag zu Citral im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA) Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Biochemical Journal. Vol. 34, S. 1196, 1940.
- ↑ a b Eintrag in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar).
- ↑ Food and Cosmetics Toxicology. Vol. 2, Pg. 327, 1964.
- ↑ 643779 (Neral)
- ↑ 638011 (Geranial)
- ↑ Juliane Daphi-Weber, Heike Raddatz, Rainer Müller: Untersuchung von Riechstoffen – Kontrollierte Düfte, S. 94–95, in Band V der Reihe HighChem hautnah – Aktuelles aus der Lebensmittelchemie (Herausgegeben von der Gesellschaft Deutscher Chemiker) 2010, ISBN 978-3-936028-64-5.
- ↑ Vorlage:CoRAP-Liste
- ↑ NODA, C., ALT, G. P., WERNECK, R. M. et al.: Aldol Condensation of Citral with Acetone on Basic Solid Catalysts, in: Braz. J. Chem. Eng., 1998, 15; doi:10.1590/S0104-66321998000200004; Abstract
- ↑ A. Russell, R.L. Kenyon: Pseudoionone In: Organic Syntheses. 23, 1943, S. 78, doi:10.15227/orgsyn.023.0078; Coll. Vol. 3, 1955, S. 747 (PDF).
- ↑ P. Claus, J. Arras, D. Ruppert: Einfluss ionischer Flüssigkeiten mit funktionalisierten Kationen auf die palladiumkatalysierte Flüssigphasenhydrierung von Citral, in: Chem. Ing. Techn. 81 (2009), S. 2007–2011; doi:10.1002/cite.200900085.
