Acetophenon
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
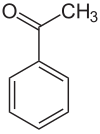
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Acetophenon | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H8O | |||||||||||||||
| Kurzbeschreibung |
farblose bis schwach gelbliche, ölige Flüssigkeit mit süßem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 120,15 g·mol−1 | |||||||||||||||
| Aggregatzustand |
über 20 °C flüssig, darunter fest | |||||||||||||||
| Dichte |
1,03 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
202 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,5372 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Acetophenon [] (Name zusammengesetzt aus: Acetyl-, o, phen von der Phenylgruppe und on zur Kennzeichnung als Keton) ist eine aromatische organisch-chemische Verbindung und gehört zu den Ketonen. Acetophenon wird unter anderem als Hypnotikum eingesetzt und ist als solches unter dem Trivialnamen Hypnon bekannt.
Vorkommen
Acetophenon ist weiterhin ein Bestandteil vieler ätherischer Öle wie etwa Labdanum, Castoreum, Stirlingia latifolia. Außerdem kommt dieses Keton in vielen natürlichen Aromen und in Steinkohleteer vor.[1]
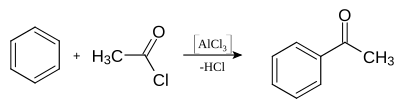
Gewinnung und Darstellung
Acetophenon lässt sich durch Friedel-Crafts-Acylierung von Benzol mit Essigsäurechlorid oder Essigsäureanhydrid herstellen. Im Gegensatz zur Friedel-Crafts-Alkylierung fungiert dabei die Lewis-Säure Aluminiumchlorid (AlCl3) nicht als Katalysator, sondern wird als Reagenz in äquivalenten Mengen verbraucht, wobei nach der notwendigen Hydrolyse des Zwischenprodukts Aluminiumhydroxid entsteht.
Eigenschaften
Physikalische Eigenschaften
Acetophenon ist eine farblose bis gelbliche Flüssigkeit mit einem süßen, an Orangenblüten erinnernden Geruch.[1] Unter Normaldruck siedet die Verbindung bei 202 °C. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,64896, B = 2006,397 und C = −43.472 im Temperaturbereich von 310 bis 475 K.[5] Acetophenon bildet mit Wasser ein azeotrop siedendes Gemisch bei 98 °C und 82 % Wasseranteil.[6]
| Eigenschaft | Typ | Wert [Einheit] | Bemerkungen |
|---|---|---|---|
| Standardbildungsenthalpie | ΔfH0liquid ΔfH0gas |
−142,5 kJ·mol−1[7] −86,7 kJ·mol−1[7] | |
| Standardentropie | S0gas | 372,88 J·mol−1·K−1[8] | als Gas |
| Verbrennungsenthalpie | ΔcH0liquid | −4148,9 kJ·mol−1[7] | |
| Wärmekapazität | cp | 227,6 J·mol−1·K−1 (25 °C)[9] | als Flüssigkeit |
| Kritische Temperatur | Tc | 709,6 K[10] | |
| Kritischer Druck | pc | 40,1 bar[10] | |
| Kritische Dichte | ρc | 2,59 mol·l−1[11] | |
| Schmelzenthalpie | ΔfH | 16,65 kJ·mol−1[12] | beim Schmelzpunkt |
| Verdampfungsenthalpie | ΔVH | 43,63 kJ·mol−1[13] | beim Normaldrucksiedepunkt |
Sicherheitstechnische Kenngrößen
Acetophenon bildet bei höheren Temperaturen entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 77 °C.[2][14] Die untere Explosionsgrenze liegt bei 1,1 Vol.‑% (55 g/m3), der untere Explosionspunkt bei 70 °C.[2][14] Die Zündtemperatur beträgt 535 °C.[2][14] Der Stoff fällt somit in die Temperaturklasse T1. Die elektrische Leitfähigkeit ist mit 3,1·10−7 S·m−1 eher gering.[15][2]
Verwendung
Acetophenon ist aufgrund seiner reaktionsfähigen Struktur Ausgangsstoff zahlreicher Synthesen als Ausgangs- oder Zwischenprodukt für andere Duftstoffe und Pharmazeutika sowie Kunstharze. Weiterhin ist er als hochsiedendes Lösungsmittel für Farben und Harze einsetzbar.
Sicherheitshinweise
Acetophenon als reiner Stoff ist beim Verschlucken gesundheitsschädlich. Er reizt die Augen und kann bei Einwirkung auf die ungeschützte Haut eine Dermatitis hervorrufen. Als Spritzschutz sollten geeignete Handschuhe getragen werden. In höheren Konzentrationen wirkt er hypnotisch, daher auch die Synonymbezeichnung Hypnon. Die Dämpfe erzeugen in einer Konzentration von 80 ppm bei einer Einwirkung von über einer Stunde starke Vergiftungserscheinungen. Acetophenon ist schwer entzündlich und wenig flüchtig. Die Dämpfe sind viel schwerer als Luft. Mit starken Oxidationsmitteln und starken Basen kann es zu stark exothermen Reaktionen kommen. Über 300 °C kommt es zur Zersetzung von Acetophenon. Dabei können Benzol, Biphenyl, 1,4-Diphenylbenzol, Kohlenstoffmonoxid, Methan, Wasserstoff, Ethen und/oder Toluol entstehen.
Derivate
Ausgehend von Acetophenon gibt es einige Derivate mit zusätzlich Hydroxy- und Methoxygruppen als Substituenten:
Einzelnachweise
- ↑ a b c d e Eintrag zu Acetophenon. In: Römpp Online. Georg Thieme Verlag
- ↑ a b c d e f g h i j k l m Eintrag zu Acetophenon in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-6.
- ↑ Eintrag zu Acetophenone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA) Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Stull, D.R.: Vapor Pressure of Pure Substances Organic Compounds in Ind. Eng. Chem. 39 (1947) 517–540, doi:10.1021/ie50448a022.
- ↑ I.M. Smallwood: Handbook of organic solvent properties, Arnold London 1996, ISBN 0-340-64578-4, S. 183–185.
- ↑ a b c Colomina, M.; Latorre, C.; Perez-Ossorio, R.: Heats of combustion of five alkyl phenyl ketones in Pure Appl. Chem. 2 (1961) 133–135.
- ↑ Stull D.R., Jr.: The Chemical Thermodynamics of Organic Compounds, Wiley, New York, 1969.
- ↑ Phillip, N.M.: Adiabatic and isothermal compressibilities of liquids in Proc. Indian Acad. Sci., 1939, A9, 109–120.
- ↑ a b Teja, A.S.; Rosenthal, D.J.: The critical pressures and temperatures of ten substances using a low residence time flow apparatus in Experimental Results for Phase Equilibria and Pure Component Properties in DIPPR DATA Series No. 1, 1991.
- ↑ Teja, A.S.; Anselme, M.J.: The critical properties of thermally stable and unstable fluids. I. 1985 results in AIChE Symp. Ser., 1990, 86, 279, 115–121.
- ↑ Luginin: Bull. Soc. Chim. Fr. 9 (1911) 223.
- ↑ Steele, W.V.; Chirico, R.D.; Knipmeyer, S.E.; Nguyen, A.: in J. Chem. Eng. Data 41 (1996) 1255–1268, doi:10.1021/je9601117.
- ↑ a b c E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- ↑ Technische Regel für Gefahrstoffe TRGS 727, BG RCI Merkblatt T033 Vermeidung von Zündgefahren infolge elektrostatischer Aufladungen, Stand August 2016, Jedermann-Verlag Heidelberg, ISBN 978-3-86825-103-6.