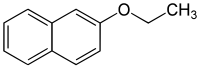
Ethyl-2-naphthylether
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Ethyl-2-naphthylether | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C12H12O | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 172,23 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
37,5 °C[4] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,5975 (36 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Ethyl-2-naphthylether ist eine chemische Verbindung, die sich vom 2-Naphthol ableitet. Der Phenolether, welcher in der Natur nicht vorkommt,[7] wird in der Parfümindustrie als Duftstoff verwendet.[8]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die farblosen Kristalle des Ethyl-2-naphthylethers sind nicht in Wasser, gering in Propylenglycol, aber gut in vielen in organischen Lösungsmitteln wie Ethanol und Kohlenstoffdisulfid löslich.[3] Die Bildungsenthalpie beträgt −134 kJ·mol−1, die Verbrennungsenthalpie −6303 kJ·mol−1[9]
Herstellung
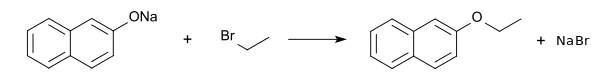
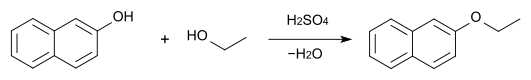
[Bearbeiten | Quelltext bearbeiten]Die Herstellung kann mittels der Williamson’sche Ethersynthese aus Natriumnaphtholat mit Bromethan oder Diethylsulfat sowie der Umsetzung von 2-Naphthol mit Ethanol und Schwefelsäure erfolgen.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Ethyl-2-naphthylether besitzt einen Geruch nach Orangenblüten und – in starker Verdünnung – einen Geschmack nach Erdbeeren.[3] Daher wird der Ether vielfach in Parfümerie und Kosmetik verwendet.[5] In Lebensmitteln wie Backwaren, Kaugummis, Getränken, Puddings und Süßigkeiten wird der Aromastoff in Konzentrationen zwischen 0,1 und maximal 16,4 ppm eingesetzt. Die erlaubte Tagesdosis (ADI, in den USA FEMA PADI) liegt bei 2,56 mg/Tag.[3] Der Gesamtverbrauch in den USA lag im Jahr 2001 bei etwa 5 Tonnen, vorwiegend als Geruchsstoff in Seifen und Waschmitteln, Kosmetikprodukten und Parfüms;[10] lediglich 3 kg wurden im Jahr 2004 in Lebensmitteln als Aromastoff eingesetzt.[3]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu ETHYL BETA-NAPHTHYL ETHER in der CosIng-Datenbank der EU-Kommission, abgerufen am 26. März 2022.
- ↑ a b Datenblatt Ethyl-2-naphthylether bei Alfa Aesar, abgerufen am 15. Dezember 2010 (Seite nicht mehr abrufbar).
- ↑ a b c d e f George A. Burdock: Fenaroli's Handbook of Flavor Ingredients. CRC Press, 2004, ISBN 978-1-4200-3787-6, S. 1353 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e f David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-236.
- ↑ a b c RÖMPP. 9. Auflage. 1995, ISBN 3-13-102759-2, S. 1261.
- ↑ a b Datenblatt Nerolin bromelia bei Sigma-Aldrich, abgerufen am 31. März 2011 (PDF).
- ↑ Karl‐Georg Fahlbusch, Franz‐Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe, Horst Surburg: Flavors and Fragrances. In: Ullmann's Encyclopedia of Industrial Chemistry. Band 15, 2012, S. 121, doi:10.1002/14356007.a11_141.
- ↑ Ignatius Valerius Stanley Stanislaus: American Soap Maker's Guide. H. C. Baird & Company, Incorporated, 1928, S. 593 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Colomina, M.; Roux, M.V.; Turrion, C.: Thermochemical properties of naphthalene compounds. IV. Enthalpies of combustion and formation of 2-methoxynaphthalene, 2-ethoxynaphthalene, and 2,3- and 2,7-dihydroxynaphthalenes in J. Chem. Thermodyn. 8 (1976) S. 869–872.
- ↑ Irving S. Rossoff: Encyclopedia of clinical toxicology: a comprehensive guide and reference to the toxicology of prescription and OTC drugs, chemicals, herbals, plants, fungi, marine life, reptiles and insect venoms, food ingredients, clothing, and environmental toxins. Informa Health Care, 2002, ISBN 978-1-84214-101-4, S. 432.