Phenylacetylen
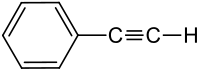
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Phenylacetylen | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H6 | ||||||||||||||||||
| Kurzbeschreibung |
gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 102,14 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,93 g·cm−3 (20 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
142–144 °C (1013 hPa)[1] | ||||||||||||||||||
| Dampfdruck |
2,7 hPa (25 °C)[1] | ||||||||||||||||||
| Löslichkeit |
0,46 g·l−1 in Wasser (25 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,5494 (bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Phenylacetylen ist das einfachste aromatische Alkin. Es ist eine farblose, viskose Flüssigkeit mit einem Flammpunkt von 27 °C.[1] In der Forschung wird es manchmal als Analogon zu Acetylen verwendet, als Flüssigkeit ist es leichter zu handhaben als gasförmiges Acetylen.
Herstellung[Bearbeiten | Quelltext bearbeiten]
Im Labor kann Phenylacetylen durch Eliminierung von Bromwasserstoff aus 1,2-Dibromphenylethan (auch fälschlicherweise als Styroldibromid bezeichnet) mit Natriumamid in flüssigem Ammoniak erhalten werden:[3]
Es kann auch durch Eliminierung von Bromwasserstoff aus 1- oder 2-Bromphenylethen (als Trivialnamen 1- oder 2-Bromstyrol) mit geschmolzenen Kaliumhydroxid hergestellt werden.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Wie Acetylen reagiert auch seine Ethinylgruppe (–C≡C–H) gegenüber sehr starken Basen (wie z. B. NaNH2) als Säure und zeigt andere, für Alkine typische Reaktionen, wie elektrophile Additionen, Hydrierung oder Polymerisationen. Die Verbindung ist thermisch instabil. In einer DSC-Messung wird oberhalb von 115 °C eine stark exotherme Zersetzung mit einer Zersetzungswärme von −1921 kJ·kg−1 bzw. −196 kJ·mol−1 beobachtet.[5] Phenylacetylen bildet mit Luft leicht entzündliche Gemische. Der Flammpunkt liegt bei 27 °C.[6]
Reaktionen[Bearbeiten | Quelltext bearbeiten]
- Phenylacetylen kann durch Wasserstoff über dem Lindlar-Katalysator zu Styrol reduziert (hydriert) werden. Die vollständige Hydrierung der Dreifachbindung führt zum Ethylbenzol. Die Reaktion verläuft mit einer Reaktionsenthalpie von −176,6 kJ·mol−1 exotherm.[7][8]
- Es trimerisiert unter Metallkatalyse zu 1,2,4- (97 %) und 1,3,5-Triphenylbenzol (3 %):[9]
- Es addiert unter Katalyse von Natriumtetrachloroaurat Wasser. Das zunächst entstehende Enol tautomerisiert spontan zu Acetophenon:
Diese Reaktion hat jedoch keine praktische Bedeutung, da Acetophenon durch eine einfache Friedel-Crafts-Acylierung von Benzol mit Acetylchlorid und Lewis-Säuren herstellbar ist.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h i Datenblatt Phenylacetylen bei Merck, abgerufen am 19. April 2011.
- ↑ Robert A. Benkeser, Richard A. Hickner: The Stereochemistry of the Addition of Silicochloroform to Acetylenes. In: Journal of the American Chemical Society. Band 80, Nr. 19, Oktober 1958, S. 5298–5300, doi:10.1021/ja01552a072.
- ↑ Kenneth N. Campbell, Barbara K. Campbell: Phenylacetylene In: Organic Syntheses. 30, 1950, S. 72, doi:10.15227/orgsyn.030.0072; Coll. Vol. 4, 1963, S. 763 (PDF).
- ↑ John C. Hessler: Phenylacetylene In: Organic Syntheses. 2, 1922, S. 67, doi:10.15227/orgsyn.002.0067; Coll. Vol. 1, 1941, S. 438 (PDF).
- ↑ Brach, N.; Le Fouler, V.; Bizet, V.; Lanz, M.; Gallou, F.; Bailly, C.; Hoehn, P.; Parmentier, M.; Blanchard, N.: Optimized Synthesis of 7‑Azaindazole by a Diels-Alder Cascade and Associated Process Safety in Org. Process Res. Dev. 24 (2020) 776–786, doi:10.1021/acs.oprd.0c00184.
- ↑ Datenblatt Phenylacetylen bei Alfa Aesar, abgerufen am 20. Mai 2016 (Seite nicht mehr abrufbar).
- ↑ Davis, H.E.; Allinger, N.L.; Rogers, D.W.: Enthalpies of hydrogenation of phenylalkynes: indirect determination of the enthalpy of formation of diphenylcyclopropenone in J. Org. Chem. 50 (1985) 3601–3604, doi:10.1021/jo00219a030.
- ↑ Rogers, D.W.; McLafferty, F.J.: A new hydrogen calorimeter. Heats of hydrogenation of allyl and vinyl unsaturation adjacent to a ring in Tetrahedron 27 (1971) 3765–3775, doi:10.1016/S0040-4020(01)98237-7.
- ↑ Hilt, G.; Vogler, T.; Hess, W.; Galbiati, F.: A simple cobalt catalyst system for the efficient and regioselective cyclotrimerisation of alkynes in Chem. Commun. 11 (2005) 1474–1475, doi:10.1039/B417832G.





