„Wurmerkrankung“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Ergänzt, jetzt auch mit ekligen Bildern… Markierung: 2017-Quelltext-Bearbeitung |
Ersetzt. Folgt noch mehr. (Belegt) Markierung: 2017-Quelltext-Bearbeitung |
||
| Zeile 1: | Zeile 1: | ||
{{Belege|Der Artikel weist keinerlei Quellen auf.}} |
|||
{{Dieser Artikel|1=behandelt die Infektion. Für den Organismus, siehe [[Parasitärer Wurm]].}} |
{{Dieser Artikel|1=behandelt die Infektion. Für den Organismus, siehe [[Parasitärer Wurm]].}} |
||
{{Infobox |
{{Infobox |
||
| Zeile 13: | Zeile 12: | ||
Bodenübertragene Helminthiasis und [[Schistosomiasis]] sind die wichtigsten Helminthiasen und gehören zu den vernachlässigten [[Tropenkrankheit]]en.<ref>{{Internetquelle |url=https://www.cdc.gov/globalhealth/ntd/diseases/index.html |titel=CDC - Neglected Tropical Diseases - Diseases |datum=2022-03-07 |sprache=en-us |abruf=2022-04-06}}</ref> Diese Gruppe von Helmianthiasen wurde im Rahmen der gemeinsamen Aktion der weltweit führenden [[Pharmaunternehmen]] und [[Nichtregierungsorganisation]]en durch ein 2012 gestartetes Projekt namens ''London Declaration on Neglected Tropical Diseases'' ins Visier genommen, das darauf abzielt, bestimmte vernachlässigte Tropenkrankheiten bis 2020 zu kontrollieren oder auszurotten.<ref>{{Internetquelle |url=http://www.dfid.gov.uk/Documents/publications1/NTD%20Event%20-%20London%20Declaration%20on%20NTDs.pdf |titel=London Declaration on Neglected Tropical Diseases |datum=2012-01-30 |abruf=2022-04-06}}</ref> |
Bodenübertragene Helminthiasis und [[Schistosomiasis]] sind die wichtigsten Helminthiasen und gehören zu den vernachlässigten [[Tropenkrankheit]]en.<ref>{{Internetquelle |url=https://www.cdc.gov/globalhealth/ntd/diseases/index.html |titel=CDC - Neglected Tropical Diseases - Diseases |datum=2022-03-07 |sprache=en-us |abruf=2022-04-06}}</ref> Diese Gruppe von Helmianthiasen wurde im Rahmen der gemeinsamen Aktion der weltweit führenden [[Pharmaunternehmen]] und [[Nichtregierungsorganisation]]en durch ein 2012 gestartetes Projekt namens ''London Declaration on Neglected Tropical Diseases'' ins Visier genommen, das darauf abzielt, bestimmte vernachlässigte Tropenkrankheiten bis 2020 zu kontrollieren oder auszurotten.<ref>{{Internetquelle |url=http://www.dfid.gov.uk/Documents/publications1/NTD%20Event%20-%20London%20Declaration%20on%20NTDs.pdf |titel=London Declaration on Neglected Tropical Diseases |datum=2012-01-30 |abruf=2022-04-06}}</ref> |
||
Helminthiasis führt zu einem schlechten Geburtsergebnis, einer schlechten kognitiven Entwicklung, einer schlechten Schul- und Arbeitsleistung, einer schlechten sozioökonomischen Entwicklung und Armut.<ref>{{Internetquelle |url=http://whqlibdoc.who.int/trs/WHO_TRS_749.pdf |titel=Prevention and Control of Intestinal Parasitic Infections |datum=1987 |abruf=2022-04-06}}</ref><ref>{{Literatur |Autor=Joy Miller Del Rosso, Tonia Marek |Titel=Class Action: Improving School Performance in the Developing World Through Better Health and Nutrition |Verlag=World Bank Publications |Datum=1996-01-01 |ISBN=978-0-8213-3672-4 |Online=https://books.google.com/books?id=XeY4-Y15cCgC&lpg=PP1&ots=cC0-ba3B-q&dq=class%20action:%20improving%20school%20performance&pg=PP1#v=onepage&q=&f=false |Abruf=2022-04-06}}</ref> [[Chronische Erkrankung]]en, [[Unterernährung]] und [[Anämie]] sind weitere Beispiele für [[Nebenwirkung]]en.<ref>{{Literatur |Autor=World Health Organization, TDR Disease Reference Group on Helminth Infections |Titel=Research priorities for helminth infections |Sammelwerk=World Health Organization Technical Report Series |Nummer=972 |Datum=2012 |ISSN=0512-3054 |PMID=23420950 |Seiten=xv–xvii, 1–174, back cover |Online=https://pubmed.ncbi.nlm.nih.gov/23420950/ |Abruf=2022-04-06}}</ref> |
Helminthiasis führt zu einem schlechten Geburtsergebnis, einer schlechten kognitiven Entwicklung, einer schlechten Schul- und Arbeitsleistung, einer schlechten sozioökonomischen Entwicklung und Armut.<ref name=":3">{{Internetquelle |url=http://whqlibdoc.who.int/trs/WHO_TRS_749.pdf |titel=Prevention and Control of Intestinal Parasitic Infections |datum=1987 |abruf=2022-04-06}}</ref><ref name=":4">{{Literatur |Autor=Joy Miller Del Rosso, Tonia Marek |Titel=Class Action: Improving School Performance in the Developing World Through Better Health and Nutrition |Verlag=World Bank Publications |Datum=1996-01-01 |ISBN=978-0-8213-3672-4 |Online=https://books.google.com/books?id=XeY4-Y15cCgC&lpg=PP1&ots=cC0-ba3B-q&dq=class%20action:%20improving%20school%20performance&pg=PP1#v=onepage&q=&f=false |Abruf=2022-04-06}}</ref> [[Chronische Erkrankung]]en, [[Unterernährung]] und [[Anämie]] sind weitere Beispiele für [[Nebenwirkung]]en.<ref name=":5">{{Literatur |Autor=World Health Organization, TDR Disease Reference Group on Helminth Infections |Titel=Research priorities for helminth infections |Sammelwerk=World Health Organization Technical Report Series |Nummer=972 |Datum=2012 |ISSN=0512-3054 |PMID=23420950 |Seiten=xv–xvii, 1–174, back cover |Online=https://pubmed.ncbi.nlm.nih.gov/23420950/ |Abruf=2022-04-06}}</ref> |
||
Bodenübertragene Helminthiasen sind für [[parasitäre Infektion]]en in bis zu einem Viertel der menschlichen Bevölkerung weltweit verantwortlich.<ref>{{Internetquelle |url=https://web.archive.org/web/20120820003930/http://www.who.int/mediacentre/factsheets/fs366/en/ |titel=WHO {{!}} Soil-transmitted helminth infections |datum=2012-08-20 |abruf=2022-04-06}}</ref> Ein bekanntes Beispiel für bodenübertragene Helminthiasen ist [[Ascariasis]]. |
Bodenübertragene Helminthiasen sind für [[parasitäre Infektion]]en in bis zu einem Viertel der menschlichen Bevölkerung weltweit verantwortlich.<ref>{{Internetquelle |url=https://web.archive.org/web/20120820003930/http://www.who.int/mediacentre/factsheets/fs366/en/ |titel=WHO {{!}} Soil-transmitted helminth infections |datum=2012-08-20 |abruf=2022-04-06}}</ref> Ein bekanntes Beispiel für bodenübertragene Helminthiasen ist [[Ascariasis]]. |
||
| Zeile 31: | Zeile 30: | ||
Als Erreger im Körper induzieren Helminthen eine [[Immunantwort]]. Immunvermittelte entzündliche Veränderungen treten in [[Haut]], [[Lunge]], [[Leber]], Darm, im [[Zentralnervensystem]] und in den [[Auge]]n auf. Anzeichen der Immunantwort des Körpers können [[Eosinophilie]], [[Ödem]] und [[Arthritis]] sein.<ref>{{Literatur |Autor=P. L. Minciullo, A. Cascio, A. David, L. M. Pernice, G. Calapai |Titel=Anaphylaxis caused by helminths: review of the literature |Sammelwerk=European Review for Medical and Pharmacological Sciences |Band=16 |Nummer=11 |Datum=2012-10 |ISSN=1128-3602 |PMID=23111963 |Seiten=1513–1518 |Online=https://pubmed.ncbi.nlm.nih.gov/23111963/ |Abruf=2022-04-06}}</ref> Ein Beispiel für die Immunantwort ist die [[Überempfindlichkeitsreaktion]], die zu [[Anaphylaxie]] führen kann. Ein weiteres Beispiel ist die Migration von [[Ascaris]]-Larven durch die [[Bronchien]] der Lunge, die [[Asthma bronchiale|Asthma]] verursachen.<ref>{{Literatur |Autor=David T. John |Titel=Markell and Voge's medical parasitology |Auflage=9th ed |Verlag=Saunders Elsevier |Ort=St. Louis, Mo. |Datum=2006 |ISBN=978-0-7216-4793-7}}</ref> |
Als Erreger im Körper induzieren Helminthen eine [[Immunantwort]]. Immunvermittelte entzündliche Veränderungen treten in [[Haut]], [[Lunge]], [[Leber]], Darm, im [[Zentralnervensystem]] und in den [[Auge]]n auf. Anzeichen der Immunantwort des Körpers können [[Eosinophilie]], [[Ödem]] und [[Arthritis]] sein.<ref>{{Literatur |Autor=P. L. Minciullo, A. Cascio, A. David, L. M. Pernice, G. Calapai |Titel=Anaphylaxis caused by helminths: review of the literature |Sammelwerk=European Review for Medical and Pharmacological Sciences |Band=16 |Nummer=11 |Datum=2012-10 |ISSN=1128-3602 |PMID=23111963 |Seiten=1513–1518 |Online=https://pubmed.ncbi.nlm.nih.gov/23111963/ |Abruf=2022-04-06}}</ref> Ein Beispiel für die Immunantwort ist die [[Überempfindlichkeitsreaktion]], die zu [[Anaphylaxie]] führen kann. Ein weiteres Beispiel ist die Migration von [[Ascaris]]-Larven durch die [[Bronchien]] der Lunge, die [[Asthma bronchiale|Asthma]] verursachen.<ref>{{Literatur |Autor=David T. John |Titel=Markell and Voge's medical parasitology |Auflage=9th ed |Verlag=Saunders Elsevier |Ort=St. Louis, Mo. |Datum=2006 |ISBN=978-0-7216-4793-7}}</ref> |
||
== |
== Sekundäre Effekte == |
||
[[Datei:Helminth in appendix 20x.jpg|mini|[[Mikrographie (Medizin)|Mikrographie]] des Schnittabschnitts des menschlichen [[Appendix vermiformis]], der einen Nadelwurm zeigt.]] |
|||
Präpatente Infektion: Die Wurminfektion beginnt mit der Aufnahme bzw. dem Eindringen infektionsfähiger Wurmstadien in einen Organismus. Anschließend entwickeln sich die Würmer im Wirtsorganismus. |
|||
=== Immunveränderungen === |
|||
Beim Menschen reagieren [[T-Helferzelle]]n und [[Eosinophiler Granulozyt|Eosinophile]] auf Helminthenbefall. Es ist allgemein bekannt, dass T-Helfer-2-Zellen die zentralen Akteure der schützenden Immunität gegen Helminthen sind,<ref>{{Literatur |Autor=Alba Cortés, Carla Muñoz-Antoli, J. Guillermo Esteban, Rafael Toledo |Titel=Th2 and Th1 Responses: Clear and Hidden Sides of Immunity Against Intestinal Helminths |Sammelwerk=Trends in Parasitology |Band=33 |Nummer=9 |Datum=2017-09 |ISSN=1471-5007 |DOI=10.1016/j.pt.2017.05.004 |PMID=28566191 |Seiten=678–693 |Online=https://pubmed.ncbi.nlm.nih.gov/28566191/ |Abruf=2022-04-06}}</ref> während die Rollen für [[B-Zellen]] und [[Antikörper]] kontextabhängig sind.<ref>{{Literatur |Autor=Aidil Zaini, Kim L. Good-Jacobson, Colby Zaph |Titel=Context-dependent roles of B cells during intestinal helminth infection |Sammelwerk=PLoS neglected tropical diseases |Band=15 |Nummer=5 |Datum=2021-05 |ISSN=1935-2735 |DOI=10.1371/journal.pntd.0009340 |PMC=8118336 |PMID=33983946 |Seiten=e0009340 |Online=https://pubmed.ncbi.nlm.nih.gov/33983946/ |Abruf=2022-04-06}}</ref> [[Entzündung]]en führen zur Verkapselung von Eiablagerungen im ganzen Körper. Helminthen scheiden toxische Substanzen nach der Fütterung in den Darm aus. Diese Substanzen gelangen dann in das [[Kreislaufsystem|Kreislauf]]- und [[Lymphsystem]] des Wirtskörpers. |
|||
Chronische Immunantworten auf Helminthiasis können zu einer erhöhten Anfälligkeit für andere Infektionen wie [[Tuberkulose]], [[HIV]] und [[Malaria]] führen.<ref>{{Literatur |Autor=Elly van Riet, Franca C. Hartgers, Maria Yazdanbakhsh |Titel=Chronic helminth infections induce immunomodulation: consequences and mechanisms |Sammelwerk=Immunobiology |Band=212 |Nummer=6 |Datum=2007 |ISSN=0171-2985 |DOI=10.1016/j.imbio.2007.03.009 |PMID=17544832 |Seiten=475–490 |Online=https://pubmed.ncbi.nlm.nih.gov/17544832/ |Abruf=2022-04-06}}</ref><ref>{{Literatur |Autor=Zilungile L. Mkhize-Kwitshana, Musawenkosi H. L. Mabaso |Titel=Status of medical parasitology in South Africa: new challenges and missed opportunities |Sammelwerk=Trends in Parasitology |Band=28 |Nummer=6 |Datum=2012-06 |ISSN=1471-5007 |DOI=10.1016/j.pt.2012.03.005 |PMID=22525798 |Seiten=217–219 |Online=https://pubmed.ncbi.nlm.nih.gov/22525798/ |Abruf=2022-04-06}}</ref><ref>{{Literatur |Autor=G. Borkow, Z. Bentwich |Titel=Eradication of helminthic infections may be essential for successful vaccination against HIV and tuberculosis |Sammelwerk=Bulletin of the World Health Organization |Band=78 |Nummer=11 |Datum=2000 |ISSN=0042-9686 |PMC=2560630 |PMID=11143198 |Seiten=1368–1369 |Online=https://pubmed.ncbi.nlm.nih.gov/11143198/ |Abruf=2022-04-06}}</ref> Es gibt widersprüchliche Informationen darüber, ob die Entwurmung die HIV-Progression und die Viruslast reduziert und die [[CD4-Rezeptor|CD4-Zahl]] bei [[AIDS|antiretroviralen]] naiven und erfahrenen Personen erhöht, obwohl die jüngste [[Cochrane (Organisation)|Cochrane]]-Überprüfung einige Hinweise darauf ergab, dass dieser Ansatz positive Auswirkungen haben könnte.<ref>{{Literatur |Autor=Alexander J. Lankowski, Alexander C. Tsai, Michael Kanyesigye, Mwebesa Bwana, Jessica E. Haberer |Titel=Empiric deworming and CD4 count recovery in HIV-infected Ugandans initiating antiretroviral therapy |Sammelwerk=PLoS neglected tropical diseases |Band=8 |Nummer=8 |Datum=2014-08 |ISSN=1935-2735 |DOI=10.1371/journal.pntd.0003036 |PMC=4125278 |PMID=25101890 |Seiten=e3036 |Online=https://pubmed.ncbi.nlm.nih.gov/25101890/ |Abruf=2022-04-06}}</ref><ref>{{Literatur |Autor=Arianna Rubin Means, Paul Burns, David Sinclair, Judd L. Walson |Titel=Antihelminthics in helminth-endemic areas: effects on HIV disease progression |Sammelwerk=The Cochrane Database of Systematic Reviews |Band=4 |Datum=2016-04-14 |ISSN=1469-493X |DOI=10.1002/14651858.CD006419.pub4 |PMC=4963621 |PMID=27075622 |Seiten=CD006419 |Online=https://pubmed.ncbi.nlm.nih.gov/27075622/ |Abruf=2022-04-06}}</ref> |
|||
Patente Infektion: Diese Phase beginnt, wenn die Entwicklung der Eindringlinge zu ausgewachsenen, eierlegenden Würmern abgeschlossen ist und ihre Fortpflanzungsprodukte in den Körperausscheidungen des Wirtes auftreten. |
|||
== |
== Chronische Krankheiten == |
||
Chronische Helminthiasis kann schwere [[Morbidität]] verursachen.<ref>{{Literatur |Autor=Derek Wakelin |Titel=Helminths: Pathogenesis and Defenses |Sammelwerk=Medical Microbiology |Auflage=4th |Verlag=University of Texas Medical Branch at Galveston |Ort=Galveston (TX) |Datum=1996 |ISBN=978-0-9631172-1-2 |PMID=21413312 |Online=http://www.ncbi.nlm.nih.gov/books/NBK8191/ |Abruf=2022-04-06}}</ref> Es wurde festgestellt, dass Helminthiasis zu einem schlechten Geburtsergebnis, einer schlechten kognitiven Entwicklung, einer schlechten Schul- und Arbeitsleistung, einer verminderten Produktivität, einer schlechten sozioökonomischen Entwicklung und Armut führt.<ref name=":3" /><ref name=":4" /><ref name=":5" /> |
|||
Die hervorgerufenen Erkrankungen werden durch die jeweils hervorrufende Wurmart oder Gruppe bezeichnet. |
|||
Die bedeutendsten Wurmerkrankungen: |
|||
* [[Spulwurm|Askariasis]] (Spulwurm) |
|||
* [[Enterobiasis]] (Madenwurm) |
|||
* [[Filariose]] (Fadenwürmer: Filarien) |
|||
* [[Bandwürmer|Taeniasis]] (Bandwürmer) |
|||
* [[Echinokokkose]] (Bandwürmer) |
|||
* [[Onchozerkose]] (Fadenwürmer) |
|||
* [[Trichinose]] (Fadenwürmer: Trichinen) |
|||
* [[Capillariasis]] (Haarwürmer) |
|||
=== Unterernährung === |
|||
Wurminfektionen werden mit [[Anthelminthikum|Antihelminthika]] behandelt.<ref>Hans-Adolf Oelkers: ''Pharmakologische Grundlagen der Behandlung von Wurmkrankheiten.'' 3. Auflage, Leipzig 1950 (= ''Beiträge zur Arzneimitteltherapie.'' Band 4).</ref> Bei Bandwürmern und Schistosomen ist [[Praziquantel]], bei Rundwürmern [[Mebendazol]] am besten wirksam und verträglich. |
|||
Helminthiasis kann [[chronische Krankheit]]en durch Unterernährung verursachen, einschließlich [[Vitaminmangel]], verkümmertes Wachstum, [[Anämie]] und Protein-Energie-[[Unterernährung]]. Würmer konkurrieren direkt mit ihren Wirten um Nährstoffe, aber das Ausmaß dieses Effekts ist wahrscheinlich minimal, da der Nährstoffbedarf von Würmern relativ gering ist.<ref name=":19">{{Internetquelle |autor=Levinger B |url=http://pdf.usaid.gov/pdf_docs/PNABQ180.pdf |titel=Nutrition, Health, and Learning: Current Issues and Trends (PDF) |datum=19l2 |abruf=2022-04-06}}</ref><ref name=":20">{{Internetquelle |url=https://web.archive.org/web/20140225050318/http://files.dcp2.org/pdf/WorldDevelopmentReport1993.pdf |titel=World Development Report 1993: Investing in Health (PDF) |abruf=2022-04-06}}</ref><ref name=":21">{{Literatur |Autor=W. E. Watkins, E. Pollitt |Titel="Stupidity or worms": do intestinal worms impair mental performance? |Sammelwerk=Psychological Bulletin |Band=121 |Nummer=2 |Datum=1997-03 |ISSN=0033-2909 |DOI=10.1037/0033-2909.121.2.171 |PMID=9100486 |Seiten=171–191 |Online=https://pubmed.ncbi.nlm.nih.gov/9100486/ |Abruf=2022-04-06}}</ref> Bei Schweinen und Menschen wurde Ascaris mit [[Laktoseintoleranz]] und [[Vitamin A]], [[Aminosäuren|Aminosäure]] und Fett-[[Malassimilation]] in Verbindung gebracht.<ref name=":3" /> Eine beeinträchtigte Nährstoffaufnahme kann durch direkte Schäden an der Darmschleimhautwand oder aus subtileren Veränderungen wie chemischen Ungleichgewichten und Veränderungen der Darmflora resultieren.<ref>{{Literatur |Autor=D. W. T. Crompton, David William Thomasson Crompton |Titel=Human Nutrition and Parasitic Infection: Volume 107, Parasitology Supplement 1993 |Verlag=Cambridge University Press |Datum=1994-07-06 |ISBN=978-0-521-45601-2 |Online=https://books.google.com/books?id=oT6BrfK7XQYC&lpg=PA5202&ots=FdAVfej2s0&dq=crompton%20Human%20Nutrition%20and%20Parasitic%20Infection.&pg=PA5202#v=onepage&q=&f=false |Abruf=2022-04-06}}</ref> Alternativ kann die Freisetzung von [[Proteasehemmer]]n durch die Würmer zur Abwehr der Verdauungsprozesse des Körpers den Abbau anderer Nährstoffe beeinträchtigen.<ref name=":19" /><ref name=":21" /> Darüber hinaus kann wurminduzierter [[Durchfall]] die Darmtransitzeit verkürzen und so die Aufnahme von Nährstoffen reduzieren.<ref name=":3" /> |
|||
[[Unterernährung]] aufgrund von Würmern kann zu [[Magersucht]] führen.<ref name=":20" /> Eine Studie mit 459 Kindern in [[Sansibar]] ergab einen spontanen Appetitanstieg nach der Entwurmung.<ref>{{Literatur |Autor=Rebecca J. Stoltzfus, Hababu M. Chway, Antonio Montresor, James M. Tielsch, Jape Khatib Jape |Titel=Low dose daily iron supplementation improves iron status and appetite but not anemia, whereas quarterly anthelminthic treatment improves growth, appetite and anemia in Zanzibari preschool children |Sammelwerk=The Journal of Nutrition |Band=134 |Nummer=2 |Datum=2004-02 |ISSN=0022-3166 |DOI=10.1093/jn/134.2.348 |PMID=14747671 |Seiten=348–356 |Online=https://pubmed.ncbi.nlm.nih.gov/14747671/ |Abruf=2022-04-06}}</ref> Magersucht könnte eine Folge der Immunantwort des Körpers und des Stresses bei der Bekämpfung von Infektionen sein.<ref name=":21" /> Insbesondere wurden einige der [[Zytokin]]e, die in der Immunantwort auf Wurmbefall freigesetzt werden, mit Magersucht bei Tieren in Verbindung gebracht.<ref name=":19" /> |
|||
== Pathogene Arten == |
|||
Hier sind nur die jeweils übergeordneten [[Taxonomie|Taxa]] der parasitären Würmer herausgehoben, für eine Gesamtübersicht siehe [[Parasiten des Menschen]]. |
|||
Ordnungen |
|||
* [[Pseudophyllidea]] |
|||
Familien |
|||
* [[Echinostomatidae]] |
|||
* [[Fasciolidae]] |
|||
* [[Opisthorchoiidae]] |
|||
* [[Heterophyidae]] |
|||
* [[Taeniidae]] |
|||
* [[Hymenolepidae]] |
|||
* [[Ancylostomatidae]] |
|||
* [[Oxyuridae]] |
|||
* [[Ascarididae]] |
|||
* [[Anisakidae]] |
|||
* [[Filariidae]] |
|||
* [[Onchocercidae]] |
|||
* [[Hirudinea]] |
|||
Gattungen und Arten |
|||
* [[Schistosoma]] |
|||
* [[Paragonimus]] |
|||
* [[Pentastomida]] |
|||
* [[Trichobilharzia szidati]] |
|||
* [[Dicrocoelium dendriticum]] |
|||
* [[Gastrodiscoides hominis]] |
|||
* [[Watsonius watsoni]] |
|||
* [[Fischoederius elongatus]] |
|||
* [[Stronyloides stercoralis]] |
|||
* [[Dracunculus medinensis]] |
|||
* [[Trichuris trichiura]] |
|||
* [[Dioctophyme renale]] |
|||
* [[Capillaria philippinensis]] |
|||
<!--zu überarbeiten, allerdings VIEL BESSER bei den einzelnen Krankheiten zu behandeln! Dies gilt IMHO auch für den großen Rest des Beitrags -- > |
|||
Der nächste [[Wirt (Biologie)|Wirt]] nimmt sie auf, wenn er mit Kot verunreinigte Nahrung zu sich nimmt. Manche Wurmlarven durchlaufen aber während ihrer Entwicklung auch den übrigen Körper manche Würmer überdauern als [[Bandwürmer|Finnen]],wo sie vom nächsten Wirt aufgenommen werden müßen. Deshalb sind diese Parasitosen nicht auf den Darm beschränkt sondern können sich im gesamten Organismus ausbreiten. |
|||
Wurmerkrankungen können lange unerkannt bleiben. Durch die [[Nahrungskonkurrenz]] können neben unspezifischen Bauchbeschwerden auch Mangelsyndrome auftreten (z. B. [[Anämie|Blutarmut]] nach jahrelangem Vitamin B12-Mangel). Invasive Wurminfektionen verursachen eine Eosinophilie (Überschuss an eosinophilen Granulozyten im Blut). Im Einzelfall kommen z. B. Muskel- und Gelenkschmerzen oder Sehstörungen bei Manifestation in einzelnen Organen vor. |
|||
--> |
|||
== Ausgewählte Arten == |
|||
=== Rundwürmer (Nematoden) === |
|||
==== ''Enterobius vermicularis'' (Madenwurm) ==== |
|||
Der [[Madenwurm]] ist ein etwa 1 cm langer weißer nichtinvasiver Wurm, der weltweit vorkommt. Er ernährt sich vom Nahrungsbrei im Darm, nachts kriechen die Weibchen nach draußen, um auf der Analhaut ihre Eier abzulegen, was einen starken Juckreiz verursacht. Ansonsten treten bei einer [[Infektion]] keine Symptome auf. Bei genauem Hinsehen kann man die kleinen Würmer auf dem Kot erkennen. Durch den Juckreiz und das Kratzen werden die Eier auf die Umgebung verteilt und über die Finger in den Mund wieder aufgenommen. Zur Diagnosestellung wird mit einem Objektträger eine Probe der Eier von der Analhaut genommen. Umgebung und Bettwäsche des Patienten müssen desinfiziert, Kontaktpersonen untersucht werden. |
|||
==== ''Trichuris trichuria'' (Peitschenwurm) ==== |
|||
Der [[Peitschenwurm]] hat seinen Namen von seinem langen dünnen Schwanz, mit dem er in der Darmschleimhaut festsitzt. Er betätigt sich als Nahrungskonkurrent, und bei starkem Befall kann er Bauchschmerzen verursachen. Er legt seine Eier in die Darmschleimhaut, die schlüpfenden [[Larve]]n entwickeln sich an Ort und Stelle zum adulten Wurm. Ausgeschiedene Eier können von nächsten Menschen mit der Nahrung aufgenommen werden. |
|||
==== ''Ascaris lumbricoides'' (Spulwurm) ==== |
|||
Der [[Spulwurm]] ist weltweit der häufigste Wurm. Sein Vermehrungszyklus ähnelt dem des Peitschenwurms. Die Larven des Spulwurms durchdringen allerdings die Darmwand und gelangen über die Blutbahn in die Lunge. Sie durchbrechen dort die Wand der Lungenbläschen und werden über die Luftröhre in den Rachen aufgehustet und dann über die Speiseröhre und den Magen wieder in den Darm verschluckt. Der Spulwurm zeigt dadurch seine Verwandtschaft zu verschiedenen Tropenwürmern, deren Larven über die Haut aufgenommen werden können, um dann auf demselben Weg zu ihrer eigentlichen Nahrungsquelle im Darm zu gelangen. |
|||
==== ''[[Ancylostoma duodenale]]'' und ''Necator americanus'', ''Strongyloides stercoralis'' ==== |
|||
Die Larven dieser Würmer können bei längerer Kontaktzeit (mindestens 20 Minuten) die Haut durchdringen, beispielsweise beim Barfußgehen über eine [[Kanalisation|Kloake]]. Ihr weiterer Vermehrungszyklus entspricht dann dem des Spulwurms. Der fertige Wurm legt im Darm Eier, aus denen noch im Darm Larven schlüpfen, die dann ausgeschieden werden. Beim Zwergfadenwurm durchdringen manche Larven wieder die Darmwand des [[Wirt (Biologie)|Wirtes]], um den Zyklus erneut zu durchlaufen (Autoinfektion). |
|||
==== ''Trichinella spiralis'' (Trichine) ==== |
|||
{{Hauptartikel|Trichinella spiralis|Trichinellose}} |
|||
Dieser Wurm produziert im Darm Larven, die die Darmwand durchdringen, sich über das Blut ausbreiten und in der Muskulatur Zysten (sehr feste Kapseln, die sich von Bindegewebszellen ernähren) bilden, um so vom nächsten Lebewesen aufgenommen zu werden. Der Vermehrungszyklus ähnelt damit dem des [[Schweinebandwurm]]s. |
|||
Infizieren kann man sich auch durch Verzehr befallenen Fleisches, was heutzutage durch Fleischbeschau selten geworden ist. |
|||
=== Bandwürmer (Cestoden) === |
|||
Bei [[Bandwürmer]]n wird unterschieden zwischen dem Endwirt, er trägt die Würmer im Darm, und dem Zwischenwirt. Der Zwischenwirt nimmt die Larven über verunreinigte Nahrung auf, sie durchdringen die Darmwand und setzten sich in der Muskulatur als [[Finnenstadium|Finnen]] ab, die so vom Endwirt (einem Raubtier) gefressen werden sollen. Da der Mensch normalerweise nicht gefressen wird, kommt er nur als Fehlzwischenwirt in Frage. |
|||
Der Mensch ist Endwirt beim [[Schweinebandwurm]] (''Taenia solium'') und beim [[Rinderbandwurm]] (''T. saginata''). Der [[Fischbandwurm]] (Diphyllobothrium latum) ist mittlerweile weitgehend ausgerottet. Der Wurm bildet im Darm mit dem Menschen eine [[Kommensalismus|Kommensale]]. Bandwürmer sind viel länger als Rundwürmer, der Patient findet ihre abgefallenen Proglottiden (Bandwurmglieder) im Stuhl. |
|||
Anders ist die Situation beim [[Dreigliedriger Hundebandwurm|Hundebandwurm]] (''Echinococcus granulosus'') und beim [[Fuchsbandwurm]] (''E. multilocolaris''), wo der Mensch [[Wirt (Biologie)#Fehlwirt|Fehlzwischenwirt]] ist. Die Finnen lagern sich meist in der Leber ab, können aber auch andere Organe betreffen und dort Beschwerden verursachen. Der Hundebandwurm kann operativ entfernt werden, die Finnen des Fuchsbandwurms sind in ihrem Wachstum schlechter abgrenzbar und führen unbehandelt auf Dauer zum Tode. |
|||
=== Bilharziose === |
|||
{{Hauptartikel|Schistosomiasis}} |
|||
Die Bilharziose oder [[Schistosomiasis]] kommt vor allem an Gewässern in Afrika, aber auch im nahen und fernen Osten vor. Erreger der Krankheit sind die [[Pärchenegel]], Saugwürmer der Gattung Schistosoma. |
|||
=== Fadenwürmer (Filarien) === |
|||
[[Filarioidea|Filarien]] sind nur einige Millimeter lang. ''[[Onchocerca volvulus]]'' und ''[[Loa loa]]'' leben unter der Haut. Die Weibchen gebären Mikrofilarien, die durch [[Insektenstich]] in die Haut des nächsten Wirtes übertragen werden. Sie können zu Erblindung führen. ''[[Wuchereria bancrofti]]'' und ''[[Brugia malayi]]'' leben in [[Lymphgefäß]]en. Im Laufe der Zeit entstehen dadurch Entzündungen, die zu [[Lymphe|Lymphstau]] und zum Krankheitsbild der [[Elefantiasis]] führen können. In Anpassung an die Flugzeit der jeweiligen [[Vektor (Biologie)|Vektoren]] sind die Mikrofilarien von ''Loa loa'' v. a. am Tag, die von ''Wuchereria bancrofti'' vor allem nachts im Blut nachzuweisen. |
|||
== Siehe auch == |
== Siehe auch == |
||
Version vom 6. April 2022, 17:43 Uhr
| Wurmerkrankung / Helminthiasis | |
|---|---|
| Medizinische Spezialität | Infektiologie |
Die Wurmerkrankung oder Helminthiasis (von altgriechisch ἕλμινς hélmins [Genitiv ἕλμινθος hélminthos] „Wurm“) ist jede makroparasitäre Erkrankung von Menschen und anderen Tieren, bei der ein Teil des Körpers mit parasitären Würmern infiziert ist, die als Helminthen bekannt sind. Es gibt zahlreiche Arten dieser Parasiten, die weitgehend in Bandwürmer, Egel und Spulwürmer eingeteilt sind. Sie leben oft im Magen-Darm-Trakt ihrer Wirte, aber sie können sich auch in andere Organe graben, wo sie physiologische Schäden verursachen.
Bodenübertragene Helminthiasis und Schistosomiasis sind die wichtigsten Helminthiasen und gehören zu den vernachlässigten Tropenkrankheiten.[1] Diese Gruppe von Helmianthiasen wurde im Rahmen der gemeinsamen Aktion der weltweit führenden Pharmaunternehmen und Nichtregierungsorganisationen durch ein 2012 gestartetes Projekt namens London Declaration on Neglected Tropical Diseases ins Visier genommen, das darauf abzielt, bestimmte vernachlässigte Tropenkrankheiten bis 2020 zu kontrollieren oder auszurotten.[2]
Helminthiasis führt zu einem schlechten Geburtsergebnis, einer schlechten kognitiven Entwicklung, einer schlechten Schul- und Arbeitsleistung, einer schlechten sozioökonomischen Entwicklung und Armut.[3][4] Chronische Erkrankungen, Unterernährung und Anämie sind weitere Beispiele für Nebenwirkungen.[5]
Bodenübertragene Helminthiasen sind für parasitäre Infektionen in bis zu einem Viertel der menschlichen Bevölkerung weltweit verantwortlich.[6] Ein bekanntes Beispiel für bodenübertragene Helminthiasen ist Ascariasis.
Anzeichen und Symptome
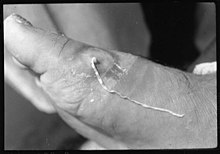

Die Anzeichen und Symptome der Helminthiasis hängen von einer Reihe von Faktoren ab, darunter: die Stelle des Befalls im Körper; die Art des beteiligten Wurms; die Anzahl der Würmer und ihr Volumen; die Art der Schäden, die die befallenden Würmer verursachen; und die immunologische Reaktion des Körpers. Wo die Belastung durch Parasiten im Körper leicht ist, gibt es möglicherweise keine Symptome.
Bestimmte Würmer können bestimmte Konstellationen von Symptomen verursachen. Zum Beispiel kann Taeniasis zu Anfällen aufgrund von Neurozystizerkose führen.[7]
Masse und Volumen
In extremen Fällen von Darmbefall können Masse und Volumen der Würmer dazu führen, dass die äußeren Schichten der Darmwand, wie die Muskelschicht, reißen. Dies kann zu Peritonitis, Volvulus und Gangrän des Darms führen.[8]
Immunologische Reaktion
Als Erreger im Körper induzieren Helminthen eine Immunantwort. Immunvermittelte entzündliche Veränderungen treten in Haut, Lunge, Leber, Darm, im Zentralnervensystem und in den Augen auf. Anzeichen der Immunantwort des Körpers können Eosinophilie, Ödem und Arthritis sein.[9] Ein Beispiel für die Immunantwort ist die Überempfindlichkeitsreaktion, die zu Anaphylaxie führen kann. Ein weiteres Beispiel ist die Migration von Ascaris-Larven durch die Bronchien der Lunge, die Asthma verursachen.[10]
Sekundäre Effekte

Immunveränderungen
Beim Menschen reagieren T-Helferzellen und Eosinophile auf Helminthenbefall. Es ist allgemein bekannt, dass T-Helfer-2-Zellen die zentralen Akteure der schützenden Immunität gegen Helminthen sind,[11] während die Rollen für B-Zellen und Antikörper kontextabhängig sind.[12] Entzündungen führen zur Verkapselung von Eiablagerungen im ganzen Körper. Helminthen scheiden toxische Substanzen nach der Fütterung in den Darm aus. Diese Substanzen gelangen dann in das Kreislauf- und Lymphsystem des Wirtskörpers.
Chronische Immunantworten auf Helminthiasis können zu einer erhöhten Anfälligkeit für andere Infektionen wie Tuberkulose, HIV und Malaria führen.[13][14][15] Es gibt widersprüchliche Informationen darüber, ob die Entwurmung die HIV-Progression und die Viruslast reduziert und die CD4-Zahl bei antiretroviralen naiven und erfahrenen Personen erhöht, obwohl die jüngste Cochrane-Überprüfung einige Hinweise darauf ergab, dass dieser Ansatz positive Auswirkungen haben könnte.[16][17]
Chronische Krankheiten
Chronische Helminthiasis kann schwere Morbidität verursachen.[18] Es wurde festgestellt, dass Helminthiasis zu einem schlechten Geburtsergebnis, einer schlechten kognitiven Entwicklung, einer schlechten Schul- und Arbeitsleistung, einer verminderten Produktivität, einer schlechten sozioökonomischen Entwicklung und Armut führt.[3][4][5]
Unterernährung
Helminthiasis kann chronische Krankheiten durch Unterernährung verursachen, einschließlich Vitaminmangel, verkümmertes Wachstum, Anämie und Protein-Energie-Unterernährung. Würmer konkurrieren direkt mit ihren Wirten um Nährstoffe, aber das Ausmaß dieses Effekts ist wahrscheinlich minimal, da der Nährstoffbedarf von Würmern relativ gering ist.[19][20][21] Bei Schweinen und Menschen wurde Ascaris mit Laktoseintoleranz und Vitamin A, Aminosäure und Fett-Malassimilation in Verbindung gebracht.[3] Eine beeinträchtigte Nährstoffaufnahme kann durch direkte Schäden an der Darmschleimhautwand oder aus subtileren Veränderungen wie chemischen Ungleichgewichten und Veränderungen der Darmflora resultieren.[22] Alternativ kann die Freisetzung von Proteasehemmern durch die Würmer zur Abwehr der Verdauungsprozesse des Körpers den Abbau anderer Nährstoffe beeinträchtigen.[19][21] Darüber hinaus kann wurminduzierter Durchfall die Darmtransitzeit verkürzen und so die Aufnahme von Nährstoffen reduzieren.[3]
Unterernährung aufgrund von Würmern kann zu Magersucht führen.[20] Eine Studie mit 459 Kindern in Sansibar ergab einen spontanen Appetitanstieg nach der Entwurmung.[23] Magersucht könnte eine Folge der Immunantwort des Körpers und des Stresses bei der Bekämpfung von Infektionen sein.[21] Insbesondere wurden einige der Zytokine, die in der Immunantwort auf Wurmbefall freigesetzt werden, mit Magersucht bei Tieren in Verbindung gebracht.[19]
Siehe auch
- Bandwurmerkrankungen des Hundes
- Fadenwurminfektionen des Hundes
- Wurminfektionen der Katze
- Hakenwürmer
- Zwergfadenwurm
- Zahnwurm
- Helminthologie
Einzelnachweise
- ↑ CDC - Neglected Tropical Diseases - Diseases. 7. März 2022, abgerufen am 6. April 2022 (amerikanisches Englisch).
- ↑ London Declaration on Neglected Tropical Diseases. 30. Januar 2012, abgerufen am 6. April 2022.
- ↑ a b c d Prevention and Control of Intestinal Parasitic Infections. 1987, abgerufen am 6. April 2022.
- ↑ a b Joy Miller Del Rosso, Tonia Marek: Class Action: Improving School Performance in the Developing World Through Better Health and Nutrition. World Bank Publications, 1996, ISBN 978-0-8213-3672-4 (google.com [abgerufen am 6. April 2022]).
- ↑ a b World Health Organization, TDR Disease Reference Group on Helminth Infections: Research priorities for helminth infections. In: World Health Organization Technical Report Series. Nr. 972, 2012, ISSN 0512-3054, S. xv–xvii, 1–174, back cover, PMID 23420950 (nih.gov [abgerufen am 6. April 2022]).
- ↑ WHO | Soil-transmitted helminth infections. 20. August 2012, abgerufen am 6. April 2022.
- ↑ Oscar H. Del Brutto: Neurocysticercosis: a review. In: TheScientificWorldJournal. Band 2012, 2012, ISSN 1537-744X, S. 159821, doi:10.1100/2012/159821, PMID 22312322, PMC 3261519 (freier Volltext) – (nih.gov [abgerufen am 6. April 2022]).
- ↑ T. E. Madiba, G. P. Hadley: Surgical management of worm volvulus. In: South African Journal of Surgery. Suid-Afrikaanse Tydskrif Vir Chirurgie. Band 34, Nr. 1, Februar 1996, ISSN 0038-2361, S. 33–35; discussion 35–36, PMID 8629187 (nih.gov [abgerufen am 6. April 2022]).
- ↑ P. L. Minciullo, A. Cascio, A. David, L. M. Pernice, G. Calapai: Anaphylaxis caused by helminths: review of the literature. In: European Review for Medical and Pharmacological Sciences. Band 16, Nr. 11, Oktober 2012, ISSN 1128-3602, S. 1513–1518, PMID 23111963 (nih.gov [abgerufen am 6. April 2022]).
- ↑ David T. John: Markell and Voge's medical parasitology. 9th ed Auflage. Saunders Elsevier, St. Louis, Mo. 2006, ISBN 978-0-7216-4793-7.
- ↑ Alba Cortés, Carla Muñoz-Antoli, J. Guillermo Esteban, Rafael Toledo: Th2 and Th1 Responses: Clear and Hidden Sides of Immunity Against Intestinal Helminths. In: Trends in Parasitology. Band 33, Nr. 9, September 2017, ISSN 1471-5007, S. 678–693, doi:10.1016/j.pt.2017.05.004, PMID 28566191 (nih.gov [abgerufen am 6. April 2022]).
- ↑ Aidil Zaini, Kim L. Good-Jacobson, Colby Zaph: Context-dependent roles of B cells during intestinal helminth infection. In: PLoS neglected tropical diseases. Band 15, Nr. 5, Mai 2021, ISSN 1935-2735, S. e0009340, doi:10.1371/journal.pntd.0009340, PMID 33983946, PMC 8118336 (freier Volltext) – (nih.gov [abgerufen am 6. April 2022]).
- ↑ Elly van Riet, Franca C. Hartgers, Maria Yazdanbakhsh: Chronic helminth infections induce immunomodulation: consequences and mechanisms. In: Immunobiology. Band 212, Nr. 6, 2007, ISSN 0171-2985, S. 475–490, doi:10.1016/j.imbio.2007.03.009, PMID 17544832 (nih.gov [abgerufen am 6. April 2022]).
- ↑ Zilungile L. Mkhize-Kwitshana, Musawenkosi H. L. Mabaso: Status of medical parasitology in South Africa: new challenges and missed opportunities. In: Trends in Parasitology. Band 28, Nr. 6, Juni 2012, ISSN 1471-5007, S. 217–219, doi:10.1016/j.pt.2012.03.005, PMID 22525798 (nih.gov [abgerufen am 6. April 2022]).
- ↑ G. Borkow, Z. Bentwich: Eradication of helminthic infections may be essential for successful vaccination against HIV and tuberculosis. In: Bulletin of the World Health Organization. Band 78, Nr. 11, 2000, ISSN 0042-9686, S. 1368–1369, PMID 11143198, PMC 2560630 (freier Volltext) – (nih.gov [abgerufen am 6. April 2022]).
- ↑ Alexander J. Lankowski, Alexander C. Tsai, Michael Kanyesigye, Mwebesa Bwana, Jessica E. Haberer: Empiric deworming and CD4 count recovery in HIV-infected Ugandans initiating antiretroviral therapy. In: PLoS neglected tropical diseases. Band 8, Nr. 8, August 2014, ISSN 1935-2735, S. e3036, doi:10.1371/journal.pntd.0003036, PMID 25101890, PMC 4125278 (freier Volltext) – (nih.gov [abgerufen am 6. April 2022]).
- ↑ Arianna Rubin Means, Paul Burns, David Sinclair, Judd L. Walson: Antihelminthics in helminth-endemic areas: effects on HIV disease progression. In: The Cochrane Database of Systematic Reviews. Band 4, 14. April 2016, ISSN 1469-493X, S. CD006419, doi:10.1002/14651858.CD006419.pub4, PMID 27075622, PMC 4963621 (freier Volltext) – (nih.gov [abgerufen am 6. April 2022]).
- ↑ Derek Wakelin: Helminths: Pathogenesis and Defenses. In: Medical Microbiology. 4th Auflage. University of Texas Medical Branch at Galveston, Galveston (TX) 1996, ISBN 978-0-9631172-1-2, PMID 21413312 (nih.gov [abgerufen am 6. April 2022]).
- ↑ a b c Levinger B: Nutrition, Health, and Learning: Current Issues and Trends (PDF). , abgerufen am 6. April 2022.
- ↑ a b World Development Report 1993: Investing in Health (PDF). Abgerufen am 6. April 2022.
- ↑ a b c W. E. Watkins, E. Pollitt: "Stupidity or worms": do intestinal worms impair mental performance? In: Psychological Bulletin. Band 121, Nr. 2, März 1997, ISSN 0033-2909, S. 171–191, doi:10.1037/0033-2909.121.2.171, PMID 9100486 (nih.gov [abgerufen am 6. April 2022]).
- ↑ D. W. T. Crompton, David William Thomasson Crompton: Human Nutrition and Parasitic Infection: Volume 107, Parasitology Supplement 1993. Cambridge University Press, 1994, ISBN 978-0-521-45601-2 (google.com [abgerufen am 6. April 2022]).
- ↑ Rebecca J. Stoltzfus, Hababu M. Chway, Antonio Montresor, James M. Tielsch, Jape Khatib Jape: Low dose daily iron supplementation improves iron status and appetite but not anemia, whereas quarterly anthelminthic treatment improves growth, appetite and anemia in Zanzibari preschool children. In: The Journal of Nutrition. Band 134, Nr. 2, Februar 2004, ISSN 0022-3166, S. 348–356, doi:10.1093/jn/134.2.348, PMID 14747671 (nih.gov [abgerufen am 6. April 2022]).
