Blutgerinnungsfaktor VIII
| Gerinnungsfaktor VIII | ||
|---|---|---|
| ||
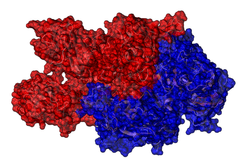
| Bänder- bzw. Oberflächenmodell von Faktor VIII (ohne B-Kette) nach PDB 3CDZ. Die leichte Kette ist rot, die schwere blau markiert. | ||
|
Vorhandene Strukturdaten: 1cfg, 1d7p, 1iqd, 1fac, 2r7e, 3cdz | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 265 kDa/2332 AS | |
| Kofaktor | Von-Willebrand-Faktor | |
| Bezeichner | ||
| Gen-Namen | F8 ; AHF; DXS1253E; F8 protein; F8B; F8C; FVIII; HEMA | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | B02BD02 | |
| DrugBank | DB00025 | |
| Vorkommen | ||
| Homologie-Familie | Gerinnungsfaktor 5 | |
| Übergeordnetes Taxon | Euteleostomi | |
Blutgerinnungsfaktor VIII (Gerinnungsfaktor VIII, Faktor VIII, F8), auch Antihämophiles Globulin A, ist ein Glykoprotein und ein Gerinnungsfaktor bei Wirbeltieren. Ein akuter Mangel bzw. Fehlen des Gerinnungsfaktors beim Menschen führt zur Hämophilie A (sog. Bluterkrankheit). Ursache ist immer eine Mutation im F8-Gen, das für den Faktor VIII codiert. Eine intravenöse Zufuhr dieses Blutgerinnungsfaktors war bis zur Markteinführung von Emicizumab im Jahr 2018 die einzige kausale Therapie für Bluterkranke und stellt auch heute noch die häufigste Therapieform dar. Bis Ende der 1980er-Jahre wurde Faktor VIII ausschließlich aus gespendetem humanem Blutplasma gewonnen, heute stehen auch mehrere gentechnisch hergestellte Präparate zur Verfügung.
Auch Erhöhungen der Faktor-VIII-Aktivität auf Werte über 150 % besitzen Krankheitswert und führen zu erhöhter Thrombose-Gefahr, z. B. wurden in Studien bei rund 20 % der Frauen mit PCO-Syndrom diese erhöhte Aktivität gefunden.[1]
Faktor VIII stand in den 1980er Jahren im Mittelpunkt eines der größten Arzneimittelskandale Deutschlands und weltweit, des sogenannten „Blut(er)skandals“, bei dem – zum großen Teil bewusst – verunreinigte Faktor-VIII-Präparate vertrieben und verabreicht wurden, obwohl Verantwortlichen in Pharmaindustrie, Medizin und Politik früh bekannt war, dass diese Präparate HIV- und Hepatitis-Infektionen verursachen würden.
Biosynthese[Bearbeiten | Quelltext bearbeiten]
Der Syntheseort des Faktor VIII ist noch nicht vollständig geklärt. Als Syntheseorte werden neben den Lebersinusoiden auch das Endothel und die Thrombozyten diskutiert, wobei letztere nach neuen Studien an Knockout-Mäusen als wahrscheinlich hauptsächlicher Syntheseort in Frage kommen.[2] Der Abbau findet in Leber und Niere statt.[3][4][5]
Das F8-Gen umspannt 187000 Basenpaare in 26 Exons. Die transkribierte mRNA ist 9029 Basen lang und wird in ein Protein mit 2351 Aminosäuren translatiert, von dem durch posttranslationale Modifikation weitere 19 Aminosäuren entfernt werden.[6]
Das Faktor-VIII-Molekül wird an 31 Aminosäureseitenketten mit komplexen Zuckermolekülen modifiziert (25 × N-Glykosylierung, 6 × O-Glykosylierung), die Aminosäurekette wird schließlich durch spezifische Proteasen an zwei Stellen geschnitten. Das fertige Molekül besteht aus zwei Ketten von 200 kDa und 80 kDa.
Biologische Funktion[Bearbeiten | Quelltext bearbeiten]
Faktor VIII, zusammen mit Calcium und Phospholipiden (die bei Verletzungen entstehen) sind die Kofaktoren für Faktor IXa, der notwendig ist, um Faktor X zu aktivieren. Dieser Reaktionsschritt ist essentiell für die Blutgerinnung, denn Faktor Xa aktiviert im Komplex mit Faktor Va Prothrombin zu Thrombin und dieses setzt Fibrin aus Fibrinogen frei.
Pharmakologie[Bearbeiten | Quelltext bearbeiten]
Die Substitution von Faktor VIII (intravenöse Applikation) ist für Hämophilie-A-Patienten die Therapie der Wahl. Bis zum Jahr 1992 wurde Faktor VIII ausschließlich aus humanem Blutplasma hergestellt. Inzwischen stehen neben den aus Plasma gewonnenen auch gentechnisch erzeugte Faktorkonzentrate wie Octocog-alfa zur Verfügung.
Herstellung aus Plasma[Bearbeiten | Quelltext bearbeiten]
Faktor VIII wird aus humanem Plasma durch Kältefällung (Kryopräzipitation) gewonnen und anschließend chromatographisch gereinigt. Ein wichtiges Ziel in der Produktion ist die Inaktivierung potentieller Pathogene (z. B. Viren). Neben der Selektion der Spender und dem Test des verarbeiteten Plasmas gehören inaktivierende Produktionsschritte wie Lösungsmittel-, Detergenz-Behandlung (S/D-Verfahren, Inaktivierung umhüllter Viren), Hitze und/oder Nanofiltration zum heutigen Sicherheitsstandard.
Octocog alfa[Bearbeiten | Quelltext bearbeiten]
Octocog alfa (INN) ist rekombinant hergestellter humaner Faktor VIII, der als Arzneistoff identische Anwendungsgebiete zum aus Plasma hergestellten Faktor VIII hat. Chemisch unterscheidet er sich nur unwesentlich von diesem. Die folgenden Ausführungen gelten daher auch für Octocog alfa.
Octocog alfa wird nicht aus humanen Blutplasma extrahiert, sondern mittels rekombinanter DNA-Technologie hergestellt: Es wird von einer Zelle produziert, in die ein Gen eingeschleust wurde, das sie zur Expression des humanen Gerinnungsfaktors VIII befähigt (siehe auch Pharmazeutische Biotechnologie).
Dosierung, Art und Dauer der Anwendung[Bearbeiten | Quelltext bearbeiten]
Die Dosierung und Häufigkeit der Anwendung richtet sich danach, ob Faktor VIII zur Behandlung von Blutungen, zur Prophylaxe von Blutungen oder im Rahmen eines chirurgischen Eingriffes eingesetzt wird. Die Dosierung wird darüber hinaus abhängig vom Schweregrad der Blutung und der Art des chirurgischen Eingriffes angepasst.
Gegenanzeigen[Bearbeiten | Quelltext bearbeiten]
Kontraindiziert sind alle Analgetika mit thrombozytenaggregationshemmender Wirkung, besonders Acetylsalicylsäure. Indiziert sind beispielsweise Dextropropoxyphen, Tilidin + Naloxon, Pentetocin, Buprenorphin, Paracetamol, Diclofenac.
Unerwünschte Wirkungen[Bearbeiten | Quelltext bearbeiten]
Patienten mit Hämophilie A können Antikörper (Inhibitoren) gegenüber Faktor VIII bilden, wodurch dieser komplett oder partiell inaktiviert wird. Dies führt zu einer so genannten „Hemmkörperhämophilie“, einer Blutung trotz Anwendung üblicher Faktordosierungen. Patienten mit solchen Hemmkörpern werden in Low Responder und High Responder eingeteilt. Hemmkörper können sich spontan zurückbilden, bei Low Respondern eher als bei High Respondern. Die Behandlung der akuten Blutung ist symptomatisch. Die kausale Behandlung besteht in der Elimination oder Reduktion der Hemmkörper durch Erzeugung einer Immuntoleranz (Immuntoleranzinduktion, ITI) und sollte immer angestrebt werden. Seit Februar 2018 steht in Europa mit dem bispezifischem Antikörper Emicizumab eine neuartige Therapieoption für die sekundäre Hemmkörperhämophilie bei Hämophilie A-Patienten zur Verfügung.[7]
Sowohl bei der symptomatischen Behandlung der akuten Blutung als auch bei der Hemmkörperelimination müssen Faktorenkonzentrate hoch dosiert verabreicht werden.
Auf dem Markt gibt es den gentechnischen Blutgerinnungsfaktor VIII in unterschiedlichen Varianten. Diese werden in eine 1., 2. und 3. Generation unterteilt. Octocog alfa gehört zur 2. Generation. In der 2013 veröffentlichten RODIN-Studie wurde die Behandlung mit Präparaten der 2. Generation mit einer häufigeren Bildung inhibitorischer Antikörper assoziiert im Vergleich zur Behandlung mit Präparaten der 3. Generation.[8] Der Pharmakovigilanzausschuss der Europäischen Arzneimittelagentur hingegen fand keine ausreichende Evidenz für ein unterschiedlich häufiges Auftreten einer Antikörperbildung, empfahl aber dennoch die Produktinformation anzupassen, um die Ergebnisse der Studie widerzuspiegeln.[9]
Bei einer allergischen Reaktion nach Infusionsbeginn muss die Infusion gestoppt und auf ein anderes Präparat gewechselt werden. Bei einer anaphylaktischen Reaktion gelten die üblichen Notfallbehandlungsmaßnahmen.
„Blut(er)skandal“ in den 1980er Jahren[Bearbeiten | Quelltext bearbeiten]
In den 1980er Jahren kam es durch verunreinigtes Spenderblut bei Hämophilen weltweit zu HIV- und Hepatitis-Infektionen – anfänglich aufgrund von Unkenntnis, später vor allem durch Fahrlässigkeit, bewusstes Ignorieren von Warnungen und Profitsucht.[10] In Deutschland wurden damals über 43 % aller Hämophilen mit HIV infiziert.[11] Dies wurde in einigen Ländern als „Blut(er)skandal“ bekannt, da Pharmaindustrie und Politik die ihnen bekannten Verunreinigungen und die damit einhergehenden Risiken vor der Öffentlichkeit verschwiegen und so einen – neben dem Contergan-Fall – der größten medizinischen Skandale verursachten, infolgedessen weltweit mindestens 10.000 damals mit HIV infizierte Hämophile allein bis Mitte der 2000er Jahre verstarben. Obwohl es bereits ab März 1983 fachliche Warnungen vor verunreinigten Präparaten gab und zum Beispiel die Verantwortlichen bei der zuständigen Tochterfirma der Bayer AG bereits im Januar 1983 in internen Schriftsätzen vor der Übertragung durch kontaminierte Faktor-VIII-Blutpräparate hinwiesen, wurden mindestens bis Sommer 1985 infektiöse Präparate vertrieben und entsprechend verabreicht.[12][13]
In Deutschland wurde 1993, also rund zehn Jahre später, vom Deutschen Bundestag ein spezifischer Untersuchungsausschuss „HIV-Infektionen durch Blut und Blutprodukte“ eingerichtet. Im Oktober 1993 wurde der damalige Präsident des Bundesgesundheitsamtes Dieter Großklaus entlassen[14] und das Amt selbst Ende Juni 1994 aufgelöst. Zu dieser Zeit waren bereits mehr als 400 der im fraglichen Zeitraum infizierten Hämophilen an einer HIV-Infektion verstorben. Andere handelnde Personen des Skandals aus der Pharmaindustrie, Medizin und Politik wurden in Deutschland nicht juristisch belangt.[15] 2013 wurde dieser Skandal durch das ZDF in dem fiktiven Fernsehfilm Blutgeld und einer dazugehörigen Dokumentation verarbeitet. Darüber hinaus thematisiert auch der Spielfilm „Unter der Haut“ (2015), mit Friedrich Mücke in der Hauptrolle, das fahrlässige Verhalten, mit der die Pharmaindustrie das Krankheitsrisiko billigte.[16]
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Öffentlicher Beurteilungsbericht (EPAR) der europäischen Arzneimittelagentur (EMA) zu: octocog alpha
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ C. J. Glueck, P. Wang, N. Goldenberg, L. Sieve: Pregnancy loss, polycystic ovary syndrome, thrombophilia, hypofibrinolysis, enoxaparin, metformin. In: Clinical and applied thrombosis/hemostasis. Band 10, Nummer 4, Oktober 2004, S. 323–334. PMID 15497018.
- ↑ S. A. Fahs, M. T. Hille, Q. Shi, H. Weiler, R. R. Montgomery: A conditional knockout mouse model reveals endothelial cells as the principal and possibly exclusive source of plasma factor VIII. In: Blood. Band 123, Nummer 24, Juni 2014, S. 3706–3713. PMID 24705491.
- ↑ Charité: Parameterbestimmung im Blut ( vom 11. Februar 2013 im Webarchiv archive.today)
- ↑ Blutgerinnungsfaktor VIII. In: Online Mendelian Inheritance in Man. (englisch).
- ↑ AOK über Faktor VIII Blutwert
- ↑ ENSEMBL-Eintrag
- ↑ Emicizumab (Hemlibra®) ▼. In: Arzneiverordnung in der Praxis / Ausgabe 3/2018. Arzneimittelkommission der deutschen Ärzteschaft, 28. Mai 2018, abgerufen am 11. April 2024.
- ↑ Samantha C. Gouw, Johanna G. van der Bom, Rolf Ljung, Carmen Escuriola, Ana R. Cid, S gol ne Claeyssens-Donadel, Christel van Geet, Gili Kenet, Anne M kipernaa, Angelo Claudio Molinari, Wolfgang Muntean, Rainer Kobelt, George Rivard, Elena Santagostino, Angela Thomas, H. Marijke van den Berg: Factor VIII Products and Inhibitor Development in Severe Hemophilia A. In: New England Journal of Medicine. 368, 2013, S. 231–239, doi:10.1056/NEJMoa1208024.
- ↑ EMA: PRAC considers benefits of Kogenate Bayer/Helixate NexGen outweigh risks in previously untreated patients.
- ↑ Advate: European Public Assessment Report / Product Information. European Medicines Agency, 10. November 2005, archiviert vom am 20. November 2006; abgerufen am 7. Dezember 2016.
- ↑ Barbara Möller: TV-Film „Blutgeld“: „Alle handelnden Personen sind frei erfunden“. In: Die Welt., 28. Oktober 2013, abgerufen am 7. Dezember 2016.
- ↑ Walt Bogdanich, Eric Koli: 2 Paths of Bayer Drug in 80's: Riskier One Steered Overseas. In: The New York Times. 22. Mai 2003, abgerufen am 17. Januar 2014.
- ↑ Aids scandals around the world. In: BBC News. 9. August 2001.
- ↑ AIDS-Skandal: Tödlicher Cocktail. In: Focus. 31, 1. August 1994, S. 40–43, abgerufen am 7. Dezember 2016.
- ↑ Die Geschichte des Blut-AIDS-Skandals in Deutschland. Interessengemeinschaft Hämophiler e. V., 9. Mai 2000, archiviert vom am 14. November 2011; abgerufen am 7. Dezember 2016.
Wolfgang Hoffmann: Seehofer bleibt stur. In: Zeit online. 28. Januar 1999, abgerufen am 7. Dezember 2016. - ↑ Michael Hanfeld: Aidskrank durch Medikamente. In: Frankfurter Allgemeine Zeitung. 2. Dezember 2015, abgerufen am 29. Mai 2016.