2-Hydroxy-4-methylthiobuttersäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Vereinfachte Strukturformel ohne Stereochemie – 1:1-Gemisch der Enantiomeren | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2-Hydroxy-4-(methylthio)buttersäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C5H10O3S | ||||||||||||||||||
| Kurzbeschreibung |
gelbe bis braune Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 150,2 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
löslich sich vollständig in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
2-Hydroxy-4-methylthiobuttersäure ist das racemische Hydroxyanalogon der natürlich vorkommenden schwefelhaltigen essentiellen proteinogenen Aminosäure L-Methionin. Die funktionelle Hydroxycarbonsäure HMTBA kann von Tieren aus dem Futter resorbiert und in L-Methionin umgewandelt werden, das die Proteinbildung fördert und zur Steigerung des Milcheiweißgehalts bei Wiederkäuern und zum schnelleren Wachstum anderer Tiere, z. B. Geflügel und Fische, eingesetzt wird.
Vorkommen und Darstellung
[Bearbeiten | Quelltext bearbeiten]Die erhebliche Bedeutung von Methionin-Ersatzstoffen in der Nutztierernährung hat zur Untersuchung mehrerer enzymatischer und chemischer Synthesewege geführt, von denen sich die erstmals 1956 patentierte Route[3] über Methylmercaptopropionaldehyd MMP (durch Michael-Addition von Methylmercaptan an Acrolein) im industriellen Maßstab als Standardverfahren etabliert hat.
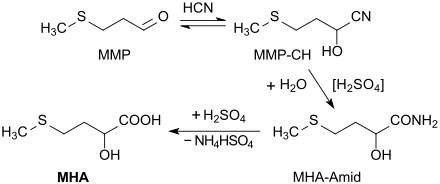
In einer Cyanhydrinsynthese addiert Blausäure HCN bei pH 7,5 praktisch quantitativ an MMP unter Bildung von 2-Hydroxy-4-methylthiobutyronitril (auch als MMP-Cyanhydrin oder MMP-CH bezeichnet). Die Cyanogruppe wird zunächst mit 65%iger Schwefelsäure bei 50 °C zur Amidgruppe und anschließend mit Wasser verdünnt und bei 90 °C zur Carboxygruppe hydrolysiert. Die Reaktionen zum MHA-Amid und weiter zur Säure MHA verlaufen ebenfalls mit sehr hoher Ausbeute zu > 98 % 2-Hydroxy-4-methylthiobuttersäure, die ca. 15 % MHA-Ester (so genannte MHA-Oligomere) – überwiegend das MHA-Dimer – enthalten.
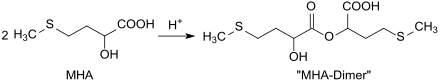
Das Reaktionsprodukt ist eine gelbe bis braune viskose Lösung von MHA in Wasser, das äquimolare Mengen Ammoniumhydrogensulfat NH4HSO4 enthält, das mit Ammoniak oder Ammoniumhydroxid zu Ammoniumsulfat (NH4)2SO4 reagiert.[4] Bei schonendem Entfernen des Wassers unter Vakuum entsteht eine Suspension mit kristallinem Ammoniumsulfat, aus der durch Extraktion, z. B. mit Aceton, das organische Produkt abgetrennt werden kann. Das vom Extraktionsmittel befreite Produkt ist eine gelb-braune Flüssigkeit, deren Viskosität stark vom Gehalt an Oligomeren abhängt.[5] Zur weiteren Reinigung kann die rohe Hydroxycarbonsäure möglichst schonend (zur Vermeidung der Bildung von Oligomeren, die den Nährwert von HMB reduzieren) im Vakuum destilliert werden, wobei farblose und lagerstabile MHA erhalten wird.
In der industriellen Praxis wird die MHA-Synthese in einem kontinuierlichen Prozess durchgeführt.
Das bei der Cyanhydrinhydrolyse – ebenso wie bei der Hydrolyse von Acetoncyanhydrin zum Endprodukt Methacrylsäuremethylester MMA – in äquimolaren Mengen anfallende Ammoniumsulfat stellt bei anderen Verfahrensvarianten ein erhebliches Abwasser- bzw. Entsorgungsproblem dar. Das reine Ammoniumsulfat kann entweder als Düngemittel genutzt oder thermisch zu Ammoniak und Schwefelsäure zerlegt werden,[6] die beide dem Prozess wieder zugeführt werden können.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2-Hydroxy-4-methylthiobuttersäure ist eine gelbe bis braune, viskose Flüssigkeit mit stechendem schwefelartigem Geruch, die stark sauer reagiert (pH <1 in 100%iger Form).[1] Handelsübliche HMTBA ist ein auf 88 % Gehalt eingestelltes wässriges, fließfähiges Konzentrat, das weniger als 17 % Oligomere enthält und sich noch leicht auf granuliertes oder pelletiertes Tierfutter versprühen lässt. Bei längerer Lagerung entstehen aus MHA oligomere intermolekulare Ester, deren Konzentration bis auf ca. 50 % steigen kann.
Anwendungen
[Bearbeiten | Quelltext bearbeiten]DL-2-Hydroxy-4-methylthiobuttersäure wird nach Resorption im tierischen Organismus durch Oxidation zur α-Ketosäure und Transaminierung zur Aminosäure L-Methionin (Met) umgewandelt. Im Zellstoffwechsel spielt Met eine wichtige Rolle als Antioxidans[7] und als Schwefelquelle, z. B. für die Aminosäure Cystein oder das Tripeptid Glutathion, oder als Methylgruppen-Donor, z. B. für Cholin, ist jedoch in vielen Futterquellen für Nutztiere nicht ausreichend vorhanden.
Während L-Methionin und das Racemat DL-Met durch aktiven Transport im Magen und Duodenum resorbiert wird, kann MHA sowohl durch aktiven Transport wie auch durch passive Diffusion absorbiert und im Wesentlichen in der Leber in L-Met metabolisiert werden.
Befunde aus umfangreichen Studien weisen darauf hin, dass 2-Hydroxy-4-methylthiobuttersäure eine brauchbare Quelle für die Proteinsynthese von Nicht-Wiederkäuern und Fischen darstellt, aber eine geringere biologische Wirksamkeit als DL-Methionin besitzt. Bei Wiederkäuern (Rindern, Schafen, Ziegen) wird MHA im Pansen langsamer abgebaut als DL-Met.[8]
Die 88 %ige MHA soll auf Vergleichsbasis ca. 20 % billiger sein als DL-Methionin. Sie spart auf Grund ihrer Acidität Futterzusätze von organischen Säuren, z. B. Milchsäure, und hemmt das Wachstum von Pilzen und pathogenen Bakterien im Futter. Die Gabe von HMTBA führt zu einer geringeren Stickstoffausscheidung der damit gefütterten Tiere.
Das Calciumsalz der 2-Hydroxy-4-methylthiobuttersäure ist ein Feststoff mit vergleichbaren Wirkungen wie MHA.[8]
Der als HMBi bezeichnete Isopropylester von HMB ist in flüssiger (95 % HMBi) und fester Form (57 % HMBi) verfügbar[9] und wird im Pansen von Rindern langsamer und in geringerem Umfang abgebaut als die Säure MHA (und als DL-Met). Der Ester wird zu 50 % im Pansen verstoffwechselt und zu 50 % durch die Pansenwand absorbiert und in der Leber zu L-Met umgewandelt. Bei der Verabreichung an Milchkühe soll HMBi den Protein- und Fettgehalt erhöhen.[10]
Hersteller und Handelsnamen
[Bearbeiten | Quelltext bearbeiten]2-Hydroxy-4-methylthiobuttersäure wird von Adisseo, einem Tochterunternehmen der ChemChina, unter dem Markennamen Rhodimet® AT 88,[1] von Novus International Inc., einem Gemeinschaftsunternehmen der Mitsui & Co., Ltd. und der Nippon Sōda, unter dem Markennamen ALIMET®[2] und von Sumitomo Chemical unter dem Markennamen SUMIMET™-L hergestellt und im Wesentlichen als Futtersupplement für Schweine, Geflügel und Tiere in Aquakulturen (Fische, Shrimps) vermarktet.
Der Isopropylester der 2-Hydrox-4-methylthiobuttersäure wird von Adisseo als MetaSmart® für Milchkühe vertrieben.
Das Calciumsalz der 2-Hydrox-4-methylthiobuttersäure wird von Adisseo als ADRY+® und Novus als MFP® für Tierfutter, sowie von Evonik unter dem REXIM®-Markennamen als DL-alpha-Hydroxymethionine, Calcium salt – zusammen mit L-Methionin und anderen Aminosäuren – zur Behandlung von chronischem Nierenversagen angeboten.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Safety Data Sheet Rhodimet AT 88 (liquid HMB). (PDF; 87 kB) Adisseo Canada Inc., 8. August 2018, abgerufen am 15. Mai 2020 (englisch).
- ↑ a b c GPS Safety Summary ALIMET®. (PDF; 87 kB) Novus International, Inc., 1. Dezember 2015, abgerufen am 15. Mai 2020 (englisch).
- ↑ Patent US2745745: Poultry feed. Angemeldet am 30. Oktober 1952, veröffentlicht am 15. Mai 1956, Anmelder: Monsanto Chemical Co., Erfinder: E.S. Blake, R.J. Wineman.
- ↑ Patent US4912257: Process for the preparation of aqueous solutions of 2-hydroxy-4-methylthio butyric acid. Angemeldet am 13. Februar 1989, veröffentlicht am 27. März 1990, Anmelder: Sociedad de Desarrollo Tecnico Industrial, Erfinder: J.A. Hernandez, L.R. Moreno.
- ↑ Patent WO199605173: Verfahren zur Herstellung von 2-Hydroxy-4-methylthiobuttersäure (MHA) und dessen Verwendung als Tierfuttermittelsupplement. Angemeldet am 12. August 1994, veröffentlicht am 22. Februar 1996, Anmelder: Degussa AG, Erfinder: H. Suchsland, V. Häfner.
- ↑ Patent EP1444166B1: Chemische und thermische Zersetzung von Ammoniumsulfat zu Ammoniak und Schwefelsäure. Angemeldet am 26. September 2002, veröffentlicht am 5. September 2007, Anmelder: Silica Tech ANS, Erfinder: T. Hansen.
- ↑ R. L. Levine, J. Moskovitz, E. R. Stadtman: Oxidation of methionine in proteins: roles in antioxidant defense and cellular regulation. In: IUBMB Life. Band 50, Nr. 4–5, 2000, S. 301–307, doi:10.1080/713803735.
- ↑ a b EFSA Panel on Additives and Products or Substances used in Animal Feed (FEEDAP): Safety and efficacy of hydroxy analogue of methionine and its calcium salt (ADRY+®) for all animal species. In: EFSA Journal. Band 16, Nr. 3, 2018, S. 5198, doi:10.2903/j.efsa.2018.5198.
- ↑ MetaSmart®, The unique isopropyl methionine analog for ruminants. (PDF; 5,5 MB) Adisseo, 2015, abgerufen am 15. Mai 2020 (englisch).
- ↑ Z.H. Chen, G.A. Broderick, N.D. Luchini, B.K. Sloan, E. Devillard: Effect of feeding different sources of rumen-protected methionine on milk production and N-utilization in lactating dairy cows. In: J. Dairy Sci. Band 94, Nr. 4, 2011, S. 1978–1988, doi:10.3168/jds.2010-3578.
