Essigsäuremethylester
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Essigsäuremethylester | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C3H6O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit fruchtigem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 74,08 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[2] | ||||||||||||||||||
| Dichte |
0,93 g·cm−3 [2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
57 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
leicht in Wasser (240–250 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Brechungsindex |
1,3614 (20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−445,9 kJ/mol[6] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Essigsäuremethylester (nach IUPAC-Nomenklatur: Methylacetat, systematisch als Methylethanoat bezeichnet) ist eine organisch-chemische Verbindung aus der Stoffgruppe der Carbonsäureester.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Industriell fällt eine große Menge an Methylacetat bei der Herstellung von Essigsäure durch Carbonylierung von Methanol als Nebenprodukt an.[7]
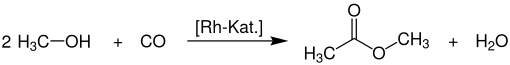
Bei diesem Prozess handelt es sich um das Monsanto- bzw. weiterentwickelte Cativa-Verfahren zur großtechnischen Herstellung von Essigsäure durch Carbonylierung von Methanol unter Rhodium- oder Iridiumkomplex-Katalyse.[7]
Methylacetat lässt sich daneben auch durch die direkte säurekatalysierte Veresterung von Essigsäure mit Methanol unter Reaktivdestillation herstellen.[7]
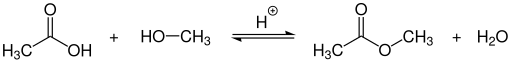
Als Katalysatoren werden neben Mineralsäuren wie Schwefel- oder p-Toluolsulfonsäure auch saure Ionentauscherharze oder Zeolithe eingesetzt. Letztere ermöglichen eine vereinfachte Aufarbeitung des Produkts sowie elegante Rückgewinnung des Katalysators. Methylacetat wird schließlich durch azeotrope Destillation aus dem Methanol/Methylacetat-Azeotrop gewonnen.[7]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Physikalische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Essigsäuremethylester ist eine farblose Flüssigkeit, die bei Normaldruck bei 57 °C siedet.[2] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in kPa, T in K) mit A = 7,06524, B = 57,630 und C = 219,726.[8][9] Die kritischen Größen betragen 506,8 K für die kritische Temperatur, 4688,8 kPa für den kritischen Druck und 228·10−6 m3·mol−1 für das kritische Volumen.[10][9] Die Verbindung ist in Wasser gut löslich mit 240 bis 250 g/l bei 20 °C.[2]
Sicherheitstechnische Kenngrößen[Bearbeiten | Quelltext bearbeiten]
Essigsäuremethylester bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von −13 °C.[2][11] Der Explosionsbereich liegt zwischen 3,1 Vol.‑% (95 g/m³) als untere Explosionsgrenze (UEG) und 16 Vol.‑% (495 g/m³) als obere Explosionsgrenze (OEG).[2][11] Experimentell wurde ein unterer Explosionspunkt von −19 °C bestimmt.[2][11] Die Sauerstoffgrenzkonzentration liegt bei 7,9 %.[12] Der maximale Explosionsdruck beträgt 9,6 bar.[2][11] Die Grenzspaltweite wurde mit 0,97 mm (50 °C) bestimmt.[2][11] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[2][11] Die Zündtemperatur beträgt 505 °C.[2][11] Der Stoff fällt somit in die Temperaturklasse T1. Unter erhöhtem Druck wird ein starkes Absinken der Zündtemperatur beobachtet.[11]
| Zündtemperaturen unter erhöhtem Druck[11] | ||||||||||||
| Druck | in bar | 3,29 | 7,4 | 10,6 | 12,46 | |||||||
| Zündtemperatur | in °C | 423 | 368 | 338 | 320 | |||||||
Verwendung[Bearbeiten | Quelltext bearbeiten]
Essigsäuremethylester wird vorwiegend als Lösungsmittel für Cellulosenitrat, Celluloseacetat und andere verwendet. Des Weiteren ist es beschränkt als Extraktionsmittel zugelassen. Außerdem wird Methylacetat auch in der weiterverarbeitenden Industrie aufgrund seiner Flüchtigkeit als Lösungsmittel für rasch trocknende Lacke eingesetzt. Ferner findet es Anwendung als Dunstmittel zur Aufweichung von Steifkappen und zur Herstellung von Klebstoffen, so UHU, auf der Basis von Polyvinylacetat; ferner bei Zelluloid-Klebstoffen aus Filmabfällen. Auch bei der Farbstoffherstellung und in der Parfümindustrie findet Methylacetat verschiedenste Anwendungsfelder.[13] In neueren Arbeiten wird auch der Einsatz in der Biodiesel-Produktion erforscht.[14]
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Methylacetat wird hauptsächlich über den Atemtrakt aufgenommen. Über diesen wird es vor allem in der Lunge und im Verdauungstrakt gut resorbiert. Dabei kommt es akut zu Reizwirkungen auf Augen und Atemwege. Des Weiteren wurde eine Störung des Zentralnervensystems festgestellt. Chronisch kann Methylacetat Hautschädigungen durch Kontakt mit der Flüssigkeit verursachen. Bei hohen Expositionen besteht die Gefahr einer Schädigung des Sehnervs. Eine Reproduktionstoxizität, Mutagenität oder Kanzerogenität konnte bisher noch nicht nachgewiesen werden bzw. es liegen keine ausreichenden Ergebnisse vor.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu METHYL ACETATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 24. Oktober 2021.
- ↑ a b c d e f g h i j k l m n o p q r s t u v Eintrag zu Methylacetat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-334.
- ↑ Eintrag zu Methyl acetate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 79-20-9 bzw. Methylacetat), abgerufen am 14. September 2019.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-24.
- ↑ a b c d Carole Le Berre, Philippe Serp, Philippe Kalck, G. Paull Torrence: Acetic Acid. In: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag GmbH & Co. KGaA., 26. März 2014, S. 25, doi:10.1002/14356007.a01_045.pub3 (Abschnitt „Methyl acetate“).
- ↑ Boublik, T.; Fried, V.; Hala, E.: The Vapor Pressures of Pure Substances Elsevier 1975.
- ↑ a b Kapoor, S.; Gill, B.K.; Rattan, V.K.: Isobaric Vapor-Liquid Equilibrium of Binary Mixture of Methyl Acetate with Isopropylbenzene at 97.3 kPa in Int. J. Chem. Mol. Eng.2 (2008) 281–284.
- ↑ Reid, R.C.; Prausnitz, J.M.; Poling, B.E.: The properties of Gases and Liquids, 4th ed. McGrawl-Hill, New York 1985.
- ↑ a b c d e f g h i Chemsafe Datenbank für sicherheitstechnische Kenngrößen im Explosionsschutz, PTB Braunschweig/BAM Berlin, abgerufen am 24. Februar 2021.
- ↑ Mitu, M.; Brandes, E.; Zakel, S.; Hirsch, W.: Explosion regions and limiting oxygen concentrations of methyl propionate, methyl acetate, dimethyl carbonate with air and inert gas mixtures in J. Loss Prev. Proc. Ind. 69 (2021) 104384, doi:10.1016/j.jlp.2020.104384.
- ↑ Eintrag zu Methylacetat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 17. Januar 2019.
- ↑ G. Doná, L. Cardozo-Filho, C. Silva, F. Castilhos: Biodiesel production using supercritical methyl acetate in a tubular packed bed reactor. In: Fuel Processing Technology. Band 106, 2013, S. 605–610, doi:10.1016/j.fuproc.2012.09.047.

