Parvoviridae
| Parvoviridae | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

Parvovirus B19, offiziell Primate erythroparvovirus 1 | ||||||||||||||
| Systematik | ||||||||||||||
| ||||||||||||||
| Taxonomische Merkmale | ||||||||||||||
| ||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||
| Parvoviridae | ||||||||||||||
| Links | ||||||||||||||
|
Die Familie Parvoviridae (Parvoviren) umfasst Spezies von Viren, die ein einzelsträngiges DNA-Genom tragen. Die Virionen (Viruspartikel) der Parvoviridae haben einen Durchmesser zwischen 18 und 26 nm; da sie damit zu den kleinsten Viren zählen, leitet sich ihr Name von lateinisch parvus ‚klein‘ ab. Parvoviren sind unbehüllt, wodurch sie sehr resistent gegen äußere Einflüsse sind.
Die Familie Parvoviridae wird nach der derzeitigen Master Species List #36 des International Committee on Taxonomy of Viruses (ICTV) in drei Unterfamilien aufgeteilt: Parvovirinae, Densovirinae und Hamaparvovirinae.[3]

Unterfamilie Parvovirinae
[Bearbeiten | Quelltext bearbeiten]Zu den Parvovirinae, welche ausschließlich Wirbeltiere infizieren, zählen die Genera Amdoparvovirus (alias Amdovirus), Artiparvovirus, Aveparvovirus, Bocaparvovirus (alias Bocavirus), Copiparvovirus, Dependoparvovirus (alias Dependovirus), Erythroparvovirus (alias Erythrovirus), Loriparvovirus sowie Tetraparvovirus und Protoparvovirus (letzteres ehemals tierpathogenes Parvovirus, beide zusammen früher Parvovirus). Die durch Parvovirinae ausgelösten Erkrankungen bezeichnet man als Parvovirosen.
Genus Amdoparvovirus
[Bearbeiten | Quelltext bearbeiten]Zu dieser Gattung gehören nach ICTV mit Stand 1. April 2024:[4][5]
- Spezies Amdoparvovirus carnivoran1 mit Aleutian mink disease parvovirus (ADV)
- Spezies Amdoparvovirus carnivoran2 mit Gray fox amdovirus (GFAV)
- Spezies Amdoparvovirus carnivoran3 mit Racoon dog and fox amdoparvovirus (RFAV)
- Spezies Amdoparvovirus carnivoran4 mit Skunk amdoparvovirus (SKAV)
- Spezies Amdoparvovirus carnivoran5 mit Red panda amdoparvovirus (RpAPV)
- Spezies Amdoparvovirus carnivoran6 mit Labrador amdoparvovirus 1 (LaAV-1)
- Spezies Amdoparvovirus carnivoran7 mit Red panda amdoparvovirus 2 (RpAPV-2)
Genus Artiparvovirus
[Bearbeiten | Quelltext bearbeiten]Mit Stand 1. April 2024 ist die Gattung monotypisch:[4][5]
- Spezies Artiparvovirus chiropteran1 mit Artibeus jamaicensis parvovirus (AjPV)
Genus Aveparvovirus
[Bearbeiten | Quelltext bearbeiten]Zu dieser Gattung gehören nach ICTV mit Stand 1. April 2024:[4][5]
- Spezies Aveparvovirus columbid1 mit Pigeon parvovirus 1 (PiPV1)
- Spezies Aveparvovirus galliform1 mit Turkey parvovirus (TuPV)
- Spezies Aveparvovirus gruiform1 mit Red-crowned crane parvovirus (RcPV)
- Spezies Aveparvovirus passeriform1 mit Pileated finch aveparvovirus (PfPV)
Genus Bocaparvovirus
[Bearbeiten | Quelltext bearbeiten]Zu dieser Gattung gehören nach ICTV mit Stand 1. April 2024[4][5] und Schirtzinger et al. (2015)[6]
- Spezies Bocaparvovirus carnivoran1 mit Canine minute virus; minute virus of canines CnMV; MVC
- Spezies Bocaparvovirus carnivoran2 mit Canine bocavirus 1 (CBoV1)
- Spezies Bocaparvovirus carnivoran3 mit Feline bocavirus (FBoV)
- Spezies Bocaparvovirus carnivoran4 mit Feline bocaparvovirus 2 (FBoV2)
- Spezies Bocaparvovirus carnivoran5 mit Feline bocaparvovirus 3 (FBoV3)
- Spezies Bocaparvovirus carnivoran6 mit Mink bocavirus 1 (MiBoV1)
- Spezies Bocaparvovirus carnivoran7 mit Canine bocavirus 3 (CnBoV3)
- Spezies Bocaparvovirus chiropteran1 mit Myotis myotis (bat) bocavirus 1 (BtBoV1)
- Spezies Bocaparvovirus chiropteran2 mit Bat bocavirus WM40 (BtBoVwm40)
- Spezies Bocaparvovirus chiropteran3 mit Bat bocavirus XM30 (BtBoVxm30)
- Spezies Bocaparvovirus chiropteran4 mit Miniopterus schreibersii bat bocavirus (BtBoV2)
- Spezies Bocaparvovirus chiropteran5 mit Rousettus leschenaultii bocaparvovirus 1 (RlBoV)
- Spezies Bocaparvovirus incertum1 mit Lupine bocavirus; rabbit bocavirus (LuBoV, RBoV)
- Spezies Bocaparvovirus lagomorph1 mit Rabbit bocaparvovirus (RBoV)
- Spezies Bocaparvovirus pinniped1 mit California sea lion bocavirus 1 (CslBoV1)
- Spezies Bocaparvovirus pinniped2 mit California sea lion bocavirus 3 (CslBoV3)
- Spezies Bocaparvovirus primate1 (Primaten-Bocaparvovirus 1) mit Human bocavirus 1 (Humanes Bocavirus 1, HBoV1) und HBoV3, Gorilla-Bocavirus
- Spezies Bocaparvovirus primate2 mit Human bocavirus 2c (Humanes Bocavirus 2c, HBoV2c) und HBoV2q, HBoV2b, HBoV4
- Spezies Bocaparvovirus primate3 mit Macaca mulatta bocaparvovirus (MmBoV)
- Spezies Bocaparvovirus rodent1 mit Rat bocavirus (RBoV)
- Spezies Bocaparvovirus rodent2 mit Murine bocavirus (MuBoV)
- Spezies Bocaparvovirus rodent3 mit Rodent bocavirus (RoBov)
- Spezies Bocaparvovirus ungulate1 (früher Ungulate bocaparvovirus 2) mit Bovine parvovirus 1 (BPV1)
- Spezies Bocaparvovirus ungulate2 mit Porcine bocavirus 1 (Porcines Bocavirus 1, PBoV1) und PBoV2, PBoV6
- Spezies Bocaparvovirus ungulate3 mit Porcine bocavirus SX (PBoVsx), Porcine bocavirus 5 (Porcines Bocavirus 5, PBoV5)
- Spezies Bocaparvovirus ungulate4 mit Porcine bocavirus H18 (PBoVh18), Porcine bocavirus 7 (Porcines Bocavirus 7, PBoV7)
- Spezies Bocaparvovirus ungulate5 mit Porcine bocavirus 3 (Porcines Bocavirus 3, PBoV3), PBoV4–1, PBoV4-2
- Spezies Bocaparvovirus ungulate6 mit Bovine bocaparvovirus 2; ungulate bocaparvovirus 6 (BBoV2; UBPV6)
- Spezies Bocaparvovirus ungulate7 mit Dromedary camel bocaparvovirus 1 (DBoV1)
- Spezies Bocaparvovirus ungulate8 mit Dromedary camel bocaparvovirus 2 (DBoV2)
- Spezies Bocaparvovirus ungulate9 mit Vicugna pacos bocaparvovirus (VpBoV)
- Spezies „Banna porcine bocavirus 1“
Genus Copiparvovirus
[Bearbeiten | Quelltext bearbeiten]Nach ICTV (Stand 1. April 2024)[4][5] und NCBI[7]
- Spezies Copiparvovirus pinniped1 (früher Pinniped copiparvovirus 1, ehem. Typusspezies) mit Sesavirus (SesaV) und mit Bovine parvovirus - 2 (BPV2)
- Spezies Copiparvovirus ungulate2 (früher Ungulate copiparvovirus 2) mit Porcine parvovirus 4 (PPV4) und PPV5
- Spezies Copiparvovirus ungulate3 (früher Ungulate copiparvovirus 3) mit Roe deer copiparvovirus (RdPV)
- Spezies Copiparvovirus ungulate4 (früher Ungulate copiparvovirus 4) mit Porcine parvovirus 6 (PPV6)
- Spezies Copiparvovirus ungulate5 (früher Ungulate copiparvovirus 5) mit Bosavirus (BosaV)
- Spezies Copiparvovirus ungulate6 (früher Ungulate copiparvovirus 6) mit Equine parvovirus-hepatitis (EqPV-H)
- Spezies Copiparvovirus ungulate7 (früher Ungulate copiparvovirus 7) mit Eqcopivirus (EqCoPV)
- Spezies Copiparvovirus ungulate8 (früher Ungulate copiparvovirus 8) mit Horse parvovirus CSF (EqPV-CSF)
Genus Dependoparvovirus
[Bearbeiten | Quelltext bearbeiten]Die Dependoviren (Genus Dependoparvovirus, früher Dependovirus, z. B. Adenoassozierte Viren) sind abhängig von Helferviren, um sich zu replizieren. Als Helferviren kommen Adenoviren, Herpesviren und Vacciniaviren in Fragen. Fehlen diese Helferviren, dann können die adenoassoziierten Viren in einen Latenzzustand übergehen, indem sie ihr eigenes Genom relativ ortsspezifisch in das zelluläre Genom einbauen und so lebenslang im Organismus verbleiben. Bei einer Koinfektion mit dem entsprechenden Helfervirus kann das integrierte virale Genom reaktiviert werden. Die adenoassoziierten Viren AAV-2, AAV-3 und AAV-5 können Menschen über Tröpfcheninfektion infizieren. Vermutlich sind über 90 % der Erwachsenen infiziert, allerdings sind keine Erkrankungsbilder bekannt.
Genus Erythroparvovirus
[Bearbeiten | Quelltext bearbeiten]
Die Erythroparvoviren (Genus Erythroparvovirus, früher Erythrovirus)[8] haben einen ausgeprägten Tropismus zu sich teilenden Vorläuferzellen von Erythrozyten, den Erythroblasten. Sie sind zur Replikation ihres Genoms auf die in der S-Phase vorliegenden zellulären Polymerasen angewiesen. Zu diesem Genus gehört unter anderem das Parvovirus B19, der Erreger der Ringelröteln.
Zur Gattung gehören mit Stand 1. April 2024:[4][5]
- Spezies Erythroparvovirus pinniped1 (früher Pinniped erythroparvovirus 1) mit Seal parvovirus (SePV)
- Spezies Erythroparvovirus primate1 (früher Primate erythroparvovirus 1) mit Human parvovirus B19 alias Erythrovirus B19 (B19V)
- Spezies Erythroparvovirus primate2 (früher Primate erythroparvovirus 2) mit Simian parvovirus (SPV)
- Spezies Erythroparvovirus primate3 (früher Primate erythroparvovirus 3) mit Rhesus macaque parvovirus (RmPV)
- Spezies Erythroparvovirus primate4 (früher Primate erythroparvovirus 4) mit Pig-tailed macaque parvovirus (PmPV)
- Spezies Erythroparvovirus rodent1 (früher Rodent erythroparvovirus 1) mit Chipmunk parvovirus (ChpPV)
- Spezies Erythroparvovirus ungulate1 (früher Ungulate erythroparvovirus 1) mit Bovine parvovirus 3 (BPV3)
Genus Loriparvovirus
[Bearbeiten | Quelltext bearbeiten]Mit Stand 1. April 2024 ist die Gattung monotypisch:[4][5]
- Spezies Loriparvovirus primate1 mit Slow loris parvovirus (SLPV)
Genus Protoparvovirus
[Bearbeiten | Quelltext bearbeiten]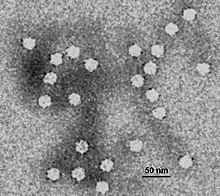
Die Viren dieses Genus[9] replizieren sich autonom. Zu ihnen zählen fast ausschließlich tierpathogene (nur bei Tieren krankheitsauslösende) Erreger und können bei Haus- und Nutztieren schwere Erkrankungen verursachen. Diese Viren sind sehr nah miteinander verwandt mit einer sich über das gesamte Genom erstreckenden Homologie bei einer Sequenzidentität von mehr als 98 %. Erin Elizabeth Schirtzinger et al. führen folgende Spezies auf:[6]


Die Gattung umfasst (Stand 1. April 2024):
- Spezies Protoparvovirus carnivoran1 (früher Carnivore protoparvovirus 1) mit Canines Parvovirus (en. Canine parvovirus, CPV)
- Spezies Protoparvovirus carnivoran2 (früher Carnivore protoparvovirus 2) mit Sea otter parvovirus (SoPV)
- Spezies Protoparvovirus carnivoran3 (früher Carnivore protoparvovirus 3) mit Canine bufavirus (CBuV)
- Spezies Protoparvovirus carnivoran4 (früher Carnivore protoparvovirus 4) mit Fox parvovirus (FoPV)
- Spezies Protoparvovirus carnivoran5 (früher Carnivore protoparvovirus 5) mit Newlavirus (NLPV)
- Spezies Protoparvovirus chiropteran1 (früher Chiropteran protoparvovirus 1) mit Megabat bufavirus 1 (BtBuV1)
- Spezies Protoparvovirus eulipotyphla1 (früher Eulipotyphla protoparvovirus 1) mit Mpulungu (shrew) bufavirus (MpBuV)
- Spezies Protoparvovirus incertum1 (früher Primate protoparvovirus 4) mit Tusavirus (TuV)
- Spezies Protoparvovirus pinniped1 mit California sea lion parvovirus Hanchett CslPV
- Spezies Protoparvovirus primate1 (früher Primate protoparvovirus 1) mit Bufavirus 2a (BuV1a) - human
- Spezies Protoparvovirus primate2 (früher Primate protoparvovirus 2) mit Wuharv (rhesus) parvovirus 1 (WuBuV1)
- Spezies Protoparvovirus primate3 (früher Primate protoparvovirus 3) mit Cutavirus (CutaV) - human
- Spezies Protoparvovirus rodent1 (früher Rodent protoparvovirus 1) mit Minute virus of mice (MVM), Parvovirus H-1 und Kilham-Ratten-Virus[10][11]
- Spezies Protoparvovirus rodent2 (früher Rodent protoparvovirus 2) mit Rat parvovirus 1 (RPV1)
- Spezies Protoparvovirus rodent3 (früher Rodent protoparvovirus 3) mit Rat bufavirus SY-2015 (RatBuV)
- Spezies Protoparvovirus ungulate1 (früher Ungulate protoparvovirus 1) mit Porcine parvovirus PPV
- Spezies Protoparvovirus ungulate2 (früher Ungulate protoparvovirus 2) mit Porcine bufavirus (PBuV, Porcines Parvovirus, PPV)
- Spezies Protoparvovirus ungulate3 (früher Ungulate protoparvovirus 3) mit Equine protoparvovirus EqPV
- Spezies „Feline parvovirus“ (Felines Parvovirus)
Das Canine Parvovirus ist 1978 vermutlich direkt aus dem Felinen Parvovirus (Erreger der Katzenseuche) entstanden und plötzlich aufgetreten. Dabei verbreitete es sich weltweit sehr schnell, worauf in dieser Pandemie Millionen von Hunden starben. Mittlerweile sind die Parvovirosen bei Hund und Katze mit Hilfe von Lebendimpfstoffen gut beherrschbar. Das Parvovirus H-1 befällt normalerweise Nagetiere, kann aber auch menschliche Zellen infizieren, verursacht jedoch beim Menschen dabei keinerlei Krankheitssymptome.
Genus Sandeparvovirus
[Bearbeiten | Quelltext bearbeiten]Mit Stand 1. April 2024 ist die Gattung monotypisch:[4][5]
- Spezies Sandeparvovirus perciform1 mit Zander parvovirus (ZPV)
Genus Tetraparvovirus
[Bearbeiten | Quelltext bearbeiten]Zu dieser Gattung gehören nach ICTV mit Stand 1. April 2024[4][5] und Schirtzinger et al. (2015)[6]
- Spezies Tetraparvovirus chiropteran1 (früher Chiropteran tetraparvovirus 1) mit Eidolon helvum (bat) parvovirus 1 (BtPARV4)
- Spezies Tetraparvovirus didelphimorph1 mit opossum tetraparvovirus OpPARV4
- Spezies Tetraparvovirus primate1 (früher Primate tetraparvovirus 1) mit Human parvovirus 4 (PARV4)
- Spezies Tetraparvovirus rodent1 mit Rodent tetraparvovirus RoPARV4
- Spezies Tetraparvovirus ungulate1 (früher Ungulate tetraparvovirus 1) mit Bovine hokovirus 1 (BPARV4)
- Spezies Tetraparvovirus ungulate2 (früher Ungulate tetraparvovirus 2) mit Porcine hokovirus; Porcine parvovirus 3 (PPARV4, PPV3)
- Spezies Tetraparvovirus ungulate3 (früher Ungulate tetraparvovirus 3) mit Porcine parvovirus 2; Porcines Hokovirus; Porcines Partetravirus; Parvovirus YX-2010/CHN PPV2 (PARV4, CnPPARV4), Cnvirus[12]
- Spezies Tetraparvovirus ungulate4 (früher Ungulate tetraparvovirus 4) mit Ovine hokovirus 1 (OvPARV4)
Die Bezeichnung „Hokovirus“ für Viren der Gattung Tetraparvovirus ist veraltet und sollte entsprechend ersetzt werden, denn „Hokovirus“ steht auch für eine vorgeschlagene Riesenviren-Gattung der Klosneuvirinae (Familie Mimiviridae); Fundort Klosterneuburg bei Wien.
Unterfamilie Densovirinae
[Bearbeiten | Quelltext bearbeiten]Die historisch zweite Unterfamilie der Densovirinae umfasst die die Parvoviren der Insekten und anderer Arthropoden. Die frühere Gattung Ambidensovirus (hervorgegangen aus Densovirus mit Pefudensovirus) wurde neu aufgeteilt und Pefudensovirus als Pefuambidensovirus wiederhergestellt. Mitglieder (Stand 1. April 2024):[4][5][13]
- Gattung Aquambidensovirus (abgetrennt von Ambidensovirus)
- Spezies Aquambidensovirus asteroid1 (veraltet Asteroid ambidensovirus 1) mit Sea star-associated densovirus (SSaDV)[14][15]
- Spezies Aquambidensovirus asteroid2 mit Asterias forbesi-associated densovirus (AfaDV)
- Spezies Aquambidensovirus decapod1 (veraltet Decapod ambidensovirus 1) mit Cherax quadricarinatus densovirus (CqDV)
- Spezies Aquambidensovirus ostreid1 mit Crassostrea ariakensis ambidensovirus 1 (CaaDV)
- Gattung Blattambidensovirus (abgetrennt von Ambidensovirus)
- Spezies Blattambidensovirus blattodean1 (veraltet Blattodean ambidensovirus 2) mit Blattella germanica densovirus 1 (BgDV1)
- Spezies Blattambidensovirus incertum1 mit Parus major densovirus (PamDV)
- Spezies Blattambidensovirus incertum2 mit SAfia-838D_Ambidensovirus (SA838DDV)
- Spezies Blattambidensovirus incertum3 mit Ambidensovirus_Croatia_17_S17 (17_S17)
- Spezies Blattambidensovirus incertum4 mit Bat-associated densovirus 3 (BaDV3)
- Gattung Diciambidensovirus (abgetrennt von Ambidensovirus)
- Spezies Diciambidensovirus hemipteran1 mit Diaphorina citri densovirus (DcDV)
- Spezies Diciambidensovirus hemipteran2 mit Bactericera_trigonica_densovirus (BtDV)
- Spezies Diciambidensovirus incertum1 mit SAfia-400D ambidensovirus (SA400DDV)
- Gattung Hemiambidensovirus
- Spezies Hemiambidensovirus hemipteran1 (veraltet Hemipteran ambidensovirus 2) mit Dysaphis plantaginea densovirus 1 (DplDV1)
- Spezies Hemiambidensovirus hemipteran2 (veraltet Hemipteran ambidensovirus 3) mit Myzus persicae densovirus 1 (MpDV1)
- Gattung Iteradensovirus (früher Iteravirus)
- Spezies Iteradensovirus incertum1 mit Bat-associated densovirus 5 (BaDV5)
- Spezies Iteradensovirus incertum2 mit Human CSF-associated densovirus (HCSFaDV)
- Spezies Iteradensovirus lepidopteran1 (veraltet Lepidopteran iteradensovirus 1, ehem. Typusspezies) mit Bombyx mori densovirus 1 (BmDV1)
- Spezies Iteradensovirus lepidopteran2 mit Casphalia extranea densovirus (CeDV)
- Spezies Iteradensovirus lepidopteran3 mit Dendrolimus punctatus densovirus (DpDV)
- Spezies Iteradensovirus lepidopteran4 mit Papilio polyxenes densovirus (PpDV)
- Spezies Iteradensovirus lepidopteran5 mit Helicoverpa armigera densovirus (HaDV)
- Gattung Miniambidensovirus
- Spezies Orthopteran miniambidensovirus 1 mit Acheta domestica mini ambidensovirus (AdMDV)
- Gattung Muscodensovirus
- Spezies Muscodensovirus dipteran1 mit Haematobia irritans densovirus (HiDV)
- Spezies Muscodensovirus dipteran2 mit Broome densovirus (BrDV)
- Gattung Pefuambidensovirus (abgetrennt von Ambidensovirus, veraltet Pefudensovirus)
- Spezies Pefuambidensovirus blattodean1 (veraltet Blattodean ambidensovirus 1) mit Periplaneta fuliginosa densovirus (PfDV, PfDNV)
- Spezies Pefuambidensovirus unionid1 mit Clinch densovirus 1 (CDV1)
- Gattung Protoambidensovirus (Restbestand von Ambidensovirus, ehemals Densovirus)[16]
- Spezies Protoambidensovirus dipteran1 (veraltet Dipteran ambidensovirus 1) mit Culex pipiens densovirus (CpDV)
- Spezies Protoambidensovirus incertum1 mit Duck-associated ambidensovirus 1 (DaaDV1)
- Spezies Protoambidensovirus lepidopteran1 (veraltet Lepidopteran ambidensovirus 1, ehem. Typusspezies) mit Galleria mellonella densovirus (GmDV)
- Gattung Scindoambidensovirus
- Spezies Scindoambidensovirus hemipteran1 (veraltet Hemipteran ambidensovirus 1) mit Planococcus citri densovirus (PcDV)
- Spezies Scindoambidensovirus hymenopteran1 (veraltet Hymenopteran ambidensovirus 1) mit Solenopsis invicta densovirus (SiDV)
- Spezies Scindoambidensovirus incertum1 mit Bat-associated densovirus 1 (BaDV1)
- Spezies Scindoambidensovirus incertum2 mit Bat-associated densovirus 2 (BaDV2)
- Spezies Scindoambidensovirus orthopteran1 (veraltet Orthopteran ambidensovirus 1) mit Acheta domestica densovirus (AdDV)
- Gattung Tetuambidensovirus
- Spezies Tetuambidensovirus incertum1 mit Bat-associated densovirus 4 (BaDV4)
- Spezies Tetuambidensovirus incertum2 mit Lupine feces-associated densovirus 2 (LfaDV2)
- Spezies Tetuambidensovirus trombidiform1 mit Tetranychus urticae-associated ambidensovirus (TuDV)
Unterfamilie Hamaparvovirinae
[Bearbeiten | Quelltext bearbeiten]Diese Unterfamilie kam 2021 mit der Master Species List #36 des ICTV hinzu.[3] Sie wurde abgetrennt von Densovirinae; die Mitglieder sind (Stand 1. April 2024):[4][5]
- Gattung Brevihamaparvovirus (früher Brevidensovirus)
- Spezies Brevihamaparvovirus dipteran1 mit Anopheles gambiae densovirus (AgDV)
- Spezies Brevihamaparvovirus dipteran2 (veraltet Dipteran brevidensovirus 2, ehem. Typusspezies) mit Aedes albopictus densovirus 2 (AalDV2)
- Gattung Chaphamaparvovirus (früher Chapparvovirus: aufgeteilt)
- Spezies Chaphamaparvovirus avian1 mit Avian chapparvovirus BR_DF10 (AvChPV-BR_DF10)
- Spezies Chaphamaparvovirus carnivoran1 mit Cachavirus 1A (CaChV 1A)
- Spezies Chaphamaparvovirus carnivoran2 mit Fechavirus (FChPV)
- Spezies Chaphamaparvovirus carnivoran3 mit Ursus americanus parvovirus (UaPV)
- Spezies Chaphamaparvovirus chiropteran1 mit Desmodus rotondus chapparvovirus (DrChPV)
- Spezies Chaphamaparvovirus dasyurid1 mit Tasmanian devil-associated chapparvovirus 1 (TdChPV1)
- Spezies Chaphamaparvovirus dasyurid2 mit Tasmanian devil-associated chapparvovirus 2 (TdChPV2)
- Spezies Chaphamaparvovirus dasyurid3 mit Tasmanian devil-associated chapparvovirus 6 (TdChPV6)
- Spezies Chaphamaparvovirus galliform1 mit Turkey parvovirus 2 (TPV2)
- Spezies Chaphamaparvovirus galliform2 mit Chicken chapparvovirus 2 (ChChPV2)
- Spezies Chaphamaparvovirus galliform3 mit Chicken chapparvovirus HK (ChChPV-HK)
- Spezies Chaphamaparvovirus primate1 mit Capuchin kidney parvovirus (CKPV)
- Spezies Chaphamaparvovirus primate2 mit Macaca fascicularis chapparvovirus (MfChPV)
- Spezies Chaphamaparvovirus psittacine1 mit Psittacara leucophthalmus chapparvovirus (PlChPV)
- …
- Gattung Hepanhamaparvovirus (früher Hepandensovirus)
- Spezies Hepanhamaparvovirus decapod1 (veraltet Decapod hepandensovirus 1, ehem. Typusspezies) mit Fenneropenaeus chinensis hepatopancreatic densovirus (FcHDV)
- Gattung Ichtchaphamaparvovirus (früher Chapparvovirus: aufgeteilt)
- Spezies Ichtchaphamaparvovirus syngnathid1 mit Syngnathus scovelli chapparvovirus (ScChPV)
- Gattung Penstylhamaparvovirus (früher Penstyldensovirus)
- Spezies Penstylhamaparvovirus decapod1 (veraltet Decapod penstyldensovirus 1, ehem. Typusspezies) mit Penaeus stylirostris penstyldensovirus 1 (PstDV1)
Ohne Unterfamilie
[Bearbeiten | Quelltext bearbeiten]Mit Stand 1. April 2024:[4][5]
- Gattung Metalloincertoparvovirus
- Spezies Metalloincertoparvovirus decapod1 mit Penaeus monodon metallodensovirus (PmMDV)
Weblinks
[Bearbeiten | Quelltext bearbeiten]- VU Wien: Allgemeine Virologie
- SIB: Parvoviridae, auf: Expasy ViralZone
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e ICTV: ICTV Taxonomy history: Primate erythroparvovirus 1, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- ↑ a b ICTV: ICTV Master Species List 2020.v1, New MSL including all taxa updates since the 2019 release, March 2021 (MSL #36)
- ↑ a b c d e f g h i j k l ICTV: Taxonomy Browser.
- ↑ a b c d e f g h i j k l ICTV: Virus Metadata Resource (VMR).
- ↑ a b c Erin Elizabeth Schirtzinger, Andrew Suddith, Benjamin M. Hause, Richard A. Hesse: First identification of porcine parvovirus 6 in North America by viral metagenomic sequencing of serum from pigs infected with porcine reproductive and respiratory syndrome virus. In: Virology Journal, Oktober 2015, (12), S. 170, doi:10.1186/s12985-015-0401-6
- ↑ NCBI: ncbi.nlm.nih.gov (Genus)
- ↑ SIB: Erythroparvovirus, auf: ViralZone
- ↑ SIB: Protoparvovirus, auf: ViralZone
- ↑ NCBI: Kilham rat virus (no rank)
- ↑ Werner Nicklas: Kilham Rat Virus (KRV) ( des vom 10. Juni 2020 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis., auf: gv-solas, DKFZ Heidelberg
- ↑ Attila Cságola, Zoltán Zádori, István Mészáros, Tamás Tuboly: Detection of Porcine Parvovirus 2 (Ungulate Tetraparvovirus 3) Specific Antibodies and Examination of the Serological Profile of an Infected Swine Herd. In: PLOS ONE, Band 11, Nr. 3, 2016, S. e0151036; doi:10.1371/journal.pone.0151036, PMID 26974825, PMC 4790921 (freier Volltext), ResearchGate:298331331, Epub 14. März 2016 (englisch). Siehe insbes. Fig1.
- ↑ S. F. Cotmore, M. Agbandje-McKenna, J. A. Chiorini, D. V. Mukha, D. J. Pintel, J. Qiu, M. Soderlund-Venermo, P. Tattersall, P. Tijssen, D. Gatherer, A. J. Davison: The family Parvoviridae. In: Archives of virology. Band 159, Nummer 5, Mai 2014, S. 1239–1247, doi:10.1007/s00705-013-1914-1, PMID 24212889, PMC 4013247 (freier Volltext).
- ↑ NCBI: Sea star-associated densovirus (no rank)
- ↑ Ian Hewson et al.; James L. Van Etten (Hrsg.): Densovirus associated with sea-star wasting disease and mass mortality, in: PNAS, 17. November 2014, doi:10.1073/pnas.1416625111. Dazu:
- Ashley Yeager: Virus blamed in starfish die-off, auf: ScienceNewsForStudents vom 19. Dezember 2014
- ↑ SIB: Protambidensovirus, auf: ViralZone