Epstein-Barr-Virus
| Epstein-Barr-Virus | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

Virionen des EBV (TEM-Abbildung, Deformationen präparationsbedingt) | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
| ||||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||||
| ||||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||||
| Human gammaherpesvirus 4 | ||||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||||
| HHV4 | ||||||||||||||||||||
| Links | ||||||||||||||||||||
|
Das Epstein-Barr-Virus (EBV, auch Humanes Herpesvirus 4, HHV4, engl. Human gammaherpesvirus 4) ist eine Spezies humanpathogener, behüllter, doppelsträngiger DNA-Viren aus der Familie der Orthoherpesviridae. Erstmals beschrieben wurde das Epstein-Barr-Virus 1964 von Anthony Epstein, Yvonne Barr und Bert Achong. Sie entdeckten EBV in B-Lymphozyten, die von einem afrikanischen Patienten mit Burkitt-Lymphom stammten. Das Epstein-Barr-Virus ist damit das erste entdeckte Onkovirus des Menschen.
Übertragung[Bearbeiten | Quelltext bearbeiten]
Hauptübertragungsweg des Virus ist eine Tröpfcheninfektion oder eine Kontaktinfektion (besonders Speichel) bzw. Schmierinfektion, seltener sind Übertragungen im Rahmen von Transplantationen oder Bluttransfusionen. Die Tatsache, dass EBV auch in Sekreten der Genitalien festgestellt werden konnte, macht auch den Übertragungsweg durch sexuelle Kontakte denkbar.[2]
Auf molekularer Ebene werden complement receptor type 1 (CR1) und complement receptor type 2 (CR2) als Adhäsionsfaktoren an der Zelloberfläche beschrieben.[3][4] Für den Eintritt in Zellen benutzt das EBV Integrine[5] oder HLA-II (HLA class II histocompatibility antigen).[6]
Infektionsfolgen[Bearbeiten | Quelltext bearbeiten]
Die Infektion mit dem Virus erfolgt zumeist im Kindesalter. Während in diesem Falle in der Regel keine Symptome auftreten, kommt es bei jugendlichen oder erwachsenen Infizierten in 30–60 % aller Fälle zum Ausbruch des Pfeiffer-Drüsenfiebers (infektiöse Mononukleose).
Ab dem 40. Lebensjahr sind ca. 98 % der Menschen mit EBV infiziert. Sowohl nach einer asymptomatischen als auch nach einer symptomatischen Infektion persistiert das Virus lebenslang im Körper. Es kann wie alle Herpesviren reaktiviert werden.
Für gewöhnlich wird eine Reaktivierung vom Wirt nicht bemerkt und schnell durch sein Immunsystem eingedämmt. Besteht eine Immunsuppression (z. B. bei HIV-Infizierten oder Organempfängern), kann sich das Virus unkontrolliert vermehren und zur Entstehung verschiedener seltener Krebserkrankungen beitragen. So besteht seit rund 40 Jahren der Verdacht, dass EBV eine wichtige ätiologische Rolle bei Krankheiten wie Morbus Hodgkin (Lymphdrüsenkrebs), Burkitt-Lymphom sowie weiteren Lymphomen und bei der posttransplantativen lymphoproliferativen Erkrankung spielt.[7][8][9][10]
EBV gehört somit zusammen mit dem Hepatitis-B-Virus (HBV), dem Hepatitis-C-Virus (HCV), den humanen Papillomviren (HPV), dem humanen T-lymphotropen Virus 1 (HTLV-1) und dem humanen Herpesvirus 8 (HHV-8, auch Kaposi-Sarkom-Herpesvirus, KSHV) zu einer Gruppe humaner Viren, die weltweit für 10 bis 15 Prozent aller Krebserkrankungen verantwortlich sind.[11]
Darüber hinaus erhärtete sich der Verdacht, dass EBV mit einer Vielzahl von Autoimmunerkrankungen, wie z. B. Multipler Sklerose (MS), systemischem Lupus erythematodes und der rheumatoiden Arthritis in Zusammenhang steht.[12][13][14][15] Eine 2022 veröffentlichte Studie zeigte bei 955 MS-Diagnosen unter mehr als 10 Millionen jungen Erwachsenen im aktiven Dienst des US-Militärs bei schließlich 35 den Endergebnissen zugrunde liegenden Personen einen um das 32-fache (95-%-Konfidenzintervall zwischen 4,3- und 245,3-fache) erhöhten Anteil einer Infektion mit EBV. Dieser war bei anderen Viren, einschließlich des ähnlich übertragenen Cytomegalovirus nicht zu beobachten.[16][17] Bei einer 2020 erschienenen Studie zu deutschen MS-Patienten im Alter von 27 bis 41 Jahren konnte bei 100 % (d. h. allen 901 Fällen) eine durchlaufene EBV-Infektion nachgewiesen werden, Vergleichswerte in der breiten Bevölkerung lagen bei 92–98 %.[18]
Auch die Myalgische Enzephalomyelitis / das Chronische Fatigue-Syndrom (ME/CFS)[19] sowie die Encephalitis lethargica[20] werden mit dem Virus in Verbindung gebracht. In Afrika existiert auch eine lokal immer wieder zu Epidemien führende (endemische) Variante des EBV-assoziierten Burkitt-Lymphoms.
Eine EBV-Infektion gilt als ein möglicher Risikofaktor für Tumoren der Nase oder des Kehlkopfes (Nasopharynxkarzinom). EBV ist jedoch für die Krebsentstehung alleine nicht ausreichend, wie die geringe Anzahl der Krebserkrankungen im Vergleich zur Virusverbreitung zeigt. Weitere Faktoren spielen hier eine Rolle (chromosomale Translokation des c-myc-Genes). Als potentielle Begleiteinflussgröße (Kofaktor) wird auch Malaria diskutiert. Auch menschliche Brustkrebszellen sind häufig durch Epstein-Barr-Viren infiziert, ohne dass ein ursächlicher Zusammenhang gesehen wird.
Obwohl EBV nicht als Brustkrebsvirus aufzufassen ist, verändert es das Ansprechen der Brustkrebszellen auf die Taxane, die bei der Chemotherapie eingesetzt werden. Noch häufiger als Brustkrebszellen sind Fibroadenome der Brust durch Epstein-Barr-Viren infiziert.
Auch psychiatrische Erkrankungen stehen im Verdacht, durch Epstein-Barr-Viren mitverursacht zu sein. So wurde in einer 2019 veröffentlichten Studie bei Schizophrenie-Erkrankten ein Zusammenhang zwischen genetischer Prädisposition und Virusexposition aufgedeckt.[21]
Bakterielle Begleitinfektionen sind möglich.
Diagnostik[Bearbeiten | Quelltext bearbeiten]
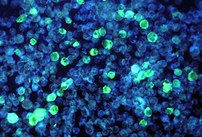
Allgemein findet man bei der Infektion mit dem Epstein-Barr-Virus fast immer einen erhöhten Anteil von Lymphozyten an den gesamten weißen Blutkörperchen (so genannte relative Lymphozytose). Die Gesamtzahl der weißen Blutkörperchen kann dabei verringert, normal oder erhöht sein. Wird ein Blutausstrich unter dem Mikroskop untersucht, sieht man atypische mononukleäre Zellen mit charakteristischen Veränderungen (so genannte Pfeiffer-Zellen – morphologisch gegen EBV gerichtete spezifische zytotoxische (CD8+) T-Lymphozyten, die einen runden oder gebuchteten Zellkern (selten gelappt) aufweisen), die manchmal bereits die Diagnose ermöglichen. Weiterhin sind die Leberwerte häufig erhöht.
Die serologische Beurteilung des EBV-Status ist nicht immer einfach. Zum Nachweis der akuten Infektion werden mancherorts sogenannte Schnelltests angewendet, die jedoch je nach Lebensalter bis zu 20 % falsch positive und 30 % falsch negative Resultate liefern. Die Diagnostik (normaler immunkompetenter Patienten) sollte gestaffelt erfolgen, und die Konstellationen, die mancher Patient oder Arzt auf seinem Laborbericht findet, sind manchmal etwas schwierig zu deuten:
- Der Nachweis von IgG-Antikörpern gegen das nukleäre Antigen von EBV (EBNA-1-IgG) beweist das Vorhandensein des Virus. Ist der EBNA-1-IgG-Test eindeutig positiv, so ist jeder weitere Test zum Virusnachweis bei einer akuten Erkrankung (Mononukleose) unnötig, denn eine Mononukleose nach frischer Infektion ist bei positivem EBNA-IgG-Nachweis ausgeschlossen, da diese Antikörper erst im Laufe mehrerer Wochen bis Monaten nach Auftreten der Symptome und beim Übergang in die Viruslatenz vom Immunsystem produziert werden. Bei etwa 95 % der Menschen mit zurückliegender EBV-Infektion sind EBNA-1-IgG-Antikörper nachweisbar.
- Ist das EBNA-1-IgG negativ, sollte das IgG gegen das virale Capsid-Antigen (VCA-IgG) getestet werden. Es ist ein Marker für aktuellen oder früheren Kontakt mit EBV und bleibt in der Regel lebenslang nachweisbar.
- Zum Nachweis einer akuten Infektion werden bei positivem VCA-IgG die IgM-Antikörper gegen das virale Capsid (VCA-IgM) getestet. Sind diese positiv, so spricht dies für eine frische bzw. kürzliche Infektion (beweist diese allerdings nicht!).
- Bei starker körperlicher Belastung (besonders bei Leistungssportlern) kann das VCA-IgM persistieren. Man spricht von einer verlängerten (prolongierten) Ausheilung, wenn das EBNA-1-IgG bereits positiv ist.
- In diagnostischen Problemfällen kann häufig durch einen Immunoblot und/oder eine Aviditätstestung eine akute von einer zurückliegenden Infektion unterschieden werden. Der Nachweis einer hohen Avidität der VCA-IgG-Antikörper beweist einen länger zurückliegenden Infektionszeitpunkt, eine deutliche VCA-p18-Bande im IgG-Immunoblot spricht ebenfalls dafür. Typische Befunde bei einer akuten Infektion sind: Fehlen von EBNA-1-IgG-Antikörpern, niedrige Avidität der VCA-IgG-Antikörper und Nachweis von IgG- und/oder IgM-Antikörper gegen EA (early antigen).
- Bei Immunschwäche (Immuninkompetenz) kann das Virus von der Ruhephase (Latenz) wieder in eine aktive Vermehrung übergehen (Reaktivierung). Hierbei kann das EBNA-1-IgG beispielsweise bei HIV-Patienten sekundär wieder negativ werden. Eine zuverlässige Einschätzung von EBV-Reaktivierungen bei Immunschwäche ist nur anhand der Bestimmung der Viruslast durch Polymerase-Kettenreaktion möglich.
- Der direkte Nachweis der Virus-DNA mittels Polymerase-Kettenreaktion ist bei Immungesunden meist nicht sinnvoll, da im Blut auch das latente Genom nachgewiesen werden kann und gleichzeitig symptomlose Träger das Virus konstant oder vorübergehend mit dem Speichel ausscheiden. Die oben genannten Reaktivierungen bereiten einem immungesunden Menschen in aller Regel keine Beschwerden, sie stellen lediglich ein labordiagnostisches Problem dar, da der Nachweis von VCA-IgG in hohen Konzentrationen und ggf. wieder auftretendes VCA-IgM zu Fehlinterpretationen führen kann.
Eine Besonderheit des EBV ist es, dass durch die akute Infektion von B-Lymphozyten (v. a. B-Gedächtniszellen) mit EBV diese wieder IgM-Antikörper schon lange ausgeheilter Infektionen oder von Impfungen bilden können. Diese Patienten zeigen dann oft das gleichzeitige Vorhandensein von IgM gegen Röteln, Masern, Hepatitis A, CMV u. v. m. und imitieren somit serologisch eine akute Infektion mit diesen Erregern. Ein Patient mit mehr als einem positiven IgM ist daher stets EBV-verdächtig.
Prävention[Bearbeiten | Quelltext bearbeiten]
Es gibt noch keine zugelassenen Epstein-Barr-Virus-Impfstoffe, jedoch befinden sich verschiedene Kandidaten in Entwicklung.
Literatur[Bearbeiten | Quelltext bearbeiten]
- M. A. Epstein, B. G. Achong, Y. M. Barr: Virus particles in cultured lymphoblasts from Burkitt’s lymphoma. In: The Lancet. 1964, Band 283, Nr. 7335, S. 702–3.
- M. A. Epstein, G. Henle et al.: Morphological and biological studies on a virus in cultured lymphoblasts from Burkitt’s lymphoma. In: Journal of Experimental Medicine. Band 121, 1965, S. 761–70.
- D. H. Crawford: Biology and disease associations of Epstein-Barr virus. In: Philosophical Transactions of the Royal Society B: Biological Sciences. Band 356, 2001, S. 461–473.
- W. Amon, PJ. Farrell: Reactivation of Epstein-Barr virus from latency. In: Reviews in Medical Virology. Mai–Juni 2005, Band 15, Nr. 3, S. 149–56, PMID 15546128.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e ICTV: ICTV Taxonomy history: Human gammaherpesvirus 4. EC 51, Berlin, Germany, Juli 2019; Email Beglaubigung: März 2020 (MSL #35).
- ↑ Epstein-Barr-Virus | Expertensprechstunde. Abgerufen am 20. Dezember 2022.
- ↑ Javier G. Ogembo, Lakshmi Kannan, Ionita Ghiran, Anne Nicholson-Weller, Robert W. Finberg: Human Complement Receptor Type 1/CD35 Is an Epstein-Barr Virus Receptor. In: Cell Reports. Band 3, Nr. 2, Februar 2013, S. 371–385, doi:10.1016/j.celrep.2013.01.023 (elsevier.com [abgerufen am 30. April 2020]).
- ↑ J. Tanner, Y. Whang, J. Sample, A. Sears, E. Kieff: Soluble gp350/220 and deletion mutant glycoproteins block Epstein-Barr virus adsorption to lymphocytes. In: Journal of Virology. Band 62, Nr. 12, 1. Dezember 1988, ISSN 0022-538X, S. 4452–4464, PMID 2460635 (asm.org [abgerufen am 30. April 2020]).
- ↑ L. S. Chesnokova, S. L. Nishimura, L. M. Hutt-Fletcher: Fusion of epithelial cells by Epstein-Barr virus proteins is triggered by binding of viral glycoproteins gHgL to integrins v 6 or v 8. In: Proceedings of the National Academy of Sciences. Band 106, Nr. 48, 1. Dezember 2009, ISSN 0027-8424, S. 20464–20469, doi:10.1073/pnas.0907508106 (pnas.org [abgerufen am 30. April 2020]).
- ↑ Q. Li, M. K. Spriggs, S. Kovats, S. M. Turk, M. R. Comeau: Epstein-Barr virus uses HLA class II as a cofactor for infection of B lymphocytes. In: Journal of Virology. Band 71, Nr. 6, Juni 1997, ISSN 0022-538X, S. 4657–4662, PMID 9151859 (nih.gov [abgerufen am 30. April 2020]).
- ↑ E. Maeda et al.: Spectrum of Epstein-Barr virus-related diseases: a pictorial review. In: Japanese Journal of Radiology. Band 27. Jahrgang, Nr. 1, 2009, S. 4–19, PMID 19373526.
- ↑ M. K. Ghandi: Epstein-Barr virus-associated lymphomas. In: Expert Review of Anti-Infective Therapy. Band 4. Jahrgang, Nr. 1, 2006, S. 77–89, PMID 16441211.
- ↑ S. A. Rezk, L. M. Weiss: Epstein-Barr virus-associated lymphoproliferative disorders. In: Human Pathology. Band 38. Jahrgang, Nr. 9, 2009, S. 1293–1304, PMID 17707260.
- ↑ M. Roweet al.: Burkitt's lymphoma: the Rosetta Stone deciphering Epstein-Barr virus biology. In: Seminars in Cancer Biology. Band 19. Jahrgang, Nr. 6, 2009, S. 377–388, PMID 19619657.
- ↑ D. Martin, J. S. Gutkind: Human tumor-associated viruses and new insights into the molecular mechanisms of cancer. In: Oncogene. Band 27. Jahrgang, Nr. 2, 2008, S. 31–42, PMID 19956178.
- ↑ E. Toussirot, J. Roudier: Epstein-Barr virus in autoimmune diseases. In: Best Practice & Research Clinical Rheumatology. Band 22. Jahrgang, Nr. 5, 2008, S. 883–896, PMID 19028369.
- ↑ B. A. Bagert: Epstein-Barr virus in multiple sclerosis. In: Current Neurology and Neuroscience Reports. Band 9. Jahrgang, Nr. 5, 2009, S. 405–410, PMID 19664371.
- ↑ D. Pohl: Epstein-Barr virus and multiple sclerosis. In: Journal of the Neurological Sciences. Band 286. Jahrgang, Nr. 1–2, 2009, S. 62–64, PMID 19361810.
- ↑ Epstein-Barr Virus und multiple Sklerose: Zusammenhang erhärtet. In: idw-online.de. 14. September 2009, abgerufen am 12. März 2022.
- ↑ Ascherio, Alberto et al.: Longitudinal analysis reveals high prevalence of Epstein-Barr virus associated with multiple sclerosis. In: Science. 2022, doi:10.1126/science.abj8222.
- ↑ Ist das Epstein-Barr-Virus die Ursache von Multipler Sklerose? Auf: multiple-sklerose.com, abgerufen am 15. Januar 2022.
- ↑ Inês Martins PhD: EBV Infections Evident in All 901 MS Patients in German Study. Abgerufen am 12. März 2022 (amerikanisches Englisch).
- ↑ Kristin Strohschein, Madlen Loebel et al.: Deficient EBV-Specific B- and T-Cell Response in Patients with Chronic Fatigue Syndrome. In: PLOS ONE. Band 9, Nr. 1, 15. Januar 2014, ISSN 1932-6203, S. e85387, doi:10.1371/journal.pone.0085387, PMID 24454857.
- ↑ F. Alarcón: Encephalitis lethargica due to Epstein-Barr virus infection. In: Movement Disorders. Band 26, Nr. 11, 2011, S. 2132–2134, PMID 21611982.
- ↑ Julia Bonengel: Neue Studie: Zusammenhang von Schizophrenie und Epstein-Barr-Virus demonstriert. In: Medumio. 24. Januar 2019, abgerufen am 28. Juni 2021 (deutsch).