Atriumseptumdefekt
| Klassifikation nach ICD-10 | |
|---|---|
| Q21.1 | Vorhofseptumdefekt |
| ICD-10 online (WHO-Version 2019) | |
Der Atriumseptumdefekt (ASD), Vorhofseptumdefekt (unübliche Abkürzung VSD[1][2]) oder Vorhofscheidewanddefekt ist ein Loch in der Herzscheidewand zwischen den beiden Vorhöfen des Herzens (Septum interatriale). Er ist mit ca. 7,5 % aller angeborenen Herzfehler die dritthäufigste angeborene Herzfehlbildung. Ein Atriumseptumdefekt kann als alleiniger Herzfehler (singuläres Vitium), oder in Kombination mit anderen Herzfehlern auftreten, seine Auswirkung sind jeweils unterschiedlich zu bewerten.
Aufgrund des höheren Druckes im linken Vorhof fließt arterialisiertes Blut über den ASD zum rechten Vorhof und bewirkt eine Volumenbelastung des Lungenkreislaufes mit exzentrische Rechtsherzhypertrophie. Steigt als krankhafte Spätfolge der Druck im Lungenkreislauf an, kann sich die Flussrichtung umdrehen und ein zyanotisches Vitium entstehen (Eisenmenger Syndrom).
Kinder mit großem ASD leiden unter Kurzatmigkeit, Infektanfälligkeit und Gedeihstörung. Kleinere ASD bleiben nicht selten zunächst unbemerkt, im Erwachsenenalter fällt dann evtl. eine Abnahme der körperlichen Belastbarkeit auf. Septumdefekte erhöhen das Risiko für gekreuzte (= paradoxe) Embolien und Schlaganfälle. Der Embolus gelangt dabei über den Defekt vom Lungen- in den Körperkreislauf und kann nicht in den Lungenarterien „abgefangen“ werden. Neben Thrombembolien kommt dieser Mechanismus auch bei Luftembolien, Fettembolien und Fruchtwasserembolien zum Tragen.
Die Entscheidung zum Verschluss des ASD und die Wahl der Methode (katheterinterventioneller oder operativer Verschluss) erfolgen individualisiert. Zu berücksichtigen sind die Symptome, die Lage, die Öffnungsfläche (Defektgröße), das Shunt-Minutenvolumen (Shuntvolumen, Durchflussrate, Volumenstrom, Volumenfluss, Shuntzeitvolumen, Volumen pro Zeitspanne, oft angegeben als Prozentanteil vom Schlagvolumen, vom Herzzeitvolumen[3] oder vom Kleinkreislaufminutenvolumen[4] [=Lungenzeitvolumen]), die Strömungsrichtung (Rechts-links-Shunt oder Links-rechts-Shunt) und die Begleiterkrankungen. Bei kleineren ASD kann ein abwartendes Verhalten ausreichend sein, bei Säuglingen und Kleinkindern verschliesst sich der Defekt manchmal während der ersten Lebensjahre von alleine. Größere Defekte mit relevantem Shuntvolumen werden regelhaft verschlossen, bevor es zu Komplikationen oder Schäden in Folge der Volumenbelastung des Lungenkreislaufes kommt.
Ein ASD ist abzugrenzen vom Kammerseptumdefekt (syn. Ventrikelseptumdefekt, Abkürzung VSD), bei dem der Defekt einen Kurzschluss beider Herzkammern mit anderen Auswirkungen und Therapiestrategien bewirkt.
Formen[Bearbeiten | Quelltext bearbeiten]
| Klassifikation nach ICD-10 | |
|---|---|
| Q21.1 | Vorhofseptumdefekt
|
| ICD-10 online (WHO-Version 2019) | |
Der ASD tritt in fünf Varianten auf:
Offenes oder persistierendes Foramen ovale[Bearbeiten | Quelltext bearbeiten]
Die „einfachste Form“ eines Atriumseptumdefektes ist das persistierende Foramen ovale (PFO; englisch: patent [lateinisch patens ‚offen‘] foramen ovale, Abkürzung ebenfalls PFO). Es gilt als Normvariante, zumeist ohne Krankheitswert. Bis zu 30 % der Bevölkerung sind davon betroffen. Es ist daher kein Septumdefekt im engeren Sinne.[5]
Das Foramen ovale ist eine türartige Verbindung zwischen den Herzvorhöfen, die im fetalen (vorgeburtlichen) Kreislauf den Blutübertritt von rechts (Lungenkreislauf, kleiner Kreislauf) nach links (Körperkreislauf, großer Kreislauf) zulässt. Da die Lunge noch nicht belüftet ist und somit auch noch nicht relevant durchblutet wird, fließt das Blut durch das Foramen ovale in den linken Vorhof und durch den Ductus arteriosus (oder auch Ductus arteriosus Botalli) aus der Lungenschlagader in die Aorta.
Das Foramen ovale verschließt sich normalerweise in den ersten Lebenstagen oder Lebenswochen vollständig. Geschieht dies nicht, spricht man von einem persistierenden (anhaltenden, andauernden) Foramen ovale. Die betroffenen Personen werden davon in den meisten Fällen zeitlebens nicht beeinträchtigt und eine Behandlung ist in diesen Fällen nicht erforderlich. Umstritten ist, in wie fern eine Schreizyanose bei Neugeborenen darauf zurückzuführen ist.[6]
Sehr selten kommt es an einem PFO zu einer paradoxen Embolie, bei der ein venöses Blutgerinnsel das Loch passiert und z. B. einen ischämischen Schlaganfall verursacht. Der Thrombus stammt bei paradoxen Embolien meist aus den Bein- oder Beckenvenen, alternativ kann er sich auch direkt im Bereich des Septumdefektes bilden. Internationale Leitlinien empfehlen (Stand 05/2024) bei bestimmten Schlaganfallpatienten mit einem offenen Foramen ovale und moderatem oder ausgeprägten Rechts-links-Shunt zur Rezidivprophylaxe den interventionellen Verschluss des PFO.[7] Der Verschluss ist nur bei einem sehr kleinen Teil der Schlaganfallpatienten unter 60 Jahren, mit hohem RoPE-Score oder besonderer Risikokonstellation sinnvoll und setzt voraus, dass andere Ursachen des Schlaganfalles zuverlässig ausgeschlossen wurden.[8] Als Alternative zur endovaskulären Okkluder-Implantation wird eine Thrombozytenaggregationshemmung oder eventuell auch eine orale Antikoagulation zur Sekundärprävention empfohlen.[9]
Nach ersten Hinweisen im Jahr 1996 haben mittlerweile mehrere Untersuchungen einen Zusammenhang zwischen persistierendem Foramen ovale und Migräne ergeben. Der interventionelle Verschluss stellt bislang jedoch keine etablierte Therapie der Migräne dar.[10]
Bei Tauchern besteht zusätzlich eine erhöhte Gefahr von zerebralen Gasembolien (arterielle Gasblasenembolie). Auch ohne Septumdefekt zählt die Gasembolie zu den häufigen Tauchunfällen. Es ist eine Luftembolie durch Gasbläschenbildung. Siehe dazu auch Dekompressionskrankheit und Barotrauma.
Vorhofseptumaneurysma[Bearbeiten | Quelltext bearbeiten]
Manchmal tritt ein offenes Foramen ovale zusammen mit einem Vorhofseptumaneurysma (atriales Septumaneurysma, Abkürzung ASA) auf. Die Prävalenz beträgt etwa ein Prozent der Bevölkerung.[11][12] In der pädiatrischen Kardiologie werden diese Aneurysmata in Abhängigkeit von der Shuntgröße in vier Schweregrade (Typen A bis D) eingeteilt. In der aktuellen ICD-10 wird das ASA noch nicht klassifiziert; in der neuen ICD-11 wird es den Schlüssel LA8E.Y bekommen (Aneurysma of the atrial septum). Es handelt sich dabei um eine ausgeprägte Mobilität des Septums[13] (hypermobiles Septum) oder um druckbedingte (interatriale Druckdifferenz) Aussackungen oder Vorwölbungen der Herzscheidewand in das rechte Atrium (Lateraldeviation). In dieser Ausbuchtung (Aneurysma) kann es zur Bildung von Thromben (Blutgerinnseln) kommen. Dadurch wird das Risiko für einen embolischen Schlaganfall erhöht. Bei bis zu 90 Prozent der Betroffenen besteht zudem ein interatrialer Shunt als Ursache gekreuzter Embolien, nach einer Perforation liegt dieser Shunt ggf. direkt im Bereich des Aneurysmas. Oft besteht bei einem Vorhofseptumaneurysma gleichzeitig ein Vorhofflimmern als weitere Ursache für embolische Schlaganfälle.[14][15] Nach kryptogenem Schlaganfall und PFO kann der Nachweis eines ASA ein Argument für den interventionellen Verschluss zur Sekundärprophylaxe sein.[16][17][18][19]
Sekundum-Typ (Ostium-secundum-Defekt)[Bearbeiten | Quelltext bearbeiten]
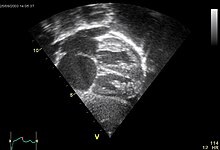
Die häufigste Form (etwa 7 % aller kongenitalen Herzfehler[20]) ist der Vorhofseptumdefekt vom Sekundumtyp, auch ASD II genannt. Das Loch liegt in der Mitte und je nach Größe fließt wegen des Druckunterschiedes in den Herzvorhöfen eine mehr oder weniger große Blutmenge von links nach rechts, also wieder in den Lungenkreislauf.
Dieser Defekt (Shunt) kann in vielen Fällen durch das Einsetzen eines Verschlusssystems mit dem Herzkatheter verschlossen werden: Ein 'Doppelschirmchen' oder ein selbstzentrierendes Metallgerüst aus Nitinol (Amplatzer-System) wird durch den Katheter in das Loch eingeführt und dort entfaltet. Nach Überwachsen mit Herzinnenhaut (Endokard) ist das Loch dauerhaft verschlossen. Voraussetzung dafür ist, dass das Loch nicht zu groß ist, mittig liegt und glatte Ränder hat. Sind diese Voraussetzungen nicht gegeben, muss das Loch chirurgisch verschlossen werden.
Eine Endokarditisprophylaxe wird beim ASD II nicht empfohlen. Eine pulmonale Hypertonie (Lungenhochdruck) durch den Shunt ist in den ersten Lebensjahrzehnten nicht zu erwarten, da der Druckunterschied in den Vorhöfen nicht sehr bedeutsam ist.
Dieser Herzfehler wird manchmal auch erst im Jugendlichen- oder im fortgeschrittenen Erwachsenenalter diagnostiziert. Es hat sich gezeigt, dass die Patienten ab einer gewissen Shuntgröße mit ansteigendem Alter oft zunehmende Beschwerden (Herzinsuffizienz) bekommen. Deshalb werden bedeutsame ASD II heute meist verschlossen, auch wenn die Patienten sich wohlfühlen.
Ein aufgrund weiterer Fehlbildungen nachgeburtlich unverschlossen gebliebenes Foramen ovale wird bei hämodynamischer Relevanz als ein ASD II eingestuft.
Ostium-primum-Typ[Bearbeiten | Quelltext bearbeiten]
Die nächst häufige Form ist der Ostium-primum-Defekt, auch ASD I genannt. Das Loch liegt im unteren Anteil der Vorhofscheidewand, reicht bis an die Klappenebene heran und ist oft mit einer Fehlfunktion der Mitralklappe (zwischen linkem Vorhof und linkem Ventrikel = Herzkammer) verbunden, seltener mit einer Fehlfunktion der Trikuspidalklappe (zwischen rechtem Vorhof und rechter Herzkammer). Zugrunde liegt diesem Herzfehler eine Hemmung der Endokardkissenbildung. Eine Herzkatheteruntersuchung oder eine transösophageale Echokardiographie („Schluckecho“) vor der Operation ist nur selten notwendig. Dieser Defekt wird immer chirurgisch mit einem Patch aus Kunststoff oder körpereigenem Gewebe verschlossen. Wird nach der Operation eine oft auftretende geringgradige Mitralklappenfehlfunktion festgestellt, muss weiter ein erhöhtes Endokarditisrisiko beachtet werden.[21]
Sinus-venosus-Typ (Sinus-venosus-Defekt)[Bearbeiten | Quelltext bearbeiten]
Eine sehr seltene Form des ASD ist der Sinus-venosus-Defekt. Er liegt im oberen Anteil der Vorhofscheidewand und in ca. 90 % der Fälle werden eine oder mehrere in den rechten Vorhof oder in die obere Hohlvene (Vena cava superior) fehleinmündende Lungenvenen nachgewiesen. Daher ist hier fast immer eine transösophageale Echokardiografie oder ein Herzkatheter vor einer Operation notwendig. Auch dieser Defekt wird chirurgisch mit einem Patch verschlossen und die Lungenvenen werden so umgesetzt, dass der normale Blutfluss in den linken Vorhof gewährleistet ist. Wie bei vielen Defekten im Vorhofbereich kommt es im Langzeitverlauf häufiger zu Herzrhythmusstörungen.
Sinus-coronarius-Defekt[Bearbeiten | Quelltext bearbeiten]
Am Sinus coronarius münden die Koronarvenen in den rechten Vorhof ein. Durch eine fehlende Überdachung am Sinus coronarius kommt es zu einer freien Verbindung zwischen beiden Vorhöfen. Auch hier besteht ein Shunt mit der Möglichkeit paradoxer Embolien. Auch dieser Defekt kann operativ verschlossen werden.
Diagnostik[Bearbeiten | Quelltext bearbeiten]
Auskultation[Bearbeiten | Quelltext bearbeiten]
Bei der körperlichen Untersuchung fällt im Rahmen der Auskultation eine Spaltung des zweiten Herztones auf, welche fixiert ist, also sich während der Ein- und Ausatmung nicht ändert. Des Weiteren findet man ein leises Systolikum im 2. ICR links (Zwischenrippenraum), welches durch die relative Verengung der Pulmonalklappe zustande kommt; durch die relative Enge der Trikuspidalklappe kann es auch zu einem am unteren Sternum betonten Diastolikum kommen.
EKG[Bearbeiten | Quelltext bearbeiten]
EKG Veränderungen sind bei vielen Patienten mit ASD nachweisbar, jedoch per se meist unspezifisch. Zu häufigen Befunden zählen der (überdrehte) Rechtslagetyp, bei Septum Primum Typ hingegen meist eine überdrehte Linkslag. Auch ein (inkompletter) Rechtsschenkelblock und T- Negativierung rechts präkordial als Ausdruck der Rechtsherzhypertrophie sind nicht ungewöhnlich.[22] Ältere Patienten können atriale Rhythmusstörung, z.B Vorhofflimmern, entwickeln.
Ultraschall[Bearbeiten | Quelltext bearbeiten]
Goldstandard zur Detektion ist die transösophagale Ultraschalluntersuchung mit einem nicht lungengängigen Kontrastmittel.[23] Manchmal ist bereits mit der Farbdopplerechokardiographie von transthorakal eine ausreichend gute Beurteilung des ASD und des Blutflusses durch den Defekt möglich.
Weitere Untersuchungen[Bearbeiten | Quelltext bearbeiten]
In einigen Fällen sind eine Herzkatheteruntersuchung, kardiale Kernspintomographie oder kardiale Computertomographie sinnvoll.
Therapie[Bearbeiten | Quelltext bearbeiten]
Bei kleinen Defekten kann eine spontane Verkleinerung oder der selbständige Verschluss abgewartet werden. Wenn jedoch bereits eine Vergrößerung der rechten Herzhälfte vorliegt, sollte ein Verschluss des Defektes im Kleinkindalter (3. oder 4. Lebensjahr) erfolgen. Auch im Kindesalter kann die Operation heutzutage minimal-invasiv durch eine seitliche Eröffnung des Brustkorbes erfolgen. Besonders bei jungen Mädchen hat sich dieser Zugang als kosmetisch günstig und sehr gut akzeptiert erwiesen.
Liegt der Defekt in der Mitte der Vorhofscheidewand, kann heute bei 70 % der Patienten ein Verschluss mit einem Doppelschirmchen durchgeführt werden. Dieses wird im Rahmen eines Herzkathetereingriffes eingesetzt. Die Durchführung kann in der Mehrzahl der Fälle unter transösophagealer echokardiografischer Kontrolle erfolgen. In Einzelfällen ist eine angiografische Darstellung erforderlich.
Bei sehr großen oder ungünstig gelegenen Defekten muss eine Operation mit Hilfe der Herz-Lungen-Maschine durchgeführt werden. Je nach Größe wird der Defekt durch direkte Naht oder mit einem Flicken aus patienteneigenem Herzbeutelgewebe verschlossen.
Risiken[Bearbeiten | Quelltext bearbeiten]
Obwohl heutzutage ein diagnostizierter Atriumseptumdefekt in der Regel verschlossen wird, stellt diese Fehlbildung ein grundsätzliches Risiko für die Betroffenen dar. Da kleinere Atriumseptumdefekte (auch bei normalen Ultraschalluntersuchungen) teilweise unbemerkt bleiben, treten beispielsweise bei vermeintlich gesunden Tauchern trotz Einhaltung aller Vorsichtsmaßnahmen Tauchunfälle auf, da die Filterfunktion der Lunge durch den Atriumseptumdefekt unvollständig bleibt, die sonst eine Embolie im Körperkreislauf verhindert. Zusätzlich muss an paradoxe zerebrale Embolien (Apoplexie) gedacht werden (siehe oben).
Geschichte[Bearbeiten | Quelltext bearbeiten]
Zumindest seit Galenos von Pergamon erkannte man das Herz als Pumpe. Man musste also erklären, wie das Blut von der rechten Herzhälfte in die linke Herzhälfte gelangt. Man behauptete die Existenz unsichtbarer Poren, durch die das Blut die Herzscheidewand durchquert. „Die schwächste Stelle im Galenischen System war zweifelsohne die Lehre von den Poren im Herzseptum.“ Solche Poren konnten nie gesehen oder beschrieben werden. Trotzdem wurde die Poren-Theorie noch gelehrt als „Realdo Colombo schon klar den Durchtritt des Blutes über die Lungen in den andern Teil des Herzens postuliert hatte.“ So wurde der Lungenkreislauf schon lange vor William Harvey (1578–1657) von Colombo (1516–1559) beschrieben: „Die Herzscheidewand ist nicht durchlässig. Alle, die das behaupten, sind auf dem Irrweg. Das Blut gelangt durch die Lunge von der rechten in die linke Herzkammer.“[24] Oder durch einen Septumdefekt nach Shuntumkehr. – Analog konnten der große Kreislauf und damit der Blutkreislauf (Circulus sanguinis minor et maior) wegen der damals ebenfalls nicht sichtbaren Kapillaren bis zur Verbreitung des Mikroskops auch von William Harvey nicht schlüssig nachgewiesen werden. Galens ‚Poren‘ befinden sich also nicht im Septum, sondern im Kapillarnetz beider Kreisläufe.
Schon Erasistratos unterschied den kleinen Lungenkreislauf vom großen Körperkreislauf und beschrieb die Herzklappen. Im 13. Jahrhundert entdeckte Ibn an-Nafis, ein arabischer Arzt und Anatom, wahrscheinlich als Erster, dass das Blut in einem Kreislauf durch die Lunge fließt. Seine Erkenntnisse, die als Zeichnungen bis in die heutige Zeit überliefert sind, gelangten jedoch nicht bis in den europäischen Raum.
Im Jahr 1952 erfolgte durch Lewis der erste Vorhofseptumdefektverschluss in Hypothermie.[25]
Literatur[Bearbeiten | Quelltext bearbeiten]
- S2k-Leitlinie Vorhofseptumdefekt der Deutschen Gesellschaft für Pädiatrische Kardiologie (DGPK). In: AWMF online (Stand 2013)
- Klaus Holldack, Klaus Gahl: Auskultation und Perkussion. Inspektion und Palpation. Thieme, Stuttgart 1955; 10., neubearbeitete Auflage ebenda 1986, ISBN 3-13-352410-0, S. 193–197.
- Franz Grosse-Brockhoff, Franz Loogen, Adalbert Schaede: Angeborene Herz- und Gefäßmißbildungen. In: Handbuch der inneren Medizin. 4. Auflage. 9. Band, 3. Teil, Springer-Verlag, Berlin / Göttingen / Heidelberg 1960, ISBN 3-540-02538-3, Spezieller Teil, Kapitel VI: Vorhofseptumdefekt, S. 249–291.
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Myron G. Sulyma: "Lexikon der Abkürzungen Herz/Kreislauf", Band M–Z, Medikon Verlag, München 1986, ISBN 3-923866-14-3, S. 497.
- ↑ Sandoz AG: "Lexikon medizinischer Abkürzungen", 7. Auflage, Nürnberg 1986, S. 244.
- ↑ Karl Vossschulte, Hanns Gotthard Lasch, Fritz Heinrich (Hrsg.): "Innere Medizin und Chirurgie", 2. Auflage, Georg Thieme Verlag, Stuttgart / New York 1981, ISBN 3-13-562602-4, S. 71.
- ↑ Walter Siegenthaler u. a. (Hrsg.): Lehrbuch der inneren Medizin. 3. Auflage, Georg Thieme Verlag, Stuttgart / New York 1992, ISBN 978-3-13-624303-9, S. 110.
- ↑ Ohne weitere Erklärung: Gerd Harald Herold et al.: Innere Medizin 2019, Eigenverlag, Köln 2018, ISBN 978-3-9814660-8-9, S. 186.
- ↑ Fritz Lange: Lehrbuch der Krankheiten des Herzens und der Blutstrombahn. Ferdinand Enke Verlag, Stuttgart 1953, S. 378.
- ↑ Peter Overbeck: Neue Leitlinie empfiehlt interventionellen PFO-Verschluss bei kryptogenem Schlaganfall. In: Cardio News. 21. Jahrgang, Nummer 9, (September) 2018, S. 12.
- ↑ DGK: Leitlinie zum PFO Verschluss. Abgerufen am 2. Mai 2024.
- ↑ Felix Jansen, Nikos Werner: Persistierendes Foramen ovale. In: Cardiovasc – Interdisziplinäre Fortbildung. 18. Jahrgang, Nummer 4, (September) 2018, S. 35–37.
- ↑ AWMF: Leitlinie zur Therapie der Migräne. Abgerufen am 2. Mai 2024.
- ↑ Heinz Lambertz, Harald Lethen (Hrsg.): "Transösophageale Echokardiographie", 2. Auflage, Georg Thieme Verlag, Stuttgart / New York 2007, ISBN 978-3-13-124572-4, S. 215–222.
- ↑ Andere Angabe: Otto M. Hess, Rüdiger W. R. Simon (Hrsg.): "Herzkatheter", Springer-Verlag, Berlin / Heidelberg 2000, ISBN 978-3-642-62957-0, S. 535: "Ein Vorhofseptumaneurysma ist hingegen mit einer Inzidenz von circa 2–3 % eher selten." Das wird wohl mit der Prävalenz verwechselt. - R. Schräder beschreibt diverse Verschlussmöglichkeiten ("Interventionelle Behandlung von Shuntvitien"), S. 526–539.
- ↑ Ursula Wilkenshoff, Irmtraut Kruck: "Handbuch der Echokardiographie", 4. Auflage, Georg Thieme Verlag, Stuttgart / New York 2008, ISBN 978-3-13-138014-2, S. 171.
- ↑ Dirk Wolfgang Droste et alii: "Paradoxe Hirnembolien als Ursache des Schlaganfalls", in: Deutsches Ärzteblatt, 99. Jahrgang, Heft 5/2002, Seiten A-281, B-224, C-211.
- ↑ Nadine Eckert: "Kryptogener Schlaganfall: Ein Schirmchen schützt – mitunter", in: Deutsches Ärzteblatt, 114. Jahrgang, Heft 42/2017, Seiten A-1930, B-1632, C-1598.
- ↑ Gerhard Bauriedel et alii: "Therapieoptionen bei symptomatischem offenen Foramen ovale: Eine aktuelle Bestandsaufnahme katheterinterventioneller Verfahren", in: Deutsches Ärzteblatt, 100. Jahrgang, Heft 34–35/2003, Seiten A-2230, B-1857, C-1760.
- ↑ Matthias Lange: "Verschluss des PFO und Schlaganfall", in: Deutsches Ärzteblatt International, 115. Jahrgang, Heft 4/2018, S. 56–57.
- ↑ C. Ochsenfahrt et alii: "Chirurgische Therapie des Vorhofseptumaneurysmas mit persistierendem Foramen ovale", in: Zeitschrift für Kardiologie, 88. Jahrgang, Ausgabe 11/1999, November 1999, S. 941–947.
- ↑ Hans-Christoph Diener, Martin Grond: "Embolic Stroke of Undetermined Source", in: "Cardiovasc – Interdisziplinäre Fortbildung", 18. Jahrgang, September 2018, Nummer 4/2018, S. 38–40.
- ↑ Reinhard Larsen: Anästhesie und Intensivmedizin in Herz-, Thorax- und Gefäßchirurgie. (1. Auflage 1986) 5. Auflage. Springer, Berlin / Heidelberg / New York u. a. 1999, ISBN 3-540-65024-5, S. 355.
- ↑ Myron G. Sulyma (Hrsg.): Wörterbuch der Kardiologie, Band I, Medikon Verlag, München 1983, ISBN 3-923866-02-X, S. 55.
- ↑ DGPK: Leitlinie ASD. Abgerufen am 2. Mai 2024.
- ↑ Solimann et al.: The use of contrast echocardiography for the detection of cardiac shunts. European Journal of Echocardiography. 2007 Jun;8(3):S2-12 PMID 17462958
- ↑ Zitat von Realdo Colombo. Quelle: Hans Schadewaldt: Über Herz und Kreislauf – Ein Rätsel für die Antike bis zur Aufklärung 1650, S. 58 und 71.
- ↑ Friedrich Wilhelm Hehrlein: Herz und große Gefäße. In: Franz Xaver Sailer, Friedrich Wilhelm Gierhake (Hrsg.): Chirurgie historisch gesehen: Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 164–185, hier: S. 182.