Terpineole
Terpineole sind eine Gruppe chemischer Verbindungen, von denen mindestens vier (α-, β-, γ- und δ-Terpineol) als sekundäre Pflanzenstoffe natürlich vorkommen. Chemisch sind es monocyclische Monoterpen-Alkohole mit der Summenformel C10H18O. Sie sind klare, farblose Flüssigkeiten mit verschiedenen, charakteristischen Gerüchen. Der Begriff Terpineol im Singular wird häufig synonym für α-Terpineol verwendet.
Struktur
[Bearbeiten | Quelltext bearbeiten]Es gibt mindestens vier strukturisomere Terpineole (siehe Abbildung), welche alles tertiäre, einwertige Alkohole sind. Terpineole sind des Weiteren strukturisomer zu Pinanol, Borneol, Myrcenol, Dihydrocarveol, Nerol, Geraniol und Linalool.
| Terpineole | |||||
| Name | (R)-(+)-α-Terpineol | (S)-(−)-α-Terpineol | β-Terpineol | γ-Terpineol | δ-Terpineol |
| Strukturformel | 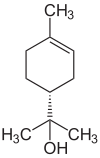 |
 |
 |
 |
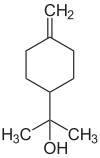
|
| CAS-Nummer | 7785-53-7 | 10482-56-1 | 138-87-4 | 586-81-2 | 7299-42-5 |
| 98-55-5 (Isomerengemisch) | |||||
| 8000-41-7 (Isomerengemisch) | |||||
| PubChem | 442501 | 443162 | 8748 | 11467 | 81722 |
| FL-Nummer | - | - | 02.097 | - | - |
| 02.014 (Isomerengemisch) | |||||
| 02.230 (Isomerengemisch) | |||||
| Summenformel | C10H18O | ||||
| Molare Masse | 154,25 g·mol−1 | ||||
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]α-Terpineol ist eine klare, farblose Flüssigkeit von hoher Viskosität, siedet bei 219 °C und erstarrt bei −34 °C. Die Dichte beträgt 0,935 g/cm3 (20 °C). Der Flammpunkt liegt bei 90 °C. Der Brechungsindex beträgt 1,48. In Wasser ist α-Terpineol nahezu unlöslich.
Der Geruch der Terpineole ist in Abhängigkeit von ihrer Struktur und ihrer Stereochemie sehr verschieden. So weist (R)-(+)-α-Terpineol einen äußerst intensiven Geruch nach Flieder auf; hingegen riecht das Stereoisomere entgegengesetzter Händigkeit, (S)-(−)-α-Terpineol, koniferenartig. Das Thiolderivat Thioterpineol ist der Stoff mit der geringsten bekannten Geruchsschwelle.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Terpineole kommen in ätherischen Ölen aus vielen Pflanzen vor, z. B. aus Sternanis,[1] Grüner Minze,[2] Thymian (Thymus vulgaris, Coridothymus capitatus),[3] Oregano (Origanum onites, Origanum vulgare),[3] Agathosma betulina,[3] Lorbeer (Laurus nobilis),[3][4] Sadebaum (Juniperus sabina),[5] Tee ( Camellia sinensis),[3] Bitterorange (Citrus aurantium),[3] Zitronenstrauch (Aloysia citrodora),[6] Ingwer (Zingiber officinale),[3] Rosmarin, Anis (Pimpinella anisum),[4] Majoran (Origanum majorana),[6] Bolivianischem Koriander (Porophyllum ruderale),[3] Thymbra-Bergminze (Satureja thymbra) Liebstöckel (Levisticum officinale),[6] Jasmin (Jasminum officinale),[7] Ysop (Hyssopus officinalis),[8] Salbei (Salvia officinalis)[4], Wacholder (Juniperus communis)[4] oder "Hanf" (Cannabis sativa)[9]. Sie finden sich auch im Terpentin. Das ätherische Öl aus Kurkuma enthält bis zu 500 ppm Terpineol, in den Samen des Muskatnussbaums kommen bis zu 9600 ppm α-Terpineol vor.
-
Wacholder
-
Grüne Minze
-
Thymian
-
Oregano
-
Majoran
-
Jasmin
-
Salbei
-
Ingwer
-
Anissamen
Synthese
[Bearbeiten | Quelltext bearbeiten]Racemisches α-Terpineol kann man wie folgt synthetisieren: Isopren wird mit Acrylsäuremethylester in einer Diels-Alder-Reaktion zu racemischen 4-Methylcyclohex-3-en-1-carbonsäuremethylester umgesetzt. Hierbei ist, aufgrund des geringen Siedepunkts von Isopren, die durch Lewissäure katalysierte Variante vorzuziehen. Dieser ergibt in einer Grignard-Reaktion mit Methylmagnesiumbromid (CH3MgBr, Grignard-Reagenz) nach der Hydrolyse α-Terpineol als Racemat:
α-Terpineol lässt sich im sauren Milieu auch aus den Cis-trans-Isomeren Geraniol und Nerol herstellen. β-Terpineol wird über 1,8-Dihydroxy-p-menthan hergestellt.
Technisch wird α-Terpineol durch Hydratation von α-Pinen oder Terpentinöl mit Säure (ergibt cis-Terpinhydrat) und anschließender teilweiser Dehydratation in Anwesenheit schwacher Säuren oder säureaktivierten Silicagels hergestellt.
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Aus α-Terpineol entsteht durch Hydrierung p-Menthan-8-ol, Dehydratisierung ergibt eine Mischung ungesättigter Terpen-Kohlenwasserstoffe. Die für die Parfumindustrie wichtigste Reaktion ist die Veresterung, insbesondere zu Terpinylacetat.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Terpineole sind Duftstoffe. Sie werden z. B. in Seifen und Parfums verwendet. Am häufigsten nimmt man ein Gemisch aus α- und γ-Terpineol für intensiven Fliederduft.
In der Schweiz und einigen Staaten der EU, nicht aber in Deutschland oder Österreich sind Pflanzenschutzmittel mit Terpineol als Haft- und Netzmittel zugelassen.[10]
Literatur
[Bearbeiten | Quelltext bearbeiten]- H. Surburg und J. Panten: Common Fragrance and Flavor Materials: preparation, properties, and uses. Wiley-VCH, Weinheim 2006, ISBN 3-527-31315-X.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Jayanta Kumar Patra, Gitishree Das, Sankhadip Bose, Sabyasachi Banerjee, Chethala N. Vishnuprasad, Maria Pilar Rodriguez‐Torres, Han‐Seung Shin: Star anise (Illicium verum): Chemical compounds, antiviral properties, and clinical relevance. In: Phytotherapy Research. Band 34, Nr. 6, Juni 2020, S. 1248–1267, doi:10.1002/ptr.6614.
- ↑ Massimo Maffei, Arnaldo Codignola, Maurizio Fieschi: Essential oil fromMentha spicata L. (spearmint) cultivated in Italy. In: Flavour and Fragrance Journal. Band 1, Nr. 3, Juni 1986, S. 105–109, doi:10.1002/ffj.2730010303.
- ↑ a b c d e f g h 4-TERPINEOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ a b c d TERPINEOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ (+)-TERPINEOL-(4) (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ a b c D-ALPHA-TERPINEOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ L-ALPHA-TERPINEOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ D-TERPINEOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2021.
- ↑ Nils Günnewich, Jonathan E. Page, Tobias G. Köllner, Jörg Degenhardt, Toni M. Kutchan: Functional Expression and Characterization of Trichome-Specific (-)-Limonene Synthase and (+)-α-Pinene Synthase from Cannabis sativa. In: Natural Product Communications. Band 2, Nr. 3, März 2007, S. 1934578X0700200, doi:10.1177/1934578X0700200301.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Terpenoid blend QRD-460 in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 7. Dezember 2019.









