Kongorot
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kongorot | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C32H22N6Na2O6S2 | ||||||||||||||||||
| Kurzbeschreibung |
rotbrauner geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 696,66 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR)[5] | ||||||||||||||||||
| MAK |
Deutschland: 4 mg·m−3 (gemessen als einatembarer Staub) bzw. 0,3 mg·m−3 (gemessen als alveolengängiger Staub)[6] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Kongorot gehört, wie auch Methylorange und Methylrot, zur Gruppe der Azofarbstoffe und wird unter anderem als pH-Indikator verwendet. Die Farbe von Kongorot schlägt bei pH 3,0 bis 5,2 von Blauviolett nach Rotorange um. Es eignet sich daher als Indikator für die Säure-Base-Titration.
Die Strukturformel zeigt Kongorot als Dinatriumsalz, bei dem beide Sulfonsäuregruppen (–SO3H) deprotoniert vorliegen. Die Werte der Tabelle beziehen sich ebenfalls auf das Salz.
Geschichte[Bearbeiten | Quelltext bearbeiten]
Kongorot war der erste Direktfarbstoff, der als solcher erkannt wurde,[8] und wurde 1883 von Paul Böttiger entwickelt, der zu dieser Zeit bei den Friedrich-Bayer-Werken angestellt war.[9] Da Bayer kein Interesse an dem neuen Farbstoff zeigte und Böttiger das Unternehmen verließ,[10][11] patentierte er die Verbindung selbst,[12] und bot sie erst Bayer, dann der BASF und später Hoechst an, welche aber alle ablehnten.[10][11] Schließlich verkaufte er das Patent an Agfa,[10] die später ein Kartell mit Bayer einging. Ein 1889 begonnener Patentprozess um Kongorot in Berlin führte das Patentmerkmal des technischen Effekts (in diesem Fall die Eigenschaft der Direktfärbung) ein.[13]
Der Name Kongorot wurde 1885 durch die Agfa (damals in Berlin) aus Marketinggründen eingeführt. Der historische Hintergrund ist vermutlich, dass in Berlin gerade die Kongokonferenz zu Ende gegangen war und daher der Begriff Kongo in aller Munde war.[14]
Darstellung[Bearbeiten | Quelltext bearbeiten]
Kongorot erhält man durch Tetrazotierung von Benzidin und Kupplung auf 4-Aminonaphthalin-1-sulfonsäure.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Die Farbe von Kongorot schlägt bei einem pH-Wert von 3,0 bis 5,2 von Blauviolett nach Rot um. Im Fotometer zeigt sich ein Absorptionsmaximum bei ca. 500 nm (pH > 6) bzw. 647 nm und 590 nm (pH < 3).
-
Absorptionsspektrum von Kongorot
-
Kongorot und Kongopapier bei drei verschiedenen pH-Werten
Verwendung[Bearbeiten | Quelltext bearbeiten]
Als Kongopapier bezeichnet man ein Indikatorpapier ähnlich dem Lackmuspapier. Es zeigt einen Farbumschlag von Rot nach Blau bei abnehmendem pH-Wert von 5,0 bis 3,0. Es dient speziell zum Nachweis von Milchsäure, z. B. in Bakterienkulturen (Kolibakterien), zur Neutralisationsanalyse sowie zum Nachweis von Säuren, etwa freier Salzsäure.[15]
In der Biologie wird Kongorot z. B. bei Fütterungsversuchen verwendet. Einzeller werden mit Hefen, die mit Kongorot gefärbt wurden, gefüttert, wobei man die Aufnahme der Nahrung und die enzymatische Verdauung beobachten kann.
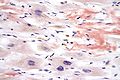
In der Pathologie dient Kongorot zur Darstellung von Amyloidablagerungen, die auf eine Amyloidose hinweisen.[16]
In der Mykologie ist Kongorot ein Färbereagenz zum Anfärben von Pilzhyphen. Es wird als wässrige Lösung in Verbindung mit Ammoniak oder Natriumdodecylsulfat (SDS) eingesetzt[17].
-
Anfärbung von Amyloid bei einer kardialen Amyloidose
-
Anfärbung von Amyloid in der Wand meningealer Blutgefäße bei der zerebralen Amyloidangiopathie
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Da unter reduktiven Bedingungen aus Kongorot wieder das kanzerogene Benzidin freigesetzt werden kann, gehört dieser Farbstoff, wie Benzidin selbst, zu den verbotenen Stoffen nach der Bedarfsgegenständeverordnung (BedGgstV) und darf nicht für Textil- und Ledererzeugnisse verwendet werden, die längere Zeit mit der menschlichen Haut oder der Mundhöhle direkt in Berührung kommen können (z. B. Kleidung, Bettwäsche, Handtücher, Schuhe, Handschuhe, für den Endverbraucher bestimmte Garne und Gewebe).[18][19]
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f Eintrag zu Dinatrium-3,3′-((1,1′-biphenyl)-4,4′-diylbis(azo))bis(4-aminonaphthalin-1-sulfonat) in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Kongorot (freie Säure): CAS-Nummer: 14684-01-6, PubChem: 11314, ChemSpider: 21865348, Wikidata: Q27104437.
- ↑ Gefahrstoffdatenbank der Länder, 19. Juni 2007.
- ↑ Eintrag zu Disodium 3,3′-[[1,1′-biphenyl]-4,4′-diylbis(azo)]bis(4-aminonaphthalene-1-sulphonate) im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 18. Oktober 2015.
- ↑ Datenblatt Kongorot (C.I. 22120) (PDF) bei Carl Roth, abgerufen am 9. November 2015.
- ↑ Datenblatt Kongorot (C.I. 22120) bei Merck, abgerufen am 4. Februar 2018.
- ↑ Heinrich Zollinger: Chemie der Azofarbstoffe. In: Lehrbücher und Monographien aus dem Gebiete der exakten Wissenschaften. Chemische Reihe. Band 13. Birkhäuser, Basel 2014, ISBN 978-3-0348-6838-9, S. 195.
- ↑ C. Röcken, N. Widulin, T. Schnalke: Die Amyloidosen des Berliner Medizinhistorischen Museums der Charité. In: Der Pathologe. Band 30, Nr. 3, Mai 2009, S. 226, doi:10.1007/s00292-009-1135-2.
- ↑ a b c Wolfgang von Hippel: Die BASF: Eine Unternehmensgeschichte. Hrsg.: Werner Abelshauser. 2. Auflage. C. H. Beck, München 2003, ISBN 3-406-49526-5, S. 69.
- ↑ a b Erik Verg, Gottfried Plumpe, Heinz Schultheis: Meilensteine 125 Jahre Bayer 1863 – 1988. Informedia, Köln 1988, ISBN 3-921349-48-6, S. 77 (bayer.com [PDF; 86,0 MB]).
- ↑ Patent DE28753C: Verfahren zur Darstellung von Azofarbstoffen durch Combination von Tetrazodipenylsalzen mit α- und β-Napthylamin oder deren Mono- und Disulfonsäuren. Angemeldet am 27. Februar 1884, veröffentlicht am 20. August 1884, Anmelder: Paul Böttiger, Erfinder: Paul Böttiger.
- ↑ Walter Beil: 75 Jahre „Congoroth-Entscheidung“. In: Chemie Ingenieur Technik – CIT. Band 36, Nr. 5, Mai 1964, S. 572, doi:10.1002/cite.330360525.
- ↑ David P. Steensma: „Congo Red“, Out of Africa? In: Archives of pathology & laboratory medicine. Band 125, Nummer 2, Februar 2001, S. 250–252, doi:10.5858/2001-125-0250-CR. PMID 11175644. (PDF)
- ↑ Kehrer, Erwin: Die physiologischen und pathologischen Beziehungen der weiblichen Sexualorgane zum Tractus intestinalis und besonders zum Magen (1905) (zum Salzsäurenachweis mit Kongopapier). (Digitalisat).
- ↑ wissenschaft-online.de: Hoffnungsvoller Kontrast, abgerufen am 25. Juni 2007.
- ↑ Heinz Clemencon: Methods for Working with macrofungi. Hrsg.: IHW-Verlag, 2009. ISBN 978-3-930167-73-9.
- ↑ Bedarfsgegenständeverordnung, Anlage 1 (zu § 3). Stoffe, die bei dem Herstellen oder Behandeln von bestimmten Bedarfsgegenständen nicht verwendet werden dürfen. Bundesministerium der Justiz und für Verbraucherschutz, abgerufen am 29. Oktober 2019.
- ↑ Eintrag zu Azofarbstoffe auf Benzidinbasis in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. November 2008. (JavaScript erforderlich)