„Toll-like-Rezeptoren“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Kuebi (Diskussion | Beiträge) K →Struktur und Liganden: steht weiter unten schon |
Ghilt (Diskussion | Beiträge) →Struktur und Liganden: + Tabelle aus en.wp |
||
| Zeile 25: | Zeile 25: | ||
TLR5 wird hauptsächlich in der ''[[Lamina propria]]'' exprimiert, wo es bakterielles Flagellin erkennt. Als Immunantwort darauf induziert TLR5 die Ausdifferenzierung von B-Zellen in lgA-produzierende Blutzellen und von T-Zellen in antigenspezifische Th17- und Th1-Zellen. TLR11 das nur in der Maus, aber nicht im Menschen vorkommt, zeigt große Ähnlichkeiten zu TLR5. Es erkennt ein Profilin-ähnliches Molekül, das vom intrazellulären [[Protozoen|Protozoon]] ''[[Toxoplasma gondii]]'' abstammt. |
TLR5 wird hauptsächlich in der ''[[Lamina propria]]'' exprimiert, wo es bakterielles Flagellin erkennt. Als Immunantwort darauf induziert TLR5 die Ausdifferenzierung von B-Zellen in lgA-produzierende Blutzellen und von T-Zellen in antigenspezifische Th17- und Th1-Zellen. TLR11 das nur in der Maus, aber nicht im Menschen vorkommt, zeigt große Ähnlichkeiten zu TLR5. Es erkennt ein Profilin-ähnliches Molekül, das vom intrazellulären [[Protozoen|Protozoon]] ''[[Toxoplasma gondii]]'' abstammt. |
||
Eine Reihe von TLRs, darunter TLR3, TLR7, TLR8 und TLR9 erkennen aus Viren oder Bakterien stammende Nukleinsäuren. Die Aktivierung dieser TLRs führt zur Bildung von Alpha-Interferon und anderen [[entzündung]]sauslösenden [[Zytokin]]en. TLR3 entdeckt virale doppelsträngige RNA im Endolysosom. Hierbei bindet die dsRNA an das N-terminale und das [[C-Terminus|C-terminale]] Ende der LRR-Sequenz. |
Eine Reihe von TLRs, darunter TLR3, TLR7, TLR8 und TLR9 erkennen aus Viren oder Bakterien stammende Nukleinsäuren. Die Aktivierung dieser TLRs führt zur Bildung von Alpha-Interferon und anderen [[entzündung]]sauslösenden [[Zytokin]]en. TLR3 entdeckt virale doppelsträngige RNA im Endolysosom. Hierbei bindet die dsRNA an das N-terminale und das [[C-Terminus|C-terminale]] Ende der LRR-Sequenz. |
||
{| class="wikitable" |
|||
! [[Rezeptor (Biochemie)|Rezeptor]] !! [[Ligand]]en<ref name=Immunology17Unless/> !! Ursprung der Liganden<ref name=Immunology17Unless>Unless else specified in boxes then ref is: {{cite book |author=Waltenbaugh C, Doan T, Melvold R, Viselli S |series=Lippincott's Illustrated reviews | title=Immunology |publisher=Wolters Kluwer Health/Lippincott Williams & Wilkins |location=Philadelphia |year=2008 |pages=17 |isbn=978-0-7817-9543-2 |oclc= |doi=}}</ref>!! Adapterprotein des TLR !! Zelluläre Lokalisation !! [[Zelltyp]]en<ref name=Immunology17Unless/> |
|||
|- |
|||
| [[TLR 1]] || Verschiedene Triacyl-[[Lipopeptide]] || Bakterielles Lipoprotein || [[MyD88]]/MAL || Zelloberfläche || |
|||
* [[Monozyt]]en/[[Makrophage]]n |
|||
* Eine Untergruppe der [[Dendritische Zelle|dendritischen Zellen]] |
|||
* [[B-Lymphozyt]]en |
|||
|- |
|||
| rowspan="6" | [[TLR 2]] || Verschiedene [[Glycolipid]]e || Bakterielle Peptidoglykane || rowspan="6" | MyD88/MAL || rowspan="6" | Zelloberfläche || rowspan="6" | |
|||
* Monozyten/Makrophagen |
|||
* [[Neutrophile]]<ref name="Sabroe 2005 S421–426">{{cite journal | author = Sabroe I, Dower SK, Whyte MK | title = The role of Toll-like receptors in the regulation of neutrophil migration, activation, and apoptosis | journal = Clinical Infectious Diseases | volume = 41 Suppl 7 | pages = S421-6 | date = November 2005 | pmid = 16237641 | doi = 10.1086/431992 }}</ref> |
|||
* Myeloide dendritische Zellen<ref name="Dendritic">{{cite journal | author = Sallusto F, Lanzavecchia A | title = The instructive role of dendritic cells on T-cell responses | journal = Arthritis Research | volume = 4 Suppl 3 | issue = | pages = S127-32 | year = 2002 | pmid = 12110131 | pmc = 3240143 | doi = 10.1186/ar567 }}</ref> |
|||
* [[Mastzelle]]n |
|||
|- |
|||
| Verschiedene Lipopeptide und [[Proteolipide]] || Bakterielle Peptidoglycane |
|||
|- |
|||
| [[Lipoteichonsäure]] || [[Gram-positiv]]e Bakterien |
|||
|- |
|||
| [[HSP70]] || Wirtszellen |
|||
|- |
|||
| [[Zymosan]] ([[Beta-Glucan]]) || [[Pilze]] |
|||
|- |
|||
| Zahlreiche Andere || |
|||
|- |
|||
| [[TLR 3]] |
|||
| Doppelsträngige [[RNA]], [[Poly I:C]] |
|||
| [[Viren]] |
|||
| [[TRIF]] |
|||
| Zellkompartiment |
|||
| |
|||
* Dendritische Zellen |
|||
* B-Lymphozyten |
|||
|- |
|||
| rowspan=7| [[TLR 4]] |
|||
|| [[Lipopolysaccharid]] || [[Gram-negativ]]e Bakterien || rowspan=7| MyD88/MAL/[[TRIF]]/TRAM || rowspan=7| Zelloberfläche || rowspan=7| |
|||
* Monozyten/Makrophagen |
|||
* Neutrophile<ref name="Sabroe 2005 S421–426"/> |
|||
* Myeloide dendritische Zellen<ref name=Dendritic /> |
|||
* Mastzellen |
|||
* B-Lymphozyten<ref>{{cite journal | author = Gerondakis S, Grumont RJ, Banerjee A | title = Regulating B-cell activation and survival in response to TLR signals | journal = Immunology and Cell Biology | volume = 85 | issue = 6 | pages = 471–5 | year = 2007 | pmid = 17637697 | doi = 10.1038/sj.icb.7100097 }}</ref> |
|||
* [[Darmepithel]]<ref>{{cite journal | author = Cario E, Rosenberg IM, Brandwein SL, Beck PL, Reinecker HC, Podolsky DK | title = Lipopolysaccharide activates distinct signaling pathways in intestinal epithelial cell lines expressing Toll-like receptors | journal = Journal of Immunology | volume = 164 | issue = 2 | pages = 966–72 | date = January 2000 | pmid = 10623846 | doi = 10.4049/jimmunol.164.2.966 }}</ref> |
|||
* Brustkrebszellen |
|||
|- |
|||
| Mehrere [[Hitzeschockprotein]]e || Bakterien und Wirtszellen |
|||
|- |
|||
| [[Fibrinogen]] || Wirtszellen |
|||
|- |
|||
| [[Heparansulfat]]fragmente || Wirtszellen |
|||
|- |
|||
| [[Hyaluronsäure]]fragmente || Wirtszellen |
|||
|- |
|||
| [[Nickel]]<ref>{{cite journal | author = Peana M, Zdyb K, Medici S, Pelucelli A, Simula G, Gumienna-Kontecka E, Zoroddu MA | title = Ni(II) interaction with a peptide model of the human TLR4 ectodomain | journal = Journal of Trace Elements in Medicine and Biology | volume = 44 | pages = 151–160 | date = December 2017 | pmid = 28965571 | doi = 10.1016/j.jtemb.2017.07.006 }}</ref> || |
|||
|- |
|||
| Verschiedene [[Opioide]] || |
|||
|- |
|||
| rowspan=2| [[TLR 5]] || Bakterielles [[Flagellin]] || Bakterien || rowspan=2| MyD88 || rowspan=2| Zelloberfläche || rowspan=2| |
|||
* Monozyten/Makrophagen |
|||
* Eine Untergruppe der dendritischen Zellen |
|||
* Darmepithel |
|||
* Brustkrebszellen |
|||
|- |
|||
| [[Profilin]]<ref>{{cite journal | author = Salazar Gonzalez RM, Shehata H, O'Connell MJ, Yang Y, Moreno-Fernandez ME, Chougnet CA, Aliberti J | title = Toxoplasma gondii- derived profilin triggers human toll-like receptor 5-dependent cytokine production | journal = Journal of Innate Immunity | volume = 6 | issue = 5 | pages = 685–94 | year = 2014 | pmid = 24861338 | pmc = 4141014 | doi = 10.1159/000362367 }}</ref> || ''[[Toxoplasma gondii]]'' |
|||
|- |
|||
| rowspan=1| [[TLR 6]] || Verschiedene Diacyl-Lipopeptide || [[Mycoplasma]] || MyD88/MAL || Zelloberfläche || |
|||
* Monozyten/Makrophagen |
|||
* Mastzellen |
|||
* B-Lymphozyten |
|||
|- |
|||
| rowspan="5" | [[TLR 7]] || [[Imidazochinolin]] || rowspan="4" | Niedermolekulare synthetische Stoffe || rowspan="5" | MyD88 || rowspan="5" | Zellkompartiment || rowspan="5" | |
|||
* Monozyten/Makrophagen |
|||
* Plasmazytoide dendritische Zellen<ref name=Dendritic/> |
|||
* B-Lymphozyten |
|||
|- |
|||
| [[Loxoribin]] (ein [[Guanosin]]analogon) |
|||
|- |
|||
| [[Bropirimin]] |
|||
|- |
|||
| [[Resiquimod]] |
|||
|- |
|||
| Einzelsträngige RNA || RNA-Viren |
|||
|- |
|||
| [[TLR 8]] || Niedermolekulare synthetische Stoffe, einzelsträngige virale RNA, [[Phagozytose|phagozytierte]] bakterielle RNA || || MyD88 || Zellkompartiment || |
|||
* Monozyten/Makrophagen |
|||
* Eine Untergruppe der dendritischen Zellen |
|||
* Mastzellen |
|||
* Darmepithelzellen bei [[Morbus Crohn]] oder [[Ulzerative Colitis|ulzerativer Colitis]] |
|||
|- |
|||
| [[TLR 9]] || Unmethylierte [[CpG-Oligonukleotid]]e (DNA) || Bakterien, DNA-Viren || MyD88 || Zellkompartiment || |
|||
* Monozyten/Makrophagen |
|||
* Plasmacytoide dendritische Zellen<ref name=Dendritic/> |
|||
* B-Lymphozyten |
|||
|- |
|||
| [[TLR 10]] || Triacylierte Lipopeptide<ref name="pmid20348427">{{cite journal | author = Guan Y, Ranoa DR, Jiang S, Mutha SK, Li X, Baudry J, Tapping RI | title = Human TLRs 10 and 1 share common mechanisms of innate immune sensing but not signaling | journal = Journal of Immunology (Baltimore, Md. : 1950) | volume = 184 | issue = 9 | pages = 5094–103 | date = May 2010 | pmid = 20348427 | doi = 10.4049/jimmunol.0901888 }}</ref>|| || unbekannt || Zelloberfläche || |
|||
* B-Lymphozyten<ref name="pmid11267672">{{cite journal | author = Chuang T, Ulevitch RJ | title = Identification of hTLR10: a novel human Toll-like receptor preferentially expressed in immune cells | journal = Biochimica Et Biophysica Acta | volume = 1518 | issue = 1-2 | pages = 157–61 | date = March 2001 | pmid = 11267672 | doi = 10.1016/s0167-4781(00)00289-x }}</ref><ref name="pmid11970999">{{cite journal | author = Hornung V, Rothenfusser S, Britsch S, Krug A, Jahrsdörfer B, Giese T, Endres S, Hartmann G | title = Quantitative expression of toll-like receptor 1-10 mRNA in cellular subsets of human peripheral blood mononuclear cells and sensitivity to CpG oligodeoxynucleotides | journal = Journal of Immunology | location = Baltimore, Md. : 1950 | volume = 168 | issue = 9 | pages = 4531–7 | date = May 2002 | pmid = 11970999 | doi = 10.4049/jimmunol.168.9.4531 }}</ref> |
|||
* Darmepithelzellen<ref name="Regan_2013">{{cite journal | author = Regan T, Nally K, Carmody R, Houston A, Shanahan F, Macsharry J, Brint E | title = Identification of TLR10 as a key mediator of the inflammatory response to Listeria monocytogenes in intestinal epithelial cells and macrophages | journal = Journal of Immunology | volume = 191 | issue = 12 | pages = 6084–92 | date = December 2013 | pmid = 24198280 | doi = 10.4049/jimmunol.1203245 }}</ref> |
|||
* Monozyten/Makrophagen<ref name="Regan_2013" /> |
|||
|- |
|||
| [[TLR 11]] || [[Profilin]] || ''[[Toxoplasma gondii]]''<ref>{{cite journal | author = Yarovinsky F, Zhang D, Andersen JF, Bannenberg GL, Serhan CN, Hayden MS, Hieny S, Sutterwala FS, Flavell RA, Ghosh S, Sher A | title = TLR11 activation of dendritic cells by a protozoan profilin-like protein | journal = Science | volume = 308 | issue = 5728 | pages = 1626–9 | date = June 2005 | pmid = 15860593 | doi = 10.1126/science.1109893 | bibcode = 2005Sci...308.1626Y }}</ref> || MyD88 || Zellkompartiment<ref name="pmid21097503">{{cite journal | author = Pifer R, Benson A, Sturge CR, Yarovinsky F | title = UNC93B1 is essential for TLR11 activation and IL-12-dependent host resistance to Toxoplasma gondii | journal = The Journal of Biological Chemistry | volume = 286 | issue = 5 | pages = 3307–14 | date = February 2011 | pmid = 21097503 | pmc = 3030336 | doi = 10.1074/jbc.M110.171025 }}</ref>|| |
|||
* Monozyten/Makrophagen |
|||
* [[Hepatozyt]]en |
|||
* [[Nephrozyt]]en |
|||
* [[Harnblase]]nepithel |
|||
|- |
|||
| [[TLR 12]] || [[Profilin]] || ''[[Toxoplasma gondii]]''<ref>{{cite journal | author = Koblansky AA, Jankovic D, Oh H, Hieny S, Sungnak W, Mathur R, Hayden MS, Akira S, Sher A, Ghosh S | title = Recognition of profilin by Toll-like receptor 12 is critical for host resistance to Toxoplasma gondii | journal = Immunity | volume = 38 | issue = 1 | pages = 119–30 | date = January 2013 | pmid = 23246311 | pmc = 3601573 | doi = 10.1016/j.immuni.2012.09.016 }}</ref> || MyD88 || Zellkompartiment || |
|||
* [[Neuron]]en<ref name=TLR11-13>{{cite journal | author = Mishra BB, Gundra UM, Teale JM | title = Expression and distribution of Toll-like receptors 11-13 in the brain during murine neurocysticercosis | journal = Journal of Neuroinflammation | volume = 5 | issue = | pages = 53 | date = December 2008 | pmid = 19077284 | pmc = 2631477 | doi = 10.1186/1742-2094-5-53 }}</ref> |
|||
* Plasmazytoide dendritische Zellen |
|||
* Klassische dendritische Zellen |
|||
* Makrophagen |
|||
|- |
|||
| [[TLR 13]]<ref>{{cite journal | author = Shi Z, Cai Z, Sanchez A, Zhang T, Wen S, Wang J, Yang J, Fu S, Zhang D | title = A novel Toll-like receptor that recognizes vesicular stomatitis virus | journal = The Journal of Biological Chemistry | volume = 286 | issue = 6 | pages = 4517–24 | date = February 2011 | pmid = 21131352 | pmc = 3039399 | doi = 10.1074/jbc.M110.159590 }}</ref><ref>{{cite journal | author = Oldenburg M, Krüger A, Ferstl R, Kaufmann A, Nees G, Sigmund A, Bathke B, Lauterbach H, Suter M, Dreher S, Koedel U, Akira S, Kawai T, Buer J, Wagner H, Bauer S, Hochrein H, Kirschning CJ | title = TLR13 recognizes bacterial 23S rRNA devoid of erythromycin resistance-forming modification | journal = Science | volume = 337 | issue = 6098 | pages = 1111–5 | date = August 2012 | pmid = 22821982 | doi = 10.1126/science.1220363 | bibcode = 2012Sci...337.1111O }}</ref> || Bakterielle ribosomale RNA-Sequenz CGGAAAGACC (unmethyliert)<ref name="pmid23802068">{{cite journal | author = Hochrein H, Kirschning CJ | title = Bacteria evade immune recognition via TLR13 and binding of their 23S rRNA by MLS antibiotics by the same mechanisms | journal = Oncoimmunology | volume = 2 | issue = 3 | pages = e23141 | date = March 2013 | pmid = 23802068 | pmc = 3661153 | doi = 10.4161/onci.23141 }}</ref> || Viren, Bakterien || MyD88, TAK-1|| Zellkompartiment || |
|||
* Monozyten/Makrophagen |
|||
* Klassische dendritische Zellen |
|||
|} |
|||
== Die intrazelluläre Signalkaskade == |
== Die intrazelluläre Signalkaskade == |
||
Version vom 26. April 2020, 00:13 Uhr
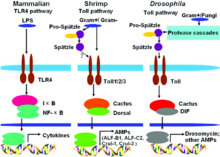
Toll-like-Rezeptoren (kurz TLR, englisch toll-like receptor) sind Strukturen des sogenannten angeborenen Abwehrsystems (innate immunity) und gehören zu einer Gruppe von Rezeptoren, den PRRs (Pattern-Recognition Receptors). Sie dienen der Erkennung von PAMPs (Pathogen-Associated Molecular Patterns), das sind Strukturen, welche ausschließlich auf oder in Krankheitserregern vorkommen, und steuern entsprechende Aktivierungen von Genen. Hierdurch wird die Aktivierung des „antigen-spezifischen erworbenen Immunsystems“ (antigen-specific acquired immunity) eingeleitet und moduliert. Durch die „toll-like receptors“ vermag das angeborene Abwehrsystem zwischen „selbst“ und „nicht selbst“ zu unterscheiden.[1] TLRs werden im Allgemeinen in dendritischen Zellen und Macrophagen exprimiert, wenig bis gar nicht in Epithelzellen.
Der Name Toll-like-Rezeptor (in der deutschsprachigen Literatur als Signaltransduktions-vermittelnde PRRs[1] oder selten auch als Toll-artiger Rezeptor bezeichnet) ist von einem Protein bei Drosophila melanogaster abgeleitet, über dessen Entdeckung die Forschungsgruppe um die Nobelpreisträgerin Christiane Nüsslein-Volhard derart begeistert war, dass sie es humorvoll nach dem deutschen Ausdruck toll nannte. TLRs bestehen aus Proteinen, die Toll ähneln, also toll-like sind.
Seit der Entdeckung des ersten Toll-like-Rezeptoren Mitte der 1990er Jahre sind immer wieder neue Varianten in Menschen und Tieren entdeckt worden. TLRs finden sich in allen Vertebraten aber auch in einfacheren Organismen, wie zum Beispiel in Drosophila melanogaster, was nahelegt, dass es sich um ein evolutionär sehr altes System handelt. Die meisten Spezies verfügen über mehr als zehn verschiedene (bekannte) TLRs, wobei manche Typen z. B. in der Maus, jedoch nicht im Menschen vorkommen.
TLRs erkennen verschiedene funktionale Bestandteile von Viren, Bakterien und Pilzen und können so biochemische Reaktionsketten in den Zellen auslösen, die der Abwehr dieser Krankheitserreger dienen.
Entdeckung der TLRs
Als Mikroganismen erstmals als die Ursache für Infektionskrankheiten identifiziert wurden, war klar, dass mehrzellige Organismen diese erkennen können müssen, und dass es dafür notwendig ist, für Mikroorganismen typische Molekülstrukturen zu erkennen. Eine große Menge an Literatur, die den Großteil des 20. Jahrhunderts umfasste, widmet sich den Schlüsselmolekülen und ihren Rezeptoren. Vor mehr als 100 Jahren prägte Richard Pfeiffer, ein Schüler von Robert Koch, den Begriff ‚Endotoxin‘, um eine Substanz, die von gramnegativen Bakterien produziert wurde und bei Tierversuchen zu Fieber und Schockzuständen führte, zu benennen. In den folgenden Jahrzehnten wurden die Endotoxine chemisch charakterisiert und als Lipopolysaccharide (LPS), die von den meisten gramnegativen Bakterien produziert werden, identifiziert. Es wurde gezeigt, dass auch andere Moleküle (bakterielle Lipopeptide, Flagelline und nicht methylierte DNA) zu einer Immunantwort führen. Logischerweise wurde daraus geschlossen, dass es Rezeptoren geben muss, die in der Lage sind, eine Immunantwort für solche Molekülstrukturen herbeizuführen. Diese wurden jedoch viele Jahre lang nicht gefunden.
In der Mitte der 1990er wurde durch Forschungen im Bereich der Entwicklungsbiologie von Drosophila melanogaster eher zufällig erkannt, dass Toll-negative Mutanten sehr anfällig gegen Pilzbefall sind.[2] Diese Beobachtung leitete eine gezielte Suche nach ähnlichen Proteinen in Säugerzellen ein. 1994 konnte von Nomura und Kollegen der erste menschliche TLR gefunden werden, der 1996 von Taguchi und Kollegen einem Chromosom zugeordnet werden konnte. Dies zeigt, dass es sich bei der über Toll-like Receptor vermittelten Immunantwort um eine evolutionär sehr alte Form handelt, die genetisch hochkonserviert ist. Da die Rolle der TLRs bei der Immunabwehr zum damaligen Zeitpunkt noch nicht bekannt war, wurde angenommen, dass TLR1 in der Entwicklungsbiologie der Säugetiere eine Rolle spielen würde. 1997 zeigten Charles Janeway und Ruslan Medzhitov, dass ein Toll-like Receptor, wenn er künstlich an entsprechende Antikörper gebunden wird, bestimmte Gene aktivieren kann, die für eine adaptive Immunantwort nötig sind. Die Funktion des TLR4 als LPS-Rezeptor wurde von Bruce A. Beutler und Kollegen entdeckt. Im Laufe der Zeit wurden auch die Liganden der anderen TLRs bestimmt. Shizuo Akira nahm dabei eine zentrale Rolle ein.
Struktur und Liganden
Die gemeinsamen Strukturmerkmale aller Toll-like-Rezeptoren sind die N-terminalen leucinreichen LRR-Sequenzen (Leucine-rich Repeats) und die TIR-Domain (Toll/IL-1R homology domain). Die unterschiedlichen TLRs können jeweils unterschiedliche PAMPs (Pathogen Associated Molecular Patterns) durch direkte Interaktion mit der jeweiligen Membranoberfläche des Krankheitserregers identifizieren. TLR3, TLR7, TLR8 und TLR9 befinden sich an der Membran von Endosomen bzw. Endolysosomen, während die restlichen Toll-like-Rezeptoren an der Zellmembran sitzen.[3]
TLR2 erkennt viele Komponenten von Bakterien, Mykoplasmen, Pilzen und Viren. Hierzu gehören auch die Lipoproteine der Bakterien und Mykoplasmen. Die Erkennung erfolgt indem TLR2 entweder mit TLR1 oder TLR6 eine Heterodimer bildet. Die entstehenden TLR1/TLR2- und TLR6/TLR2-Komplexe erkennen dabei Triacyl- bzw. Diacyllipoproteine. Die Aktivierung von TLR2 führt zur Ausschüttung einer Reihe von Zytokinen. Alpha-Interferon (IFN-α) wird dabei nur teilweise freigesetzt. Allgemein wird vermutet, dass die Ausschüttung von IFN-α vom Zelltyp abhängig ist. TLR10 ähnelt in seiner Primärstruktur (Sequenzübereinstimmung) TLR1 und TLR6, der Ligand ist jedoch noch nicht bekannt. TLR4 kann Lipopolysaccharid (LPS) auf der Zelloberfläche zusammen mit MD2 (myeloid differentiation factor 2) erkennen. LPS ist ein Stoff aus der äußeren Membran von gramnegativen Bakterien und wird in Tiermodellen zur eingeschränkten Simulation von akuten Infektionen verwendet. Bei der Detektion von LPS arbeiten zwei TLR-4-MD2-LPS-Komplexe zusammen und formen ein TLR-4-Homodimer.
TLR5 wird hauptsächlich in der Lamina propria exprimiert, wo es bakterielles Flagellin erkennt. Als Immunantwort darauf induziert TLR5 die Ausdifferenzierung von B-Zellen in lgA-produzierende Blutzellen und von T-Zellen in antigenspezifische Th17- und Th1-Zellen. TLR11 das nur in der Maus, aber nicht im Menschen vorkommt, zeigt große Ähnlichkeiten zu TLR5. Es erkennt ein Profilin-ähnliches Molekül, das vom intrazellulären Protozoon Toxoplasma gondii abstammt. Eine Reihe von TLRs, darunter TLR3, TLR7, TLR8 und TLR9 erkennen aus Viren oder Bakterien stammende Nukleinsäuren. Die Aktivierung dieser TLRs führt zur Bildung von Alpha-Interferon und anderen entzündungsauslösenden Zytokinen. TLR3 entdeckt virale doppelsträngige RNA im Endolysosom. Hierbei bindet die dsRNA an das N-terminale und das C-terminale Ende der LRR-Sequenz.
| Rezeptor | Liganden[4] | Ursprung der Liganden[4] | Adapterprotein des TLR | Zelluläre Lokalisation | Zelltypen[4] |
|---|---|---|---|---|---|
| TLR 1 | Verschiedene Triacyl-Lipopeptide | Bakterielles Lipoprotein | MyD88/MAL | Zelloberfläche |
|
| TLR 2 | Verschiedene Glycolipide | Bakterielle Peptidoglykane | MyD88/MAL | Zelloberfläche |
|
| Verschiedene Lipopeptide und Proteolipide | Bakterielle Peptidoglycane | ||||
| Lipoteichonsäure | Gram-positive Bakterien | ||||
| HSP70 | Wirtszellen | ||||
| Zymosan (Beta-Glucan) | Pilze | ||||
| Zahlreiche Andere | |||||
| TLR 3 | Doppelsträngige RNA, Poly I:C | Viren | TRIF | Zellkompartiment |
|
| TLR 4 | Lipopolysaccharid | Gram-negative Bakterien | MyD88/MAL/TRIF/TRAM | Zelloberfläche |
|
| Mehrere Hitzeschockproteine | Bakterien und Wirtszellen | ||||
| Fibrinogen | Wirtszellen | ||||
| Heparansulfatfragmente | Wirtszellen | ||||
| Hyaluronsäurefragmente | Wirtszellen | ||||
| Nickel[9] | |||||
| Verschiedene Opioide | |||||
| TLR 5 | Bakterielles Flagellin | Bakterien | MyD88 | Zelloberfläche |
|
| Profilin[10] | Toxoplasma gondii | ||||
| TLR 6 | Verschiedene Diacyl-Lipopeptide | Mycoplasma | MyD88/MAL | Zelloberfläche |
|
| TLR 7 | Imidazochinolin | Niedermolekulare synthetische Stoffe | MyD88 | Zellkompartiment |
|
| Loxoribin (ein Guanosinanalogon) | |||||
| Bropirimin | |||||
| Resiquimod | |||||
| Einzelsträngige RNA | RNA-Viren | ||||
| TLR 8 | Niedermolekulare synthetische Stoffe, einzelsträngige virale RNA, phagozytierte bakterielle RNA | MyD88 | Zellkompartiment |
| |
| TLR 9 | Unmethylierte CpG-Oligonukleotide (DNA) | Bakterien, DNA-Viren | MyD88 | Zellkompartiment |
|
| TLR 10 | Triacylierte Lipopeptide[11] | unbekannt | Zelloberfläche | ||
| TLR 11 | Profilin | Toxoplasma gondii[15] | MyD88 | Zellkompartiment[16] |
|
| TLR 12 | Profilin | Toxoplasma gondii[17] | MyD88 | Zellkompartiment | |
| TLR 13[19][20] | Bakterielle ribosomale RNA-Sequenz CGGAAAGACC (unmethyliert)[21] | Viren, Bakterien | MyD88, TAK-1 | Zellkompartiment |
|
Die intrazelluläre Signalkaskade
Die Chemoattraktorproteine „C3a“ und „C5a“ des Komplementsystems entstehen durch proteolytische Spaltung aus den inaktiven Vorstufen C3, bzw. C5. Aktiviert locken sie Makrophagen und neutrophile Granulozyten an. Diese Phagozyten haben auf ihrer Oberfläche Rezeptoren vom TLR-Typ. Die TLRs reagieren auf bakterielle Proteoglykane bzw. Lipopolysaccharide (LPS), DNA und RNA. Sie lösen in ihren Trägerzellen eine Signalkaskade aus, die schließlich zur Stimulation der Infektionsabwehr führt. Nach Erkennen dieser bakteriellen Oberflächenstrukturen auf extrazellulärer Seite, werden intrazellulär – durch TLR – Signalkaskaden ausgelöst.
Die Erkennung von PAMPs (Pathogen Associated Molecular Patterns) durch TLRs führt zu einer Erhöhung der Transkriptionsrate bestimmter Gene, je nachdem welche TLRs und welche Zelltypen beteiligt sind. Der Unterschied zwischen den von den einzelnen TLRs aktivierten Signalkaskaden kann zumindest teilweise durch die TIR-domain enthaltenden Adaptormoleküle (TIR domain-containing adaptor molecules) erklärt werden. Es gibt dabei fünf TIR domain-containing adaptor molecules, darunter MyD88, TRIF/TICAM-1 (TIR-domain-containing adaptor inducing IFN-β), TIRAP/Mal, TRAM (TRIF-related adaptor molecule), und SARM (Sterile-alpha and Armadillo motif-containing protein). TLR- Signalketten werden abhängig von der Beteiligung der Adaptormoleküle MyD88 und TRIF grob in zwei unterschiedliche Reaktionsketten unterteilt.
Dabei kommt es zur Phosphorylierung und somit Aktivierung intrazellulärer Kinasen, deren Aufgabe in der Phosphorylierung intrazellulärer Inhibitoren von Transkriptionsfaktoren besteht. Als Erstes bindet das Adapterprotein MyD88 an den zytoplasmatischen Abschnitt des TLR. Als Folge bindet nun die IL-1-Rezeptor-assoziierte Kinase (IRAK) an MyD88 und aktiviert sich durch Autophosphorylation selbst. Über weitere Einzelschritte kommt es schließlich zur Aktivierung des Transkriptionsfaktors NF-κB, der daraufhin in den Zellkern transloziert und dort die Expression von Genen für TNFα, IL-1, IL-12 und E-Selektin reguliert.
An TLRs bindende Medikamente
Das bei verschiedenen Hautkrankheiten verwendete Imiquimod und dessen potenzielle Nachfolgesubstanz Resiquimod (R 848) sind Liganden für TLR7 resp. TLR7 und TLR 8.[1] CpG-Oligonukleotide binden an TLR9.[22] Eritoran bindet an TLR4.[23][24] Poly I:C (Polyinosinsäure:Polycytidinsäure), ein Doppelstrang-RNA-Mimetikum, bindet an TLR3.[25]
Literatur
- K. Takeda, S. Akira: Toll-like receptors in innate immunity. In: International immunology, Band 17, Nummer 1, Januar 2005, ISSN 0953-8178, S. 1–14, doi:10.1093/intimm/dxh186, PMID 15585605 (Review).
- Luke A. J. O’Neill: Das immunologische Frühwarnsystem. Spektrum der Wissenschaft, August 2005, S. 68–75
- S. E. Turvey, T. R. Hawn: Towards subtlety: understanding the role of Toll-like receptor signaling in susceptibility to human infections. In: Clinical immunology (Orlando FL), Band 120, Nr. 1, Juli 2006, ISSN 1521-6616, S. 1–9, doi:10.1016/j.clim.2006.02.003, PMID 16563867 (Review).
- Nicola Siegmund-Schultze: Deutsches Ärzteblatt: Toll-like-Rezeptoren: Neue Zielstruktur für immunstimulierende Medikamente. In: Deutsches Ärzteblatt. Band 104, Nr. 16. Deutscher Ärzte-Verlag, 20. April 2007, S. A-1072 / B-954 / C-908.
Einzelnachweise
- ↑ a b c Peter Fritsch: Dermatologie und Venerologie. 2. Auflage. Springer Verlag, 2004, ISBN 3-540-00332-0
- ↑ B. Lemaitre, E. Nicolas, L. Michaut, J. M. Reichhart, J. A. Hoffmann: The dorsoventral regulatory gene cassette spätzle/Toll/cactus controls the potent antifungal response in Drosophila adults. In: Cell. Band 86, Nummer 6, September 1996, ISSN 0092-8674, S. 973–983, PMID 8808632.
- ↑ T. Kawai, S. Akira: The role of pattern-recognition receptors in innate immunity: update on Toll-like receptors. In: Nature Immunology. Band 11, Nummer 5, Mai 2010, S. 373–384, doi:10.1038/ni.1863, PMID 20404851 (Review).
- ↑ a b c Unless else specified in boxes then ref is: Waltenbaugh C, Doan T, Melvold R, Viselli S: Immunology (= Lippincott's Illustrated reviews). Wolters Kluwer Health/Lippincott Williams & Wilkins, Philadelphia 2008, ISBN 978-0-7817-9543-2, S. 17.
- ↑ a b Sabroe I, Dower SK, Whyte MK: The role of Toll-like receptors in the regulation of neutrophil migration, activation, and apoptosis. In: Clinical Infectious Diseases. 41 Suppl 7. Jahrgang, November 2005, S. S421–6, doi:10.1086/431992, PMID 16237641.
- ↑ a b c d Sallusto F, Lanzavecchia A: The instructive role of dendritic cells on T-cell responses. In: Arthritis Research. 4 Suppl 3. Jahrgang, 2002, S. S127–32, doi:10.1186/ar567, PMID 12110131, PMC 3240143 (freier Volltext).
- ↑ Gerondakis S, Grumont RJ, Banerjee A: Regulating B-cell activation and survival in response to TLR signals. In: Immunology and Cell Biology. 85. Jahrgang, Nr. 6, 2007, S. 471–5, doi:10.1038/sj.icb.7100097, PMID 17637697.
- ↑ Cario E, Rosenberg IM, Brandwein SL, Beck PL, Reinecker HC, Podolsky DK: Lipopolysaccharide activates distinct signaling pathways in intestinal epithelial cell lines expressing Toll-like receptors. In: Journal of Immunology. 164. Jahrgang, Nr. 2, Januar 2000, S. 966–72, doi:10.4049/jimmunol.164.2.966, PMID 10623846.
- ↑ Peana M, Zdyb K, Medici S, Pelucelli A, Simula G, Gumienna-Kontecka E, Zoroddu MA: Ni(II) interaction with a peptide model of the human TLR4 ectodomain. In: Journal of Trace Elements in Medicine and Biology. 44. Jahrgang, Dezember 2017, S. 151–160, doi:10.1016/j.jtemb.2017.07.006, PMID 28965571.
- ↑ Salazar Gonzalez RM, Shehata H, O'Connell MJ, Yang Y, Moreno-Fernandez ME, Chougnet CA, Aliberti J: Toxoplasma gondii- derived profilin triggers human toll-like receptor 5-dependent cytokine production. In: Journal of Innate Immunity. 6. Jahrgang, Nr. 5, 2014, S. 685–94, doi:10.1159/000362367, PMID 24861338, PMC 4141014 (freier Volltext).
- ↑ Guan Y, Ranoa DR, Jiang S, Mutha SK, Li X, Baudry J, Tapping RI: Human TLRs 10 and 1 share common mechanisms of innate immune sensing but not signaling. In: Journal of Immunology (Baltimore, Md. : 1950). 184. Jahrgang, Nr. 9, Mai 2010, S. 5094–103, doi:10.4049/jimmunol.0901888, PMID 20348427.
- ↑ Chuang T, Ulevitch RJ: Identification of hTLR10: a novel human Toll-like receptor preferentially expressed in immune cells. In: Biochimica Et Biophysica Acta. 1518. Jahrgang, Nr. 1-2, März 2001, S. 157–61, doi:10.1016/s0167-4781(00)00289-x, PMID 11267672.
- ↑ Hornung V, Rothenfusser S, Britsch S, Krug A, Jahrsdörfer B, Giese T, Endres S, Hartmann G: Quantitative expression of toll-like receptor 1-10 mRNA in cellular subsets of human peripheral blood mononuclear cells and sensitivity to CpG oligodeoxynucleotides. In: Journal of Immunology. 168. Jahrgang, Nr. 9. Baltimore, Md. : 1950 Mai 2002, S. 4531–7, doi:10.4049/jimmunol.168.9.4531, PMID 11970999.
- ↑ a b Regan T, Nally K, Carmody R, Houston A, Shanahan F, Macsharry J, Brint E: Identification of TLR10 as a key mediator of the inflammatory response to Listeria monocytogenes in intestinal epithelial cells and macrophages. In: Journal of Immunology. 191. Jahrgang, Nr. 12, Dezember 2013, S. 6084–92, doi:10.4049/jimmunol.1203245, PMID 24198280.
- ↑ Yarovinsky F, Zhang D, Andersen JF, Bannenberg GL, Serhan CN, Hayden MS, Hieny S, Sutterwala FS, Flavell RA, Ghosh S, Sher A: TLR11 activation of dendritic cells by a protozoan profilin-like protein. In: Science. 308. Jahrgang, Nr. 5728, Juni 2005, S. 1626–9, doi:10.1126/science.1109893, PMID 15860593, bibcode:2005Sci...308.1626Y.
- ↑ Pifer R, Benson A, Sturge CR, Yarovinsky F: UNC93B1 is essential for TLR11 activation and IL-12-dependent host resistance to Toxoplasma gondii. In: The Journal of Biological Chemistry. 286. Jahrgang, Nr. 5, Februar 2011, S. 3307–14, doi:10.1074/jbc.M110.171025, PMID 21097503, PMC 3030336 (freier Volltext).
- ↑ Koblansky AA, Jankovic D, Oh H, Hieny S, Sungnak W, Mathur R, Hayden MS, Akira S, Sher A, Ghosh S: Recognition of profilin by Toll-like receptor 12 is critical for host resistance to Toxoplasma gondii. In: Immunity. 38. Jahrgang, Nr. 1, Januar 2013, S. 119–30, doi:10.1016/j.immuni.2012.09.016, PMID 23246311, PMC 3601573 (freier Volltext).
- ↑ Mishra BB, Gundra UM, Teale JM: Expression and distribution of Toll-like receptors 11-13 in the brain during murine neurocysticercosis. In: Journal of Neuroinflammation. 5. Jahrgang, Dezember 2008, S. 53, doi:10.1186/1742-2094-5-53, PMID 19077284, PMC 2631477 (freier Volltext).
- ↑ Shi Z, Cai Z, Sanchez A, Zhang T, Wen S, Wang J, Yang J, Fu S, Zhang D: A novel Toll-like receptor that recognizes vesicular stomatitis virus. In: The Journal of Biological Chemistry. 286. Jahrgang, Nr. 6, Februar 2011, S. 4517–24, doi:10.1074/jbc.M110.159590, PMID 21131352, PMC 3039399 (freier Volltext).
- ↑ Oldenburg M, Krüger A, Ferstl R, Kaufmann A, Nees G, Sigmund A, Bathke B, Lauterbach H, Suter M, Dreher S, Koedel U, Akira S, Kawai T, Buer J, Wagner H, Bauer S, Hochrein H, Kirschning CJ: TLR13 recognizes bacterial 23S rRNA devoid of erythromycin resistance-forming modification. In: Science. 337. Jahrgang, Nr. 6098, August 2012, S. 1111–5, doi:10.1126/science.1220363, PMID 22821982, bibcode:2012Sci...337.1111O.
- ↑ Hochrein H, Kirschning CJ: Bacteria evade immune recognition via TLR13 and binding of their 23S rRNA by MLS antibiotics by the same mechanisms. In: Oncoimmunology. 2. Jahrgang, Nr. 3, März 2013, S. e23141, doi:10.4161/onci.23141, PMID 23802068, PMC 3661153 (freier Volltext).
- ↑ C. Maisonneuve, S. Bertholet u. a.: Unleashing the potential of NOD- and Toll-like agonists as vaccine adjuvants. In: Proceedings of the National Academy of Sciences. Band 111, Nummer 34, August 2014, ISSN 1091-6490, S. 12294–12299, doi:10.1073/pnas.1400478111, PMID 25136133, PMC 4151741 (freier Volltext) (Review).
- ↑ K. A. Shirey, W. Lai u. a.: The TLR4 antagonist Eritoran protects mice from lethal influenza infection. In: Nature. Band 497, Nummer 7450, Mai 2013, ISSN 1476-4687, S. 498–502, doi:10.1038/nature12118, PMID 23636320, PMC 3725830 (freier Volltext).
- ↑ E. J. Hennessy, A. E. Parker, L. A. O’Neill: Targeting Toll-like receptors: emerging therapeutics? In: Nature reviews. Drug discovery. Band 9, Nummer 4, April 2010, ISSN 1474-1784, S. 293–307, doi:10.1038/nrd3203, PMID 20380038 (Review).
- ↑ C. F. Nicodemus, J. S. Berek: TLR3 agonists as immunotherapeutic agents. In: Immunotherapy. Band 2, Nummer 2, März 2010, S. 137–140, doi:10.2217/imt.10.8, PMID 20635920 (Review).