Benutzer:Orci/Namensreaktionen/G
Zur Navigation springen
Zur Suche springen
| Entdecker | Jahr | Reagenzien | Kurzbeschreibung | Zielmolekül(e) | Quelle |
|---|---|---|---|---|---|
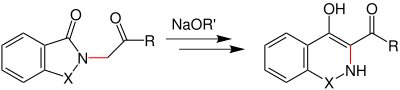
| Gabriel-Colman-Umlagerung | |||||
| Siegmund Gabriel, James Colman | 1900 | Maleimidylacetate, Base | Umlagerung | Isochinolin-1,4-diole | [1] |
| |||||
| Gabriel-Reaktion | |||||
| Siegmund Gabriel | 1888 | Halogenamine, Alkalihydroxide | Eliminierung von Alkalihalogenen | cyclische Amine | [2] |
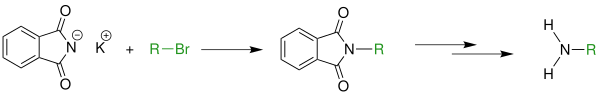
| Gabriel-Synthese | |||||
| Siegmund Gabriel | 1887 | Kaliumphthalimid, Halogenalkane | Nukleophile Substitution, Hydrolyse | primäre Amine | [3] |
| |||||
| Gallagher-Hollander-Abbau | |||||
| Garegg-Samuelsson-Reaktion | |||||
| Per J. Garegg, Bertil Samuelsson | 1979 | Alkohole, Iod, Triphenylphosphin, Imidazol | Aktivierung, SN2-Reaktion | Organoiodverbindungen | [4] |
| Garst-Spencer-Furananellierung | |||||
| Michael E. Garst, Thomas A. Spencer | 1973 | Methylenthioether von Cycloketonen, Trimethylsulfoniumverbindungen, Iod | Bildung eines Epoxids, Umlagerung, Desulfonierung | anellierte Furane | [5] |
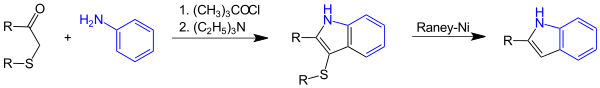
| Gassman-Indolsynthese | |||||
| Paul G. Gassman | 1974 | Anilin, org. Hypohalogenide, β-Carbonylsulfide, Base | Nukleophile Substitution, Sommelet-Hauser-Umlagerung, intramolekulare Addition, Eliminierung | 3-Thioalkoxyindole | [6] |
| |||||
| Gassman-Oxindol-Synthese | |||||
| Paul G. Gassman | 1973 | Aniline, tert-Butylhypochlorit, β-Methylthioester, Base, Raney-Nickel | Bildung des N-Chloranilins, nukleophile Substitution, sigmatrope Umlagerung | Oxindole | [7] |
| Gassman-Reaktion | |||||
| Paul G. Gassman | 1978 | Aniline, tert-Butylhypochlorit, Thioether, Base, Raney-Nickel | Bildung des N-Chloranilins, nukleophile Substitution, intramolekulare Reaktion zum Imin, Eliminierung, Entschwefelung | ortho-substituierte Aniline | [8] |

| |||||
| Gattermann-Synthese | |||||
| Ludwig Gattermann | 1898 | Aromaten, Blausäure, Chlorwasserstoff, Aluminium- oder Zinkchlorid | elektrophile aromatische Substitution | aromatische Aldehyde | [9] |
| Gattermann-Koch-Synthese | |||||
| Ludwig Gattermann, Julius Arnold Koch | 1897 | Aromaten, Kohlenstoffmonoxid, Chlorwasserstoff, Aluminium- oder Kupfer(I)-chlorid | elektrophile aromatische Substitution | aromatische Aldehyde | [10] |
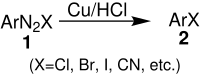
| Gattermann-Reaktion | |||||
| Ludwig Gattermann | 1890 | aromatische Diazoniumsalze, Kupfer, Salzsäure | Abspaltung von Stickstoff, radikalische Reaktion auf Oberfläche | Halogenaromaten | [11] |
| |||||
| Gewald-Reaktion | |||||
| Karl Gewald | 1966 | Ketone/Aldehyde, α-Cyanoester, Schwefel, Base | Knoevenagel-Reaktion, Ringschluss | 2-Amino-thiophene | [12] |

| |||||
| Ghosez-Keteniminium-Olefin-Cyclisierung | |||||
| Léon Ghosez | 1974 | Ketenimine, Alkene | [2+2]-Cycloaddition | Cyclobutanone | [13] |
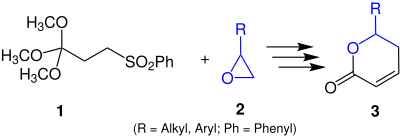
| Ghosez-Cyclisierung | |||||
| Léon Ghosez | 1988 | Phenylsulfonyl-Orthobuttersäuretrimethylester, Epoxide, Buthyllithium, Diazabicycloundecen | Deprotonierung, nucleophiler Angriff, Cyclisierung, Abspaltung von Methano, Deprotonierung, Abspaltung der Phenylsulfonylgruppe | δ-Lactone | [14] |
| |||||
| Gibbs-Wohl-Naphthalinoxidation | |||||
| Harry Gibbs, Alfred Wohl | 1916/17 | Naphthalin, Vandium(V)-oxid, Sauerstoff | Oxidation des Naphthalins, Rückgewinnung des Vandadium(V)-oxides | Phthalsäureanhydrid | [15][16] |

| |||||
| Gilman-Cason-Ketonsynthese | |||||
| Gilman-Speeter-Reaktion | |||||
| Henry Gilman, Merrill E. Speeter | 1943 | α-halogenierte Carbonsäureester, Zink, Imine | Bildung eines Reformatzki-Reagenzes, Cyclisierung | β-Lactame | [17] |

| |||||
| Gilman-van-Ess-Synthese | |||||
| Henry Gilman, Paul R. van Ess | 1933 | Carbonsäuren, Lithiumalkylverbindungen, Säure | Deprotonierung, nucleophiler Angriff, Hydrolyse | Ketone | [18] |

| |||||
| Glaser-Kupplung | |||||
| C. Glaser | 1869 | terminale Alkine, Kupfer(I)-chlorid, Sauerstoff | Kupplungsreaktion | 1,3-Diine | [19] |

| |||||
| Gomberg-Bachmann-Reaktion | |||||
| Moses Gomberg, Werner Bachmann | 1924 | Aryldiazoniumsalze, Aromat, Base | radikalische Kupplung | Biaryle | [20] |

| |||||
| Gomberg-Bachmann-Pinacol-Synthese | |||||
| Gomberg-Radikalreaktion | |||||
| Moses Gomberg | 1900 | Triphenylchlormethan, Zink/Silber | Ein-Elektron-Übertragung mit Chloridabspaltung | Triphenylmethan-Radikal | [21] |

| |||||
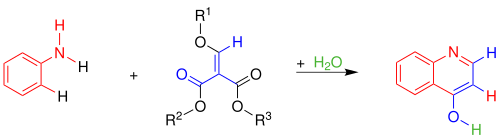
| Gould-Jacobs-Reaktion | |||||
| R. Gordon Gould, Walter A. Jacobs | 1939 | Aniline, Arylmalonsäureester | Kondensation, Cyclisierung | 4-Hydroxychinoline | [22] |
| |||||
| Graebe-Ullmann-Synthese | |||||
| Carl Graebe, Fritz Ullmann | 1896 | ortho-Aminodiphenylamine, salpetrige Säure | Disazotierung, Cyclsierung zum Triazol, N2-Abspaltung, radikalische Umlagerung, Cyclisierung | Carbazole | [23] |

| |||||
| Gränacher-Synthese | |||||
| Gribble-Aminierung | |||||
| Gordon W. Gribble | 1974 | Indole, Natriumborhydrid/Natriumcyanoborhydrid, Essigsäure | Reduktion | Indoline | [24] |
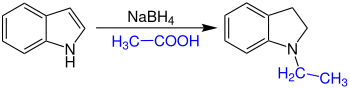
| |||||
| Griess-Diazoreaktion | |||||
| Peter Griess | 1879 | Aniline, Distickstofftrioxid, Salpetersäure | Diazotierung | Diazoniumsalze | [25] |
| Grignard-Abbau | |||||
| Wilhelm Steinkopf (so benannt wegen des Reagenzes) | 1934 | polyhalogenierte Verbindungen, Magnesium | Bildung des Grignard-Reagenzes, Hydrolyse | Abspaltung eines Halogen-Atoms | [26] |

| |||||
| Grignard-Reaktion | |||||
| Victor Grignard | 1900 | Carbonyl-Verbindungen, Grignard-Verbindungen | Nukleophile Addition an der Carbonyl-Gruppe, Hydrolyse | Aufbau von C-C-Einfachbindungen | [27] |
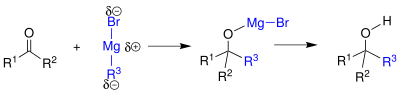
| |||||
| Grignard-Reduktion | |||||
| Victor Grignard | sterisch gehinderte Grignard-Verbindungen, Ketone | cyclische Reaktion unter Alken-Bildung (Nebenreaktion der Grignard-Reaktion) | Alkohole | ||

| |||||
| Grob-Fragmentierung | |||||
| Cyril A. Grob | 1955 | längere aliphatische Ketten | Fragmentierung in mehrere Teile | Kation, Alken, Anion | [28] |
| Grosheintz-Fischer-Reissert-Aldehydsynthese | |||||
| Jean M. Grosheintz, Hermann O. L. Fischer, Arnold Reissert | 1941 | Carbonsäurechloride, Cyanwasserstoff, Chinolin, Benzol (Lösungsmittel) | Reissert-Reaktion, saure Hydrolyse | Aldehyde | [29] |

| |||||
| Grundmann-Aldehydsynthese | |||||
| Christoph Grundmann | 1931 | Carbonsäurechloride, Diazomethan, Essigsäure, Aluminiumtriisopropylat, Blei(IV)-acetat | Diazotierung, Veresterung, Reduktion zum Glycol, Spaltung | Aldehyde | [30] |
| Gryszkiewicz-Trochimowski- und Mccombie-Fluorierung | |||||
| Guareschi-Thorpe-Kondensation (Guareschi-Reaktion) | |||||
| Icilio Guareschi, Jocelyn Field Thorpe | 1896, 1904 | Acetessigsäureester, Cyanoessigsäureester | Kondensation | Pyridin-Derivate | [31][32] |

| |||||
| Guerbet-Reaktion | |||||
| Marcel Guerbet | 1899 | Alkohole, Alkoxide | Aldolkondensation, Cannizzaro-Reaktion | längerkettige Alkohole | [33] |
| Gustavson-Reaktion (Freund-Gustavson-Reaktion) | |||||
| Gawriil Gawriilowitsch Gustawson | 1887 | 1,3-Dihalogenpropan, Zink | Freund-Reaktion | Cyclopropan | [34] |

| |||||
| Gutknecht-Pyrazinsynthese | |||||
| H. Gutknecht | 1879 | α-Aminoketone, Sauerstoff | Kondensation, Dehydrogenierung | Pyrazine | [35] |

| |||||
Quellen[Bearbeiten | Quelltext bearbeiten]
- ↑ S. Gabriel, J. Colman: Ueber die Einwirkung von Natriumalkylaten auf Phtalylglycinester und dessen Homologe. In: Berichte der deutschen chemischen Gesellschaft. 33, 1900, S. 980–995, doi:10.1002/cber.190003301172.
- ↑ S. Gabriel: Ueber Vinylamin. In: Berichte der deutschen chemischen Gesellschaft. 21, 1888, S. 1049, doi:10.1002/cber.188802101196.
- ↑ S. Gabriel: Ueber eine Darstellungsweise primaerer Amine aus den entsprechenden Halogenverbindungen. In: Berichte der deutschen chemischen Gesellschaft. 20, 1887, S. 2224–2236, doi:10.1002/cber.18870200227.
- ↑ Per J. Garegg, Bertil Samuelsson: Novel reagent system for converting a hydroxy-group into an iodo-group in carbohydrates with inversion of configuration. In: Journal of the Chemical Society, Chemical Communications. 1979, S. 978, doi:10.1039/C39790000978.
- ↑ Michael E. Garst, Thomas A. Spencer: General method for the synthesis of 3- and 3,4-substituted furans. Simple syntheses of perillene and dendrolasin. In: Journal of the American Chemical Society. 95, 1973, S. 250, doi:10.1021/ja00782a051.
- ↑ Paul G. Gassman, T. J. Van Bergen, David P. Gilbert, Berkeley W. Cue: General method for the synthesis of indoles. In: Journal of the American Chemical Society. 96, 1974, S. 5495–5508, doi:10.1021/ja00824a028.
- ↑ Paul G. Gassman, T. J. Van Bergen, Gordon Gruetzmacher: Use of halogen-sulfide complexes in the synthesis of indoles, oxindoles, and alkylated aromatic amines. In: Journal of the American Chemical Society. 95, 1973, S. 6508, doi:10.1021/ja00800a088.
- ↑ Paul G. Gassman, H. Roger Drewes: The ortho functionalization of aromatic amines. Benzylation, formylation, and vinylation of anilines. In: Journal of the American Chemical Society. 100, 1978, S. 7600, doi:10.1021/ja00492a028.
- ↑ L. Gattermann, W. Berchelmann: Synthese aromatischer Oxyaldehyde. In: Berichte der deutschen chemischen Gesellschaft. 31, 1898, S. 1765, doi:10.1002/cber.18980310281.
- ↑ L. Gattermann, J. A. Koch: Eine Synthese aromatischer Aldehyde. In: Berichte der deutschen chemischen Gesellschaft. 30, 1897, S. 1622, doi:10.1002/cber.18970300288.
- ↑ Ludwig Gattermann: Untersuchungen über Diazoverbindungen. In: Berichte der deutschen chemischen Gesellschaft. 23, 1890, S. 1218, doi:10.1002/cber.189002301199.
- ↑ Karl Gewald, Elfriede Schinke, Horst Böttcher: Heterocyclen aus CH-aciden Nitrilen, VIII. 2-Amino-thiophene aus methylenaktiven Nitrilen, Carbonylverbindungen und Schwefel. In: Chemische Berichte. 99, 1966, S. 94, doi:10.1002/cber.19660990116.
- ↑ Abdul Sidani, Jacqueline Marchand-Brynaert, Léon Ghosez: A Convenient Procedure for the Synthesis of Cyclobutanones. In: Angewandte Chemie International Edition in English. 13, 1974, S. 267, doi:10.1002/anie.197402671.
- ↑ Juan Carlos Carretero, Léon Ghosez: A practical route towards α,β-unsaturated δ-lactones based on a [3+3] strategy. Synthesis of (−)-argentilactone. In: Tetrahedron Letters. 29, 1988, S. 2059, doi:10.1016/S0040-4039(00)87834-X.
- ↑ Patent DE379822: Verfahren zur Herstellung von Phthalsaeureanhydrid. Angemeldet am 29. Juni 1916, Erfinder: Alfred Wohl.
- ↑ Patent US1285117: PROCESS FOR THE MANUFACTURE OF PHTHALIC ANHYDRID, PHTHALIC ACID, BENZOIC ACID, AND NAPHTHAQUINONES.. Angemeldet am 17. Februar 1917, Erfinder: Harry Gibbs, Courtney Conover.
- ↑ Henry Gilman, Merrill Speeter: The Reformatsky Reaction with Benzalaniline. In: Journal of the American Chemical Society. 65, 1943, S. 2255, doi:10.1021/ja01251a503.
- ↑ Henry Gilman, Paul R. van Ess: The Preparation of Ketones by the Carbonation of Organolithium Compounds. In: Journal of the American Chemical Society. 55, 1933, S. 1258, doi:10.1021/ja01330a070.
- ↑ C. Glaser: Beitraege zur Kenntniss des Acetenylbenzols. In: Berichte der deutschen chemischen Gesellschaft. 2, 1869, S. 422–424, doi:10.1002/cber.186900201183.
- ↑ M. Gomberg, W. E. Bachmann: The synthesis of biaryl compounds by means of the diazo reaction. In: Journal of the American Chemical Society. 46, 1924, S. 2339–2343, doi:10.1021/ja01675a026.
- ↑ M. Gomberg: Triphenylmethyl, ein Fall von dreiwerthigem Kohlenstoff. In: Berichte der deutschen chemischen Gesellschaft. 33, 1900, S. 3150, doi:10.1002/cber.19000330369.
- ↑ R. Gordon Gould, Walter A. Jacobs: The Synthesis of Certain Substituted Quinolines and 5,6-Benzoquinolines. In: Journal of the American Chemical Society. 61, 1939, S. 2890–2895, doi:10.1021/ja01265a088.
- ↑ C. Graebe, F. Ullmann: Ueber eine neue Carbazolsynthese. In: Justus Liebig's Annalen der Chemie. 291, 1896, S. 16–17, doi:10.1002/jlac.18962910104.
- ↑ Gordon W. Gribble, Pierre D. Lord, Jerauld Skotnicki, Stephen E. Dietz, Jefferson T. Eaton, Jerry Johnson: Reactions of sodium borohydride in acidic media. I. Reduction of indoles and alkylation of aromatic amines with carboxylic acids. In: Journal of the American Chemical Society. 96, 1974, S. 7812, doi:10.1021/ja00832a035.
- ↑ Peter Griess: Bemerkungen zu der Abhandlung der HH. Weselsky und Benedikt "Ueber einige Azoverbindungen". In: Berichte der deutschen chemischen Gesellschaft. 12, 1879, S. 426–428, doi:10.1002/cber.187901201117.
- ↑ Wilhelm Steinkopf, Hans Jacob, Herbert Penz: Studien in der Thiophenreihe. XXVI. Isomere Bromthiophene und die Konstitution der Thiophendisulfonsäuren. In: Justus Liebig's Annalen der Chemie. 512, 1934, S. 136–164, doi:10.1002/jlac.19345120113.
- ↑ V. Grignard: Sur quelques nouvelles combinaisons organométalliques du magnèsium et leur application à des synthèses d'alcools et d'hydrocarbures. In: CR Hebd. Séances Acad. Sci., Ser. C. 130, 1900, S. 1322–1324 (Digitalisat auf Gallica).
- ↑ C. A. Grob, W. Baumann: Die 1,4-Eliminierung unter Fragmentierung. In: Helvetica Chimica Acta. 38, 1955, S. 594–610, doi:10.1002/hlca.19550380306.
- ↑ J. M. Grosheintz, Hermann O. L. Fischer: Preparation of 1-Acyl-1,2-dihydroquinaldonitriles and their Hydrolysis to Aldehydes . In: Journal of the American Chemical Society. 63, 1941, S. 2021, doi:10.1021/ja01852a066.
- ↑ Christoph Grundmann: Ein neues Verfahren zur Überführung von Carbonsäuren in Aldehyde. In: Justus Liebig's Annalen der Chemie. 524, 1936, S. 31–48, doi:10.1002/jlac.19365240105.
- ↑ Icilio Guareschi: In: Mem. Reale Accad. Sci. Torino II. 46, 7, 11, 25 (1896)
- ↑ Harold Baron, Frederick George Percy Remfry, Jocelyn Field Thorpe: The formation and reactions of imino-compounds. Part I. Condensation of ethyl cyanoacetate with its sodium derivative. In: Journal of the Chemical Society, Transactions. 85, 1904, S. 1726, doi:10.1039/CT9048501726.
- ↑ M. Guerbet: Action de l'alcool amylique de fermentation sur son dérivé sodé. In: Comptes rendus de l’Académie des sciences. 128, 1899, S. 511–513 (Digitalisat auf Gallica)
- ↑ G. Gustavson: Ueber eine neue Darstellungsmethode des Trimethylens. In: Journal für Praktische Chemie. 36, 1887, S. 300, doi:10.1002/prac.18870360127.
- ↑ H. Gutknecht: Ueber Nitrosoäthylmethylketon. In: Berichte der deutschen chemischen Gesellschaft. 12, 1879, S. 2290, doi:10.1002/cber.187901202284.