Anthracen
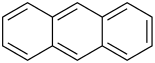
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Anthracen | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C14H10 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 178,24 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,25 g·cm−3[3] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
340 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: persistent, bioakkumulativ und toxisch (PBT)[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||

Anthracen [] (von griech. anthrax, ‚Kohle‘), auch Paranaphthalin oder veraltet Anthrazen ist ein farbloser kristalliner Feststoff, der leicht sublimiert. Es ist ein polycyclischer aromatischer Kohlenwasserstoff und organischer Halbleiter mit der Summenformel C14H10, der nach dem Bauprinzip der Acene aus drei anellierten Benzolringen aufgebaut ist.

Geschichte[Bearbeiten | Quelltext bearbeiten]
Anthracen wurde 1832 zum ersten Mal von Auguste Laurent und Jean-Baptiste Dumas aus dem Teer isoliert. Laurent stellte auch 1836 durch Oxidation des Anthracens Anthrachinon und Phthalsäure zum ersten Mal her.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Auf der Erde findet sich Anthracen in Steinkohlenteer. Oxidierte Anthracenderivate – meist Anthrachinone – kommen häufig in Organismen vor. Positiv geladene Anthracenmoleküle wurden sowohl in Meteoriten wie auch kürzlich von der Royal Astronomical Society in interstellarer Materie nachgewiesen.[6] Das komplexeste Molekül, das vor dem Anthracen im interstellaren Raum entdeckt wurde, war Naphthalin.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Anthracen wird industriell aus Steinkohlenteer gewonnen. Die synthetische Herstellung erfolgt durch Pyrolyse von 2-Methylbenzophenon[7] oder durch Friedel-Crafts-Alkylierung von 2-Brombenzylbromid. Alternativ kann es auch durch Reduktion von Anthrachinon hergestellt werden, welches wiederum durch Diels-Alder-Reaktion von p-Benzochinon mit 1,3-Butadien oder durch Friedel-Crafts-Acylierung von Benzol mit Phthalsäureanhydrid in Gegenwart von Aluminiumchlorid zugänglich ist. Letztere war die ursprüngliche Synthese, die 1883 von Richard Anschütz erfunden wurde. Die am häufigsten verwendeten Reduktionsmittel für Anthrachinon sind:
- Zink im alkalischen Milieu,
- amalgamiertes Aluminium in sekundären Alkoholen,
- Zinn(II)-chlorid und HCl in Essigsäure
- Natriumborhydrid
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Anthracen kristallisiert in farblosen bis gelblichen Blättchen, die violett fluoreszieren[2] und leicht sublimieren. Sie schmelzen bei 216,3 °C und sieden bei 340 °C. Anthracen ist in Wasser nahezu unlöslich (etwa 0,1 mg/l bei 25 °C), wenig löslich in Ethanol (15 g/l) und Diethylether, und gut löslich in siedendem Benzol. Anthracen riecht nur sehr schwach aromatisch und ist nahezu geruchlos. Da im Anthracen nur ein Sechsring ein -Elektronensextett enthält, ist es ziemlich reaktiv, reaktiver als das Isomer Phenanthren, das im Gegensatz zum Anthracen zwei Ringe mit einem -Elektronensextett aufweist. Vor allem die Positionen 9 und 10 stellen hier ideale Angriffspunkte z. B. für Oxidationen dar, durch welche Anthracen beispielsweise in Anthrachinon umgewandelt werden kann.
Anthracen dimerisiert durch UV-Licht-Einfluss in einer photochemisch erlaubten [4πs+ 4πs]-Cycloaddition; das Dimer zerfällt bei Wärmeeinwirkung unter Rückbildung von Anthracen.[8]
Da es bei Anthracen nach dem Inkrementsystem zwei unterschiedliche mesomere Grenzstrukturen gibt, sind diese bei der Berechnung der Mesomerieenergie zu beachten und der Mittelwert der Bildungsenthalpien zu bilden, bevor man die Differenz zur tatsächlichen Bildungsenthalpie zieht.
Der Flammpunkt liegt bei 121 °C, die Zündtemperatur bei 540 °C.[9] Die untere Explosionsgrenze (UEG) beträgt in Luft 0,6 Vol.-% (45 g/m3).[9] Anthracen ist wassergefährdend (WGK 2).[1] Die Standardbildungsenthalpie beträgt in der Festphase 121 ± 10 kJ·mol−1[10], in der Gasphase 223 ± 10 kJ·mol−1[11]. Die Standardverbrennungsenthalpie in der Festphase liegt bei −7061 ± 10 kJ·mol−1[10].
Verwendung[Bearbeiten | Quelltext bearbeiten]
Anthracen wird fast ausschließlich zu Anthrachinon weiterverarbeitet,[12] welches den Ausgangspunkt für die Anthrachinonfarbstoffe darstellt und somit die Grundlage für die Alizarin- und Indanthrenfarbstoffe ist. Eine weitere Verwendung findet das Anthracen als Basisstoff für die Herstellung von Schädlingsbekämpfungsmitteln und Gerbstoffen. Der Anthracen-Abkömmling Dithranol ist der älteste Wirkstoff, der für die Behandlung von Schuppenflechte entwickelt wurde.[13]
Regulierung[Bearbeiten | Quelltext bearbeiten]
Anthracen ist als „prioritärer gefährlicher Stoff“ in Anhang X der europäischen Richtlinie 2000/60/EG (Wasserrahmenrichtlinie) aufgeführt.[14]
Über den Safe Drinking Water and Toxic Enforcement Act of 1986 besteht in Kalifornien seit 11. August 2023 eine Kennzeichnungspflicht für Produkte, die Anthracen enthalten.[15]
Nomenklatur[Bearbeiten | Quelltext bearbeiten]
Nach der IUPAC-Nomenklatur gibt es für Anthracen, wie auch für das isomere Phenanthren, einen speziellen Lokantensatz, der von der systematischen Bezifferung abweicht.[16] Dieser Lokantensatz wird teilweise auch auf heterocyclische Verbindungen mit derselben Grundstruktur (bei denen lediglich Kohlenstoffatome durch andere Atome ersetzt sind) übertragen. Ein Beispiel ist 4-Azaphenothiazin (Pyridobenzothiazin, Pyrido[3,2-b]benzothiazin) und Derivate davon wie Prothipendyl. Dort fällt dann die übliche dominante Rolle der Hetero-Atome bei der Nummerierung weg.
-
Lokanten von Anthracen gemäß IUPAC
-
Lokanten von Tricyclo[8.4.0.03,8]tetradeca-1,3,5,7,9,11,13-heptaen
gemäß der Von-Baeyer-Nomenklatur
Nach der Von-Baeyer-Nomenklatur für polycyclische Verbindungen, die allerdings für aromatische Verbindungen nicht empfohlen wird,[17] wird Anthracen als Tricyclo[8.4.0.03,8]tetradeca-1,3,5,7,9,11,13-heptaen bezeichnet.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f Eintrag zu Anthracen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ a b c d e Eintrag zu Anthracen. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2014.
- ↑ Wolfgang Gerhartz (Hrsg.): Ullmann's Encyclopedia of Industrial Chemistry. Vol. A./ 2., 5. Aufl., VCH, Weinheim 1985, ISBN 3-527-20102-5.
- ↑ Datenblatt Anthracen zur Synthese bei Merck, abgerufen am 31. Mai 2013.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 14. Juli 2014.
- ↑ Scinexx: Komplexer Kohlenwasserstoff im All entdeckt. Meldung vom 23. Juni 2010.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 2-Methylbenzophenon: CAS-Nummer: 131-58-8, EG-Nummer: 205-032-0, ECHA-InfoCard: 100.004.576, PubChem: 67230, ChemSpider: 60565, Wikidata: Q27283162.
- ↑ Gary W. Breton, Xoua Vang: Photodimerization of Anthracene: A [4πs+ 4πs] Photochemical Cycloaddition. In: Journal of Chemical Education. Band 75, Nr. 1, 1998, S. 81, doi:10.1021/ed075p81.
- ↑ a b E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- ↑ a b Eintrag zu Anthracene (Condensed phase thermochemistry data). In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD, abgerufen am 17. November 2019.
- ↑ Eintrag zu Anthracene (Gas phase thermochemical data). In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD, abgerufen am 17. November 2019.
- ↑ Bertram Philipp, Peter Stevens: Grundzüge der Industriellen Chemie. VCH Verlagsgesellschaft mbH, 1987, ISBN 3-527-25991-0, S. 183.
- ↑ Ulrich Mrowietz und Gerhard Schmid-Ott: Schuppenflechte - Was Sie schon immer über Psoriasis wissen wollten. 3. aktualisierte Auflage, Karger Verlag, 2012, ISBN 978-3-8055-9396-0, S. 24.
- ↑ Richtlinie 2000/60/EG des Europäischen Parlaments und des Rates vom 23. Oktober 2000 zur Schaffung eines Ordnungsrahmens für Maßnahmen der Gemeinschaft im Bereich der Wasserpolitik in der konsolidierten Fassung vom 20. November 2014, abgerufen am 28. Februar 2024. Anhang X.
- ↑ Anthracene. OEHHA, 11. August 2023, abgerufen am 21. August 2023 (englisch).
- ↑ IUPAC Nomenclature of Organic Chemistry: Rule A-22.5 (siehe Beispiele).
- ↑ Dieter Hellwinkel: Die systematische Nomenklatur der Organischen Chemie: Eine Gebrauchsanweisung. 4. Auflage. Springer-Verlag, Berlin, Heidelberg 1998, ISBN 978-3-540-63221-4, S. 31 (eingeschränkte Vorschau in der Google-Buchsuche).






![Lokanten von Tricyclo[8.4.0.03,8]tetradeca-1,3,5,7,9,11,13-heptaen gemäß der Von-Baeyer-Nomenklatur](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f8/Anthracene-numbering_%28Von_Baeyer_nomenclature%29.svg/240px-Anthracene-numbering_%28Von_Baeyer_nomenclature%29.svg.png)