Asparagin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Strukturformel des natürlich vorkommenden L-Asparagins | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Asparagin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C4H8N2O3 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 132,12 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| pKS-Wert | |||||||||||||||||||
| Löslichkeit |
schlecht in Wasser (22 g·l−1 bei 20 °C, Monohydrat, L-Asparagin)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Asparagin, abgekürzt Asn oder N, ist in der natürlichen L-Form eine der proteinogenen α-Aminosäuren.
Asparagin ist ein Derivat der Aminosäure Asparaginsäure, das statt deren γ-Carboxygruppe eine Amidgruppe trägt. Daher enthält die Seitenkette – im Unterschied zu Asparaginsäure – keine saure Gruppe, doch ist sie polar.
Der Einbuchstabencode N für Asparagin wurde willkürlich zugeordnet,[4] wobei als Merkhilfe asparagiNe vorgeschlagen wurde.[5]
Stereoisomerie[Bearbeiten | Quelltext bearbeiten]
In biosynthetischen Proteinen kommt ausschließlich L-Asparagin [Synonym: (S)-Asparagin] neben anderen Aminosäuren peptidisch gebunden vor. Enantiomer dazu ist das spiegelbildliche D-Asparagin [Synonym: (R)-Asparagin], das in Proteinen nicht vorkommt. Racemisches DL-Asparagin [Synonym: (RS)-Asparagin] besitzt geringe Bedeutung.
Wenn „Asparagin“ in der Literatur ohne weiteren Namenszusatz (Deskriptor) erwähnt wird, ist gemeinhin L-Asparagin gemeint.
| Isomere von Asparagin | ||
| Name | L-Asparagin | D-Asparagin |
| Andere Namen | (S)-Asparagin | (R)-Asparagin |
| Strukturformel |  |
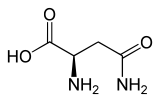
|
| CAS-Nummer | 70-47-3 | 2058-58-4 |
| 3130-87-8 (DL) | ||
| EG-Nummer | 200-735-9 | 218-163-3 |
| 221-521-1 (DL) | ||
| ECHA-Infocard | 100.000.669 | 100.016.513 |
| 100.019.565 (DL) | ||
| PubChem | 6267 | 439600 |
| 236 (DL) | ||
| DrugBank | DB00174 | - |
| - (DL) | ||
| Wikidata | Q29519883 | Q27094804 |
| Q185906 (DL) | ||
Geschichte[Bearbeiten | Quelltext bearbeiten]

L-Asparagin ist diejenige proteinogene Aminosäure, die zuerst entdeckt wurde.[6] Der in Paris tätige Professor für Chemie und Pharmazie Louis-Nicolas Vauquelin beobachtete 1805 in einem von seinem Schüler Pierre-Jean Robiquet nach dem Eindampfen von Spargelsaft stehen gelassenem Rückstand die Ausscheidung zweier Kristalle.[7]
Neben einer zuckerartigen Substanz konnten die beiden Franzosen eine salzartige Substanz isolieren, der sie den Namen Asparagin gaben, abgeleitet vom lateinischen Namen Asparagus für den Spargel. Ihre genaueren Ergebnisse veröffentlichten Vauquelin und Robiquet im darauffolgenden Jahr 1806.[8]
Nach der Isolierung und Feststellung der Zusammensetzung vergingen jedoch weitere 57 Jahre bis zur finalen Strukturaufklärung. Erst 1862 gelang es Hermann Kolbe, die beiden Strukturformeln von Asparagin und Asparaginsäure eindeutig zu beschreiben.[9]
Vorkommen[Bearbeiten | Quelltext bearbeiten]
L-Asparagin ist Bestandteil zahlreicher Peptide (z. B. Insulin und Proteine). Größere natürliche Vorkommen finden sich im Spargel (Asparagus officinalis) und in den Keimlingen von Schmetterlingsblütlern und Kartoffeln.[10]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Bereits seit Ende des 19. Jahrhunderts ist bekannt, dass nur eines der beiden Stereoisomere (D-Asparagin) süß schmeckt, und dies war für Louis Pasteur der Grund, auf „die chemische Asymmetrie der Nervensubstanz“ zu schließen. L-Asparagin schmeckt hingegen bitter.[11][12][13][14][15]

Asparagin liegt überwiegend als „inneres Salz“ bzw. Zwitterion vor, wobei das Proton der Carboxygruppe sich an das einsame Elektronenpaar des Stickstoffatoms der Aminogruppe anlagert:
Im elektrischen Feld wandert das Zwitterion nicht, da es als Ganzes ungeladen ist. Genau genommen ist dies am isoelektrischen Punkt (IEP) der Fall, der bei Asparagin bei einem pH von 5,41 liegt. Bei diesem pH-Wert hat das Asparagin auch seine geringste Löslichkeit in Wasser.

Reaktionen[Bearbeiten | Quelltext bearbeiten]
Wenn in einem Lebensmittel gleichzeitig Asparagin und reduzierende Zucker (z. B. Traubenzucker) vorliegen (vor allem bei Kartoffeln und Getreide), kann bei höheren Temperaturen und geringem Wassergehalt Acrylamid entstehen, das wegen seiner möglicherweise krebserzeugenden Wirkung in die Schlagzeilen geraten ist.
Biochemie[Bearbeiten | Quelltext bearbeiten]
L-Asparaginsäure reagiert mithilfe der Asparaginsynthetase und Anlagerung eines Ammoniumions von Glutamin zu L-Asparagin. Adenosintriphosphat wird in dieser Reaktion als Energielieferant benötigt und reagiert dabei zu Adenosinmonophosphat und Pyrophosphat (PPi). Durch Hydrolyse von L-Asparagin entsteht wiederum L-Asparaginsäure.
Verwendung[Bearbeiten | Quelltext bearbeiten]
Asparagin ist Bestandteil von Infusionslösungen zur parenteralen Ernährung.[16]
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b Datenblatt L-(+)-Asparagine, 99% bei Alfa Aesar, abgerufen am 21. Dezember 2019 (Seite nicht mehr abrufbar).
- ↑ a b c Eintrag zu Asparagin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 17. November 2022. (JavaScript erforderlich)
- ↑ a b c d Eintrag zu L-Asparagin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Mai 2014.
- ↑ IUPAC-IUB Commission on Biochemical Nomenclature A One-Letter Notation for Amino Acid Sequences. In: Journal of Biological Chemistry. 243. Jahrgang, Nr. 13, 10. Juli 1968, S. 3557–3559, doi:10.1016/S0021-9258(19)34176-6 (englisch, jbc.org [PDF]).
- ↑ Godwin I Adoga, Bh Nicholson: Letters to the editor. In: Biochemical Education. 16. Jahrgang, Nr. 1, Januar 1988, S. 49, doi:10.1016/0307-4412(88)90026-X (englisch, wiley.com [PDF]).
- ↑ S. Hansen: Die Entdeckung der proteinogenen Aminosäuren von 1805 in Paris bis 1935 in Illinois. ( vom 15. Juni 2016 im Internet Archive) Berlin 2015.
- ↑ P. J. Robiquet: Essai Analytique des Asperges. In: Ann. Chim., Bd. 55 (1), 1805, S. 152–171 (Digitalisat).
- ↑ L.-N. Vauquelin, P.-J. Robiquet: Découverte d’un Nouvelle Principe Végétal dans le Suc des Asperges. In: Annales de Chimie. Band 57, 1806, S. 88–93 (Digitalisat)
- ↑ H. Kolbe: Ueber die chemische Constitution des Asparagins und der Asparaginsäure, Liebigs Annalen der Chemie, Band 121, S. 232ff (1862).
- ↑ Otto-Albrecht Neumüller (Herausgeber): Römpps Chemie Lexikon, 8. Auflage, Frank’sche Verlagshandlung, Stuttgart 1983, ISBN 3-440-04513-7, S. 293–294.
- ↑ Piutti, MA: Sur une nouvelle espèce d'asparagine. In: Comptes rendus. 103. Jahrgang, 1886, S. 134–137 (französisch, bnf.fr).
- ↑ Pasteur, L: Observations de M. Pasteur, relatives à la Communication de M. Piutti. In: Comptes rendus. 103. Jahrgang, 1886, S. 138 (französisch, bnf.fr).
- ↑ Ohloff G: Chemistry of odor stimuli. In: Experientia. 42. Jahrgang, Nr. 3, März 1986, S. 271–279, PMID 3514264 (englisch).
- ↑ Hans-Dieter Belitz, Werner Grosch, Peter Schieberle: Lehrbuch der Lebensmittelchemie. 5. Auflage, Springer Verlag, 2001. ISBN 3-540-41096-1, S. 33. eingeschränkte Vorschau in der Google-Buchsuche.
- ↑ Gerhard G. Habermehl, Peter E. Hammann u. a.: Naturstoffchemie. 3. Auflage, Springer, 2008, ISBN 3-540-73732-4, S. 252. eingeschränkte Vorschau in der Google-Buchsuche.
- ↑ S. Ebel und H. J. Roth (Herausgeber): Lexikon der Pharmazie, Georg Thieme Verlag, 1987, S. 66, ISBN 3-13-672201-9.